Chimica organica/Alcheni: differenze tra le versioni
| Riga 20: | Riga 20: | ||
* <u>I gruppi alchilici sono a maggior '''rilascio elettronico''' rispetto al protone</u>, poiché ospitano gli elettroni con i quali formano legami in orbitali sp<sup>3</sup>, più protesi lontano dal nucleo rispetto all'orbitale s. |
* <u>I gruppi alchilici sono a maggior '''rilascio elettronico''' rispetto al protone</u>, poiché ospitano gli elettroni con i quali formano legami in orbitali sp<sup>3</sup>, più protesi lontano dal nucleo rispetto all'orbitale s. |
||
'''La minore stabilità della prima molecola rispetto alla seconda''' si può interpretare secondo il concetto della iperconiugazione notando come nel primo caso ci sia un solo gruppo metilico che possa formare un orbitale molecolare esteso con l'orbitale π del doppio legame, mentre nel secondo caso ce ne sono due. Secondo i nostri concetti "empirici ma utili" i carboni legati con doppi legami sono ibridati sp<sup>2</sup> e sono pertanto a minore rilascio elettronico rispetto ad un carbonio ibridato sp<sup>3</sup>, ma a maggiore rilascio elettronico rispetto ad un idrogeno. Nella prima molecola la "richiesta" di elettroni da parte dei carboni formanti il doppio legame è soddisfatta da un gruppo CH< |
'''La minore stabilità della prima molecola rispetto alla seconda''' si può interpretare secondo il concetto della iperconiugazione notando come nel primo caso ci sia un solo gruppo metilico che possa formare un orbitale molecolare esteso con l'orbitale π del doppio legame, mentre nel secondo caso ce ne sono due. Secondo i nostri concetti "empirici ma utili" i carboni legati con doppi legami sono ibridati sp<sup>2</sup> e sono pertanto a minore rilascio elettronico rispetto ad un carbonio ibridato sp<sup>3</sup>, ma a maggiore rilascio elettronico rispetto ad un idrogeno. Nella prima molecola la "richiesta" di elettroni da parte dei carboni formanti il doppio legame è soddisfatta da un gruppo CH<sub>3</sub>; nel secondo caso da due gruppi CH<sub>3</sub>. |
||
La minore stabilità della '''terza molecola rispetto alla quarta''' è interpretabile in modo simile a quanto appena visto. |
La minore stabilità della '''terza molecola rispetto alla quarta''' è interpretabile in modo simile a quanto appena visto. |
||
Versione delle 11:48, 24 mar 2010
Definizioni
Quando una catena carboniosa è caratterizzata da più doppi legami, questi possono essere isolati, quando tra l'uno e l'altro ci siano più legami semplici, coniugati, quando siano distanziati da un solo legame semplice, o condensati, quando un medesimo carbonio regga due doppi legami.
Stabilità relativa degli alcheni monoinsaturi
| Stabilità relativa di alcuni isomeri |
|---|

|
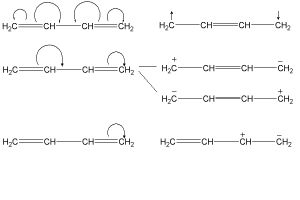
Il confronto tra le reazioni schematizzate a destra permette di introdurre l'effetto di stabilizzazione delle molecole detto di iperconiugazione. Il concetto di iperconiugazione non è particolarmente complesso, eppure viene spesso snobbato da molti autori di libri di chimica organica. Per usare le parole che R.C. Ferreira scrisse nel 1952 per il Journal of Chemical Education:
La iperconiugazione consiste nella interazione degli elettroni di un legame σ (di solito C-H o C-C) con un orbitale p vuoto o parzialmente riempito che può essere non impegnato in legami o di antilegame oppure con un orbitale π riempito. Tale interazione origina un orbitale molecolare esteso che aumenta la stabilità del sistema.
In realtà il concetto di iperconiugazione viene spesso by-passato alla grande, sostituito dai seguenti concetti non particolarmente rigorosi da un punto di vista chimico, ma molto utili al fine di predire corretamente il comportamento di molte molecole in comuni reazioni chimiche:
- Gli elettroni che si trovano in orbitali sp2 sono trattenuti maggiormente rispetto a quelli ospitati in orbitali sp3. Questo dato sperimentale è qualitativamente interpretato notando come gli orbitali s siano più raccolti attorno al nucleo rispetto ai p e che un orbitale sp3 sia il risultato della combinazione lineare di un orbitale s con un numero maggiore di orbitali p rispetto ad un sp2.
- I gruppi alchilici sono a maggior rilascio elettronico rispetto al protone, poiché ospitano gli elettroni con i quali formano legami in orbitali sp3, più protesi lontano dal nucleo rispetto all'orbitale s.
La minore stabilità della prima molecola rispetto alla seconda si può interpretare secondo il concetto della iperconiugazione notando come nel primo caso ci sia un solo gruppo metilico che possa formare un orbitale molecolare esteso con l'orbitale π del doppio legame, mentre nel secondo caso ce ne sono due. Secondo i nostri concetti "empirici ma utili" i carboni legati con doppi legami sono ibridati sp2 e sono pertanto a minore rilascio elettronico rispetto ad un carbonio ibridato sp3, ma a maggiore rilascio elettronico rispetto ad un idrogeno. Nella prima molecola la "richiesta" di elettroni da parte dei carboni formanti il doppio legame è soddisfatta da un gruppo CH3; nel secondo caso da due gruppi CH3.
La minore stabilità della terza molecola rispetto alla quarta è interpretabile in modo simile a quanto appena visto.
I nostri concetti "empirici ma utili" si devono arrendere nel confronto tra seconda e terza molecola, dato che i carboni del doppio legame sono uniti ad uno stesso numero di gruppi metilici. Il concetto della iperconiugazione, invece, offre una valida interpretazione all'osservazione sperimentale. Nella terza molecola i legami sigma tra i carboni sp2 e i rispettivi gruppi metilici sono paralleli tra loro, mentre nella quarta formano un angolo di 120°. Gli orbitali che il legame π forma con i legami σ si possono nel primo caso sovrapporre, dando origine ad un orbitale molecolare che si estende lungo l'intera molecola, conferendole una certa stabilità.
Le nostre considerazioni "empiriche ma utili" torneranno comode anche nell'interpretazione della scala di acidità di alcani, alcheni e alchini, che verrà discussa in una prossima sezione.
Stabilità relativa degli alcheni diinsaturi con doppi legami coniugati
Bibliografia