Laboratorio di chimica in casa/Approfondimento: Elettrolisi
L'elettrolisi è il processo chimico mediante il quale si trasformano gli ioni di un sale, fuso o sciolto in un solvente, in specie chimiche neutre, tramite il passaggio di corrente elettrica.
Pratica
[modifica | modifica sorgente]
Per avviare un processo elettrolitico sarà necessario semplicemente introdurre i poli di una batteria o di un generatore di corrente continua in una soluzione di acqua e di un sale.
I fattori che entrano in gioco possono essere vari, ma sono rari i casi in cui sono necessari parametri standard per avviare un'elettrolisi, basta sapere che:
- Il materiale di cui sono fatti gli elettrodi influisce molto sull'esito della reazione elettrochimica;
- La quantità di corrente impiegata cambia il tempo in cui avviene la reazione;
- La quantità di sale disciolto in acqua modifica la conduttività della soluzione
- Il tipo del sale disciolto in acqua fa variare, tra le altre cose, anche il tempo di reazione.
A seguito dell'introduzione degli elettrodi (e quindi della corrente elettrica) nella soluzione, si noteranno sviluppo di gas ad uno o ad entrambi i poli, e si potrà osservare che:
- L'anodo si consuma.
- Il catodo si ingrossa.
Lo sprigionamento di gas è spiegato dal fatto che durante il passaggio da ione a specie chimica che avviene agli elettrodi, accadono varie reazioni intermedie, in cui la singola specie chimica si trasforma in gas, si decompone producendo composti gassosi secondari o si lega all'acqua di soluzione, producendo idrossidi con rilascio di idrogeno.
I due elettrodi invece cambiano d'aspetto per due motivi: Il catodo si ingrossa solo nelle reazioni redox con un metallo, perché cedendo l'elettrone allo ione positivo, questo tenderà a depositarsi su di lui. Man mano che arriveranno altri ioni metallici si legheranno anch'essi al metallo sottostante formando una placca che varia di aspetto e consistenza a seconda del tipo di metallo e della velocità di reazione.
L'anodo invece si consuma perché tenderà a legarsi con le specie chimiche con cui viene a contatto formando molecole di altri sali che andranno in soluzione, riducendo sempre più le dimensioni dell'elettrodo. Questa continua disgregazione in alcuni casi provoca il distacco di frammenti dell'elettrodo anche senza legarsi con gli ioni. Può succedere usando elettrodi di grafite, di carta di alluminio ecc.
Precauzioni
[modifica | modifica sorgente]Durante ogni reazione elettrolitica è bene avere alcuni accorgimenti:
- Badare che i poli della batteria e/o degli elettrodi non vengano a contatto, facendo cortocircuito;
- Non utilizzare recipienti di metallo;
- Pulire elettrodi e recipiente prima dell'elettrolisi;
- Utilizzare materiali di cui si conosce la composizione esatta;
- Non eseguire l'esperimento al chiuso (si sprigionano sempre dei gas).
- Informarsi sulle proprietà del sale che si sta manipolando, per prevederne il comportamento durante l'elettrolisi.
Meccanismo
[modifica | modifica sorgente]Le molecole dei sali idrosolubili, se sciolti in acqua si scindono in due specie chimiche, dette ioni. Questo processo è detto dissociazione, nel quale gli ioni vengono accerchiati da un numero imprecisato di molecole d'acqua, attraverso il legame a dipolo.
A causa del legame ionico, una delle due parti tratterrà l'elettrone dell'altra dopo la separazione, assumendo permanentemente la carica negativa della compagna. Essendo caricata negativamente, esposta ad un campo elettrico la molecola seguirà il corso della corrente elettrica, spostandosi a gran velocità verso il polo positivo, detto anodo. Per questo la specie chimica che viene da esso attirata è denominata anione. Al contrario, la parte positiva è attirata dal polo negativo detto catodo e per questo la specie chimica viene detta catione.
A contatto con i due poli della batteria avviene un processo redox in cui l'anione cede il suo elettrone all'anodo, perdendo la carica negativa precedentemente strappata alla controparte più elettropositiva, mentre al polo negativo il catodo cede un suo elettrone al catione (il quale, se è un metallo, si trasforma appunto in atomo metallico e si deposita sul catodo) trasformandosi anch'esso da ione (positivo) a specie chimica neutra.
Leggi di Faraday
[modifica | modifica sorgente]Nei primi anni seguenti la scoperta dell'elettrolisi, lo scienziato Michael Faraday eseguì una serie di misurazioni riguardanti la quantità di corrente che passava attraverso gli elettrodi e gli effetti che questa produceva, scoprendo che:
La massa di una sostanza prodotta in corrispondenza di un elettrodo durante l'elettrolisi è direttamente proporzionale alla quantità di carica trasferita a quell'elettrodo.
Significa che aumentando la quantità di corrente elettrica aumenta anche la quantità di sostanza che si deposita agli elettrodi, e diminuendola diminuirà con essa anche la quantità di sostanza depositata, in maniera costante.
Analizzò poi gli effetti dell'elettrolisi su sali diversi e scoprì che fornendo ad ognuno la medesima quantità di corrente il processo era più lento o veloce a seconda del sale che si stava manipolando.
La medesima quantità di carica elettrica, fatta passare attraverso più soluzioni di elettroliti diversi, produce un ugual numero di equivalenti chimici (moli) di questi elettroliti.
Quest'ultima legge, nota come Seconda legge di Faraday sull'elettrolisi gli è stata utile per capire l'esatta composizione di alcuni composti chimici:
Prendendo in considerazione, per esempio, il tricloruro di alluminio ed il cloruro di sodio, si noterà che la stessa quantità di corrente fatta passare in ognuna delle soluzioni produce (anche se in tempi diversi) quantità di sostanze diverse agli elettrodi, ma esattamente uguali alle quantità di "equivalenti" chimici impiegati per la sintesi di tale sostanza. Questa constatazione fu la "culla" che permise di collegare le quantità di sostanze impiegate in una reazione chimica ed il rapporto in cui si combinano fra loro, tramite il termine mole.
Questa parte del racconto prosegue nella pagina Approfondimento: Mole.
Col tempo questi principi vennero analizzati nel loro aspetto quantitativo, riassumendone i dati nella seguente formula generale:
è il numero di moli di sostanza depositata all'elettrodo.
è l'intensità della corrente applicata all'elettrodo.
è la valenza degli ioni.
è la costante di Faraday = 96.485,339 C/mol.
Questa formula ci è molto utile, perché permette di ricavare il tempo di reazione, la quantità di corrente da impiegare, la quantità di moli di sostanza sprigionata al secondo ed altro ancora. qualsiasi altro calcolo utile a risolvere un problema, sapendo in anticipo quali dati inserire in tabella per ricavare l'incognita che si cerca.
Formula derivata
[modifica | modifica sorgente]
Possiamo riplasmare l'equazione riassuntiva delle leggi di Faraday in una formula più semplice, il cui valore da trovare può essere il tempo di reazione, la quantità di corrente da impiegare o la quantità di moli sprigionate in un certo tempo impiegando una certa quantità di corrente.
- Incognita tempo
In questo primo caso è mostrato come ricavare il tempo in cui avverrà la reazione.
Il tempo impiegato è uguale al numero di moli di sostanza moltiplicate per la valenza dello ione da ridurre o ossidare per 1 Faraday, tutto diviso per l'intensità di corrente
Trasformando le unità derivate in semplici sarà chiara la logica del calcolo:
Adesso riprendiamo i dati da inserire in tabella: la costante di Faraday è 96 485 A/(mol·s), la quantità di moli con cui si lavora è 1 mol, l'intensità di corrente che viene fornita alla soluzione è 1 A e si esegue l'elettrolisi del cloruro di sodio, nel quale la valenza di entrambi gli ioni è 1. Si considerano nulli le eventuali resistenze elettriche, gli sbalzi di temperatura ecc.
- Valenza ionica maggiore.
Questa sezione è ancora vuota; aiutaci a scriverla! |
Alla formula per ricavare il tempo in cui avviene la reazione manca una delle incognite presenti nella legge di Faraday: la valenza ionica .
Aumentando la valenza degli ioni in soluzione aumenterà anche la quantità di carica elettrica da somministrargli perché necessitano di più elettroni per diventare atomi neutri, e di conseguenza aumenta anche il tempo.
Per far passare ad atomo neutro 1 mol di ioni monovalenti in 1 secondo occorre 1 F, mentre per neutralizzare ioni bivalenti ne occorreranno due, per ioni trivalenti tre e così via, per questo il numero di F aumenta di z volte a seconda del sale che si elettrolizza.
Storia
[modifica | modifica sorgente]
La prima reazione elettrolitica venne praticata per la prima volta poco tempo dopo l'invenzione, da parte di Alessandro Volta, della sua famosa pila elettrica: Il chirurgo Anthony Carlisle volle riprodurre l'esperimento di Volta costruendo da sé una pila zinco-argento. Quando immerse i due poli nell'acqua vide che in prossimità di essi si formavano delle bolle di gas, che vennero in seguito identificate da Johann Wilhelm Ritter come idrogeno e ossigeno.
All'epoca, Sir Humphry Davy era un chimico membro della Royal Society, la prima e più prestigiosa società di filosofia naturale al mondo.
Venne a conoscenza degli studi di Ritter sull'elettrolisi dell'acqua, e volle sperimentare anche lui tale reazione chimica.
Fece test di alta precisione, a seguito dei quali confermò la sua teoria: quell'energia che scaturisce quando si rompe quello stato di equilibrio in cui si trova nei due metalli e che fluisce all'interno dell'acqua e nel corpo delle rane durante gli esperimenti di Galvani, rompe anche l'equilibrio che tiene legati assieme gli atomi costituenti la materia.
Dapprima provò a far passare corrente attraverso soluzioni di composti che non permettevano il passaggio di corrente elettrica, ma quando provò a scindere le molecole di potassa caustica fusa, scoprì un metallo nuovo, estremamente reattivo, di cui mostrò le prime proprietà di fronte ai membri della Royal Society stupiti e che chiamò potassio.
Incantato da questo nuovo potere che lui paragonava al potentissimo solvente magico dell'alkahest, costruì una gigantesca pila zinco-argento di lunghissima durata, con cui intraprese gli studi in cui scoprì buona parte degli elementi della tabella periodica, tra cui sodio, magnesio, stronzio, calcio e bario.
Nel 1812, Davy rimase accecato da un'esplosione avvenuta nel suo laboratorio, che lo costrinse a trovare un assistente che lo aiutasse nelle ricerche. Scelse un suo "ammiratore", un giovane apprendista rilegatore che aveva assistito a molte delle sue conferenze, Michael Faraday, ventenne curioso e intelligente i cui contributi fecero avanzare soprattutto la fisica, nell'ambito dell' elettromagnetismo.
Fra le molte cose, Faraday è ricordato per l'aver enunciato le due leggi dell'elettrolisi.
I contributi di Davy e Faraday furono estremamente preziosi ed influenzarono molti scienziati e filosofi dell'epoca, ed aprirono la via a due nuove branche della chimica: la teoria atomica e l'elettrochimica industriale, oltre alle teorie del campo elettrico e magnetico dalla parte della fisica e l'invenzione di apparecchi, processi e composti chimici nuovi.
Cronologia dei processi elettrolitici industriali
[modifica | modifica sorgente]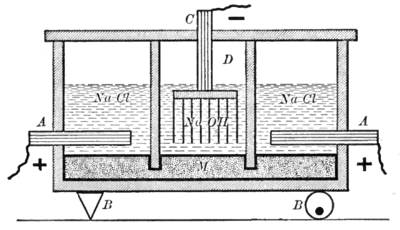
- Uno dei primi esperimenti sull'elettrolisi dei sali metallici, avvenuto nel 1800, diede vita al moderno processo di galvanostegia o placcatura, denominazione generica che indica processi come la ramatura, l'argentatura, la zincatura, la cromatura ed il placcaggio in oro o rodio.
- Uno dei più famosi processi elettrochimici è quello di Hall-Héroult, risalente al 1886, adibito ad estrarre elettroliticamente l'alluminio dall'allumina (Ossido di alluminio Al2O3). L'alluminio ebbe grande successo durante i primi tempi della sua produzione: venne valutato come metallo prezioso fino agli inizi del '900, e stimato per la sua lucentezza e leggerezza.
- Contemporaneamente al processo di Hall-Héroult venne introdotto in Inghilterra il processo Castner in cui si faceva fondere l' idrossido di sodio in un crogiolo di acciaio a 330 °C e si provvedeva a svolgerne l'elettrolisi. Il sodio fuso prodotto veniva aspirato e conservato sotto formalina. Venne soppiantato nel 1962 dal processo di Downs che prevedeva l'estrazione di sodio dal suo cloruro fatto fondere in un crogiolo assieme a cloruro di calcio a circa 600 °C.
- Lo stesso processo è valido per la produzione di bario e stronzio.
- Un processo elettrochimico industriale molto diffuso è il processo cloro-soda; introdotto nel 1892, impiega il cloruro di sodio come elettrolita per produrre soda caustica, cloro e idrogeno.
Fonti esterne
[modifica | modifica sorgente]Qui viene spiegata ancora più dettagliatamente la storia dell'elettrolisi e della pila di Volta:









