Laboratorio di chimica in casa/Acido solforico: differenze tra le versioni
| Riga 134: | Riga 134: | ||
KNO<sub>3</sub> + H<sub>2</sub>SO<sub>4</sub> → KHSO<sub>4</sub> + HNO<sub>3</sub>↑ (Ka = 25,1) |
KNO<sub>3</sub> + H<sub>2</sub>SO<sub>4</sub> → KHSO<sub>4</sub> + HNO<sub>3</sub>↑ (Ka = 25,1) |
||
I bisolfati conservano le proprietà acide dell'anione bisolfato,<ref>Una soluzione 1M di |
I bisolfati conservano le proprietà acide dell'anione bisolfato,<ref>Una soluzione 1M di NaHSO<sub>4</sub> presenta pH inferiore ad 1. Si veda la voce su en.Wikipedia [[w:en:Sodium bisulfate|sodium bisulfate]].</ref> e reagiscono con le basi ed i sali degli acidi deboli dando i rispettivi solfati. |
||
CaCO<sub>3</sub> + 2 NaHSO<sub>4</sub> → CaSO<sub>4</sub>↓ + Na<sub>2</sub>SO<sub>4</sub> + CO<sub>2</sub>↑ + H<sub>2</sub>O |
CaCO<sub>3</sub> + 2 NaHSO<sub>4</sub> → CaSO<sub>4</sub>↓ + Na<sub>2</sub>SO<sub>4</sub> + CO<sub>2</sub>↑ + H<sub>2</sub>O |
||
Versione delle 16:31, 28 ago 2013

L'acido solforico è sicuramente l'acido più utile in laboratorio, perché permette di ottenere da moltissimi sali i rispettivi acidi, oltre ad essere il catalizzatore di molte reazioni diverse (idrolisi, deidratazione, nitrazione, esterificazione, ...).
Viene commercializzato in concentrazione tra il 94% e il 98% (molto concentrato) sia come prodotto da laboratorio che come sgorgante, o diluito in concentrazione tra il 30% e il 40% come acido per le batterie al piombo.
L'acido solforico concentrato è estremamente corrosivo: corrode la carta, i tessuti, il PET e reagisce violentemente con l'acqua e le sostanze basiche. Reagisce con numerosissime sostanze diverse e spesso da queste reazioni si liberano gas tossici.
Caratteristiche chimico-fisiche




L'acido solforico è un liquido denso (1,84 g/cm3 al 100%) dall'alto punto di ebollizione ed è anche un buon conduttore elettrico.
Quando viene versato nell'acqua libera tantissimo calore, precipitando sul fondo senza sciogliersi subito.
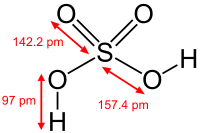
I legami dativi tra l'atomo di zolfo e quelli di ossigeno sono lunghi 142 pm e sono molto stabili, come quelli covalenti tra gli altri due ossigeni, che sono lunghi 154 pm per via della carica negativa proveniente dagli atomi di idrogeno, la cui distanza da quelli di ossigeno è 97 pm.
L'acido solforico è un acido forte, più forte dell'acido nitrico e dell'acido cloridrico; tuttavia solo il primo protone è sempre dissociato in soluzione, al contrario dell'altro avente Ka di un acido debole (simile a quella dell' acido ossalico):
H2SO4 + H2O ↔ HSO4- + H3O+ Ka1 = 106
HSO4- + H2O ↔ SO42- + H3O+ Ka2 = 10-2
Esso è un buon conduttore di corrente poiché (nelle sue soluzioni prossime al 100%) parte delle molecole di H2SO4 si dissociano (autoprotolisi) come quelle dell'acqua, anche se in numero molto maggiore:[1]
2 H2SO4 ↔ HSO4- + H3SO4+ Kapl = 2,7·10-4
2 H2O ↔ H3O+ + OH- Kapl = 10-14
Come detto in precedenza, l'acido solforico è una molecola molto stabile, e le sue proprietà ossidanti sono minime.[2] Ad alte temperature l'acido solforico mostra le proprie proprietà ossidanti con metalli poco reattivi come rame e stagno:[3]
Cu + 2 H2SO4 → CuSO4 + SO2 + 2 H2O
Sn + 2 H2SO4 → SnSO4 + SO2 + 2 H2O
I solfati possono anche essere calcinati per dare solfuri ed anidride carbonica.[4]
MeSO4 + 2 C → MsS + 2 CO2
La sua capacità di separarsi dal suo primo protone rimane comunque la più sfruttata, rendendo l'acido solforico un catalizzatore e reagente indispensabile in innumerevoli reazioni chimiche.
Proprietà corrosive
L'acido solforico è ben conosciuto per le sue capacità corrosive. Esso infatti è in grado di corrodere un'innumerevole quantità di oggetti, tra cui il marmo, la stoffa, i metalli ed alcuni tipi di plastica.
Le reazioni che avvengono in questi casi possono essere o reazioni di doppio scambio, in cui l'acido partecipa come reagente, o di idrolisi acida, dove non funge da reagente bensì da catalizzatore.
Queste sono alcune delle reazioni che avvengono quando l'acido solforico corrode qualcosa:
| Materiale corroso |
Reazione | Commento |
|---|---|---|
| Marmo Calce Cemento |
CaCO3 + H2SO4 → CaSO4↓ + H2O + CO2↑ | Reazione di doppio scambio tra carbonato di calcio ed acido solforico. |
| Cotone Carta Jeans |
 + H2O 2 + H2O 2  |
Idrolisi dei legami glicosidici presenti nelle molecole di cellulosa che compongono alcuni tessuti vegetali. I prodotti sono molecole di glucosio. |
| PET |  + H2O + H2O |
Idrolisi del polietilene tereftalato che costituisce la plastica delle bottiglie. I prodotti sono acido tereftalico e glicole etilenico. |
| Lana Seta Nylon |
 + H2O + H2O  + +  |
Idrolisi dei legami peptidici presenti nelle proteine o nelle fibre di poliammidi che compongono diverse plastiche e tessuti. |
| Metalli | Fe + H2SO4 → FeSO4 + H2↑ Pb + H2SO4 → PbSO4↓ + H2↑ 2 Al + 3 H2SO4 → Al2(SO4)3 + 3 H2↑ Cu + H2SO4 → CuSO4 + H2↑ Sn + H2SO4 → SnSO4 + H2↑ |
L'acido solforico corrode molti metalli a temperatura ambiente tra cui Fe, Pb, Al e ad alte temperature anche Cu, Sn e varie leghe, aciaio inox compreso, sviluppando idrogeno e calore. |
Proprietà chimiche utili
| Densità delle soluzioni acquose | |||
|---|---|---|---|
| P/P% H2SO4 |
Molarità | Densità () |
° Bé |
| 0,261 | 0,027 | 1,000 | 0 |
| 7,704 | 0,825 | 1,050 | 6,87 |
| 14,73 | 1,652 | 1,100 | 13,12 |
| 21,38 | 2,507 | 1,150 | 18,82 |
| 27,72 | 3,302 | 1,200 | 24,05 |
| 33,82 | 4,310 | 1,250 | 28,86 |
| 39,68 | 5,259 | 1,300 | 33,3 |
| 45,26 | 6,229 | 1,350 | 37,42 |
| 50,50 | 7,208 | 1,400 | 41,23 |
| 55,45 | 8,198 | 1,450 | 44,79 |
| 60,17 | 9,202 | 1,500 | 48,11 |
| 64,71 | 10,23 | 1,550 | 51,21 |
| 69,09 | 11,27 | 1,600 | 54,12 |
| 73,37 | 12,43 | 1,650 | 56,85 |
| 77,63 | 13,46 | 1,700 | 59,43 |
| 82,09 | 14,65 | 1,750 | 61,85 |
| 87,69 | 16,09 | 1,800 | 64,14 |
L'acido solforico ha proprietà chimiche estremamente utili ed interessanti. Essendo uno degli acidi minerali più forti è in grado di partecipare ad innumerevoli reazioni di doppio scambio. La maggior parte dei suoi sali sono solubili, eccetto il solfato di piombo PbSO4 e quello di ferro(III) Fe2(SO4)3 (sempre parlando di quelli sintetizzabili in casa). La sua forza acida lo rende anche un catalizzatore estremamente versatile in innumerevoli reazioni organiche ed inorganiche.
Sintesi di altri acidi
Questa sezione è ancora vuota; aiutaci a scriverla! |
Bisolfati
Come detto in precedenza, l'acido solforico tende a dissociarsi in acqua dando H3O+ + HSO4-. Non è però altrettanto disposto a dissociarsi nello ione solfato SO42-, e quindi possiede due Ka diverse:
H2SO4 + H2O ↔ HSO4- + H3O+ Ka1 = 106
HSO4- + H2O ↔ SO42- + H3O+ Ka2 = 10-2
Questa caratteristica gli permette di creare sali idrogenati stabili detti idrogenosolfati o bisolfati quando reagisce con sali di metalli alcalini combinati con acidi aventi Ka superiore a 10-2:
NaCl + H2SO4 → NaHSO4 + HCl↑ (Ka = 107)
KNO3 + H2SO4 → KHSO4 + HNO3↑ (Ka = 25,1)
I bisolfati conservano le proprietà acide dell'anione bisolfato,[5] e reagiscono con le basi ed i sali degli acidi deboli dando i rispettivi solfati.
CaCO3 + 2 NaHSO4 → CaSO4↓ + Na2SO4 + CO2↑ + H2O
NH4OH + KHSO4 → Na(NH4)SO4 + H2O
I bisolfati sono molto usati nelle scuole a fini didattici,come additivi alimentari e per controllare il pH delle soluzioni tampone.
Idrolisi
Questa sezione è ancora vuota; aiutaci a scriverla! |
Deidratazione
Questa sezione è ancora vuota; aiutaci a scriverla! |
Sintesi
Questa sezione è ancora vuota; aiutaci a scriverla! |
Note
- ↑ Si veda su en.Wikipedia Sulfuric acid.
- ↑ Si confronti con l'acido nitrico, l'acido clorico e l'acido perclorico.
- ↑ Si veda su en.Wikipedia Sulfuric acid.
- ↑ Questa reazione viene sfruttata per ottenere i solfuri dei metalli alcalino-terrosi (per esempio solfuro di stronzio.)
- ↑ Una soluzione 1M di NaHSO4 presenta pH inferiore ad 1. Si veda la voce su en.Wikipedia sodium bisulfate.



