Termodinamica classica/Cicli termodinamici
Un ciclo termodinamico è definito come una serie di trasformazioni termodinamiche che riportano il sistema allo stato iniziale. Ci sono diversi tipi di cicli, ne studieremo due tipi caratteristici.
Ciclo di politropiche
[modifica | modifica sorgente]Consideriamo un ciclo composto da quattro trasformazioni a due a due accoppiate, che siano politropiche, ovvero del tipo . Consideriamo le quattro trasformazioni singolarmente; distingueremo i due tipi di politropiche con diversi esponenti e . Le leggi che regolano le quattro trasformazioni, che passano per i quattro stati termodinamici sono dunque:
Moltiplichiamo tutte queste espressioni, ottenendo ; rimettendo le cose in ordine:
Ovvero il prodotto dei volumi opposti nel ciclo è uguale a due a due, così come resta uguale il fattore di compressione del ciclo, ovvero . Questa è una caratteristica di tutte le politropiche e dei cicli formati da quattro politropiche accoppiate.
Prima di procedere, vediamo l'espressione del calore specifico di una politropica generica. Data la legge , quale sarà il rispettivo calore specifico ? Ricordiamo che vale
Valutiamo l'espressione di per la politropica:
Ora sfruttiamo questa espressione sostituendola nella legge del gas perfetto, opportunamente differenziata:
Sostituendola nella formula per otteniamo:
Ciclo di Carnot
[modifica | modifica sorgente]Il più famoso dei cicli termodinamici è il ciclo di Carnot, composto da due isoterme e due adiabatiche tutte reversibili. Nel piano è rappresentato come nell'immagine seguente.
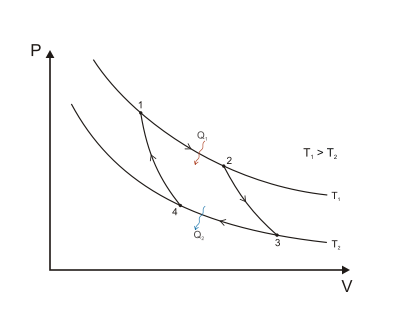
Le isoterme sono a temperatura e , con .
Calcoliamoci lavoro compiuto/subito e calore ceduto/assorbito per ogni trasformazione:
Il lavoro totale compiuto dal ciclo sarà pari a:
Sfruttando la caratteristica dei cicli di politropiche discussa poco sopra, abbiamo che , quindi otteniamo che il lavoro totale del ciclo è pari a
Per compiere questo lavoro, ovviamente, è stato ceduto al sistema del calore, che assorbe calore solo nella trasformazione . Quando si ha a che fare con un ciclo termodinamico è ininfluente parlare di lavoro compiuto, in quanto si deve cedere del calore al sistema per compierlo; allora un termine di confronto tra cicli è il rendimento, un numero adimensionale definito come:
Questo valore è compreso . Il ciclo di Carnot, in particolare, lavora tra due sorgenti, per essere più precisi, lavora con sole due sorgenti, ed è reversibile; per queste caratteristiche, è unico nel suo genere e presenta un rendimento altissimo. Infatti, in base a quanto calcolato prima, possiamo esprimere il rendimento come:
Come vedremo col secondo principio, questo valore è il limite superiore per il rendimento di macchine termiche.
Discutiamo brevemente la validità del rendimento. Questo è definito bene per valori del lavoro positivi , dall'espressione vista poco fa abbiamo che
Ora, sul calore assorbito c'è libertà assoluta, ma sul calore ceduto no. Infatti, se il lavoro è negativo, il rendimento non è ben definito, o meglio, ha poco senso una macchina termica a rendimento negativo. Per questo abbiamo due casi limite:
Quindi otteniamo che ; come vedremo col secondo principio, non potremo però avere un rendimento esattamente uguale a 1.































