Biologia per il liceo/Il metabolismo cellulare
Introduzione
[modifica | modifica sorgente]La membrana plasmatica inoltre non è un semplice contenitore. Essa ha molte funzioni, ma la più basilare è quella di definire i confini della cellula e mantenerla funzionale. La membrana plasmatica è selettivamente permeabile. Ciò significa che la membrana consente ad alcuni materiali di entrare o uscire liberamente dalla cellula, mentre altri materiali non possono muoversi liberamente, ma richiedono una struttura specializzata e, occasionalmente, persino un investimento energetico per l'attraversamento.
Entrando dentro la cellula, praticamente ogni compito svolto dalla cellula richiede energia. Gli organismi hanno bisogno di energia per svolgere lavori pesanti ed esercizi, ma gli esseri umani usano anche molta energia mentre pensano e persino durante il sonno. Le cellule viventi di ogni organismo usano costantemente energia. Gli organismi importano nutrienti e altre molecole. Metabolizzano (scompongono) e possibilmente sintetizzano in nuove molecole. Se necessario, le molecole si modificano, si muovono nella cellula e possono distribuirsi all'intero organismo. Ad esempio, le grandi proteine che compongono i muscoli sono costruite attivamente da molecole più piccole. I carboidrati complessi si scompongono in zuccheri semplici che la cellula usa per produrre energia. Proprio come l'energia è necessaria sia per costruire che per demolire un edificio, l'energia è necessaria per sintetizzare e scomporre le molecole. Inoltre, le molecole di segnalazione come ormoni e neurotrasmettitori trasportano tra le cellule. Le cellule ingeriscono e scompongono batteri e virus. Le cellule devono anche esportare rifiuti e tossine per rimanere sane e molte cellule devono nuotare o spostare i materiali circostanti tramite il movimento pulsante di appendici cellulari come ciglia e flagelli.
I processi cellulari che abbiamo elencato sopra richiedono un apporto costante di energia. Da dove e in quale forma proviene questa energia? Come ottengono energia le cellule viventi e come la usano? Questo capitolo discuterà le diverse forme di energia e le leggi fisiche che governano il trasferimento di energia. Questo capitolo descriverà anche come le cellule usano l'energia e la ripristinano, e come le reazioni chimiche nella cellula funzionano con grande efficienza.
La membrana plasmatica
[modifica | modifica sorgente]La membrana plasmatica, la membrana cellulare, ha molte funzioni, ma la più basilare è quella di definire i confini della cellula e mantenerla funzionale. La membrana plasmatica è selettivamente permeabile. Ciò significa che la membrana consente ad alcuni materiali di entrare o uscire liberamente dalla cellula, mentre altri materiali non possono muoversi liberamente, ma richiedono una struttura specializzata e, occasionalmente, persino un investimento energetico per l'attraversamento.
La membrana plasmatica di una cellula definisce la cellula, ne delinea i confini e determina la natura della sua interazione con l'ambiente (vedere la Tabella 5.1 per un riepilogo). Le cellule escludono alcune sostanze, ne assorbono altre ed espellono altre ancora, il tutto in quantità controllate. La membrana plasmatica deve essere molto flessibile per consentire a certe cellule, come i globuli rossi e bianchi, di cambiare forma mentre passano attraverso stretti capillari. Queste sono le funzioni più evidenti della membrana plasmatica. Inoltre, la superficie della membrana plasmatica trasporta marcatori che consentono alle cellule di riconoscersi a vicenda, il che è fondamentale per la formazione di tessuti e organi durante lo sviluppo precoce e che in seguito svolge un ruolo nella distinzione tra "self" e "non-self" della risposta immunitaria.
Tra le funzioni più sofisticate della membrana plasmatica c'è la capacità delle proteine complesse e integrali, i recettori, di trasmettere segnali. Queste proteine agiscono sia come ricevitori di input extracellulari che come attivatori di elaborazione intracellulare. Questi recettori di membrana forniscono siti di attacco extracellulare per effettori come ormoni e fattori di crescita e attivano cascate di risposta intracellulare quando i loro effettori sono legati. Occasionalmente, i virus dirottano i recettori (l'HIV, virus dell'immunodeficienza umana, è un esempio) che li usano per entrare nelle cellule e, a volte, i geni che codificano i recettori mutano, causando il malfunzionamento del processo di trasduzione del segnale con conseguenze disastrose.
Modello di mosaico fluido
[modifica | modifica sorgente]La spiegazione, il modello del mosaico fluido , si è evoluta un po' nel tempo, ma è ancora la migliore spiegazione della struttura e della funzione della membrana plasmatica come le intendiamo oggi. Il modello del mosaico fluido descrive la struttura della membrana plasmatica come un mosaico di componenti, tra cui fosfolipidi, colesterolo, proteine e carboidrati, che conferisce alla membrana un carattere fluido. Le membrane plasmatiche variano da 5 a 10 nm di spessore. Per fare un confronto, i globuli rossi umani, visibili tramite microscopia ottica, sono larghi circa 8 µm, ovvero circa 1.000 volte di più di una membrana plasmatica. La membrana assomiglia un po' a un sandwich ( Figura 1 ).

I componenti principali di una membrana plasmatica sono lipidi (fosfolipidi e colesterolo), proteine e carboidrati legati ad alcuni dei lipidi e delle proteine. Un fosfolipide è una molecola composta da glicerolo, due acidi grassi e un gruppo di testa legato al fosfato. Il colesterolo, un altro lipide composto da quattro anelli di carbonio fusi, è situato accanto ai fosfolipidi nel nucleo della membrana. Le proporzioni di proteine, lipidi e carboidrati nella membrana plasmatica variano a seconda del tipo di cellula, ma per una tipica cellula umana, le proteine rappresentano circa il 50 percento della composizione in massa, i lipidi (di tutti i tipi) rappresentano circa il 40 percento e i carboidrati comprendono il restante 10 percento. Tuttavia, la concentrazione di proteine e lipidi varia a seconda delle diverse membrane cellulari. Ad esempio, la mielina, una crescita della membrana delle cellule specializzate che isola gli assoni dei nervi periferici, contiene solo il 18 percento di proteine e il 76 percento di lipidi. La membrana interna mitocondriale contiene il 76 percento di proteine e solo il 24 percento di lipidi. La membrana plasmatica dei globuli rossi umani è composta per il 30 percento da lipidi. I carboidrati sono presenti solo sulla superficie esterna della membrana plasmatica e sono legati alle proteine, formando glicoproteine , o legati ai lipidi, formando glicolipidi .
-
Fig. 1B (vedi sotto la spiegazione)
-
Schema della struttura della membrana
-
struttura della membrana
-
Altro schema della membrana
-
Diversi tipi di fosfolipidi
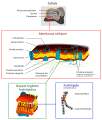
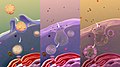
Nel primo disegno in galleria abbiamo :A Spazio intracellulare o citosol - B Spazio extracellulare o lume della vescicola/apparato del Golgi - 1: Membrana non-raft - 2: Zattera lipidica - 3: Proteina transmembrana associata alla zattera lipidica - 4: Proteina di membrana non-raft - 5: Modifiche della glicosilazione (su glicoproteine e glicolipidi) - 6: Proteina ancorata al GPI - 7: Colesterolo - 8: Glicolipide
Fosfolipidi
[modifica | modifica sorgente]Il tessuto principale della membrana è costituito da molecole anfipatiche (o anfifiliche), fosfolipidiche. Le aree idrofile o "amanti dell'acqua" di queste molecole (che sembrano una raccolta di palline in una resa artistica del modello) ( Figura 1) sono a contatto con il fluido acquoso sia all'interno che all'esterno della cellula. Le molecole idrofobiche , o che "odiano l'acqua", tendono a essere non polari. Interagiscono con altre molecole non polari nelle reazioni chimiche, ma generalmente non interagiscono con le molecole polari. Quando vengono poste in acqua, le molecole idrofobiche tendono a formare una palla o un cluster. Le regioni idrofile dei fosfolipidi formano legami idrogeno con l'acqua e altre molecole polari sia all'esterno che all'interno della cellula. Pertanto, le superfici della membrana che si affacciano sull'interno e sull'esterno della cellula sono idrofile. Al contrario, l'interno della membrana cellulare è idrofobico e non interagisce con l'acqua. Pertanto, i fosfolipidi formano un'eccellente membrana cellulare a due strati che separa il fluido all'interno della cellula dal fluido all'esterno della cellula.

Una molecola di fosfolipide ( Figura 2 ) è costituita da una struttura portante di glicerolo a tre atomi di carbonio con due molecole di acido grasso attaccate ai carboni 1 e 2 e un gruppo contenente fosfato attaccato al terzo atomo di carbonio. Questa disposizione conferisce alla molecola complessiva un'area di testa (il gruppo contenente fosfato), che ha un carattere polare o carica negativa, e un'area di coda (gli acidi grassi), che non ha carica. La testa può formare legami idrogeno, ma la coda no. Gli scienziati chiamano una molecola con un'area carica positivamente o negativamente e un'area non carica, o non polare, anfipatica o anfifilica o "amante dei doppi".

Questa caratteristica è fondamentale per la struttura della membrana plasmatica perché, in acqua, i fosfolipidi si dispongono con le loro code idrofobiche rivolte l'una verso l'altra e le loro teste idrofile rivolte verso l'esterno. In questo modo, formano un doppio strato lipidico, una barriera fosfolipidica a doppio strato che separa l'acqua e gli altri materiali da un lato dall'acqua e dagli altri materiali dall'altro lato. I fosfolipidi riscaldati in una soluzione acquosa di solito formano spontaneamente piccole sfere o goccioline (micelle o liposomi), con le loro teste idrofile che formano l'esterno e le loro code idrofobiche all'interno ( Figura 3 ).
Proteine
[modifica | modifica sorgente]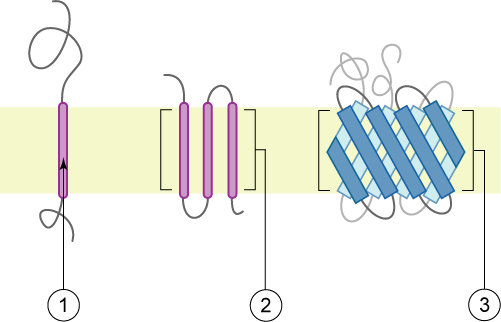
Le proteine integrali. Le proteine costituiscono il secondo componente principale delle membrane plasmatiche. Le proteine integrali , o integrine, come suggerisce il nome, si integrano completamente nella struttura della membrana e le loro regioni idrofobiche che attraversano la membrana interagiscono con la regione idrofobica del doppio strato fosfolipidico ( Figura 1). Le proteine integrali di membrana a passaggio singolo hanno solitamente un segmento transmembrana idrofobico che consiste di 20-25 amminoacidi. Alcune attraversano solo una parte della membrana, associandosi a un singolo strato, mentre altre si estendono da un lato all'altro e sono esposte su entrambi i lati. Fino a 12 segmenti proteici singoli comprendono alcune proteine complesse, che sono ampiamente ripiegate e incorporate nella membrana ( Figura 4 ). Questo tipo di proteina ha una o più regioni idrofile e una o più regioni leggermente idrofobiche. Questa disposizione delle regioni proteiche orienta la proteina lungo i fosfolipidi, con la regione idrofobica della proteina adiacente alle code dei fosfolipidi e la regione o le regioni idrofile della proteina che sporgono dalla membrana e sono a contatto con il citosol o il fluido extracellulare acquoso.
Le proteine periferiche si trovano sulle superfici esterne e interne delle membrane, attaccate alle proteine integrali o ai fosfolipidi. Le proteine periferiche, insieme alle proteine integrali, possono fungere da enzimi, da attacchi strutturali per le fibre del citoscheletro o come parte dei siti di riconoscimento della cellula. Gli scienziati a volte si riferiscono a queste come proteine "self", "specifiche delle cellule". Il corpo riconosce le proprie proteine e attacca le proteine estranee associate a patogeni invasivi.
Spesso le proteine di membrana sono associate a lipidi, formando le lipoproteine, e a zuccheri, formano le glicoproteine. In galleria ci sono degli esempi.
-
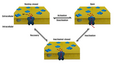
Schema delle proteine di membrana: 1: phosphlipid - 2: cholesterolo - 3:glycolipidi - 4: sugar - 5: polytopic protein (transmembrane protein) - 6: monotopic protein (here, a glycoprotein)
-
Proteine di membrana
-
Componenti del glicocalice (vedi par. sotto): A) glicolipide B) glicoproteina periferica C) glicoproteina integrale D) proteoglicano
Carboidrati
[modifica | modifica sorgente]
I carboidrati sono il terzo componente principale della membrana plasmatica. Sono sempre sulla superficie esterna delle cellule e sono legati alle proteine (formando glicoproteine) o ai lipidi (formando glicolipidi) ( Figura 1). Queste catene di carboidrati possono essere composte da 2–60 unità monosaccaridiche e possono essere dritte o ramificate. Insieme alle proteine periferiche, i carboidrati formano siti specializzati sulla superficie cellulare che consentono alle cellule di riconoscersi a vicenda. Questi siti hanno modelli unici che consentono il riconoscimento cellulare, proprio come i tratti del viso unici di ogni persona consentono agli individui di riconoscersi. Questa funzione di riconoscimento è molto importante per le cellule, poiché consente al sistema immunitario di distinguere tra cellule del corpo ("self") e cellule o tessuti estranei ("non-self"). Tipi simili di glicoproteine e glicolipidi si trovano sulla superficie dei virus e possono cambiare frequentemente, impedendo alle cellule immunitarie di riconoscerli e attaccarli.
Ci riferiamo collettivamente a questi carboidrati sulla superficie esterna della cellula, sia delle glicoproteine che dei glicolipidi, come glicocalice (che significa "rivestimento di zucchero"). Il glicocalice è altamente idrofilo e attrae grandi quantità di acqua sulla superficie della cellula. Ciò aiuta l'interazione della cellula con il suo ambiente acquoso e la capacità della cellula di ottenere sostanze disciolte nell'acqua. Come abbiamo discusso sopra, il glicocalice è anche importante per l'identificazione delle cellule, l'autodeterminazione/non autodeterminazione e lo sviluppo embrionale, ed è utilizzato negli attacchi cellula-cellula per formare tessuti.
Fluidità della membrana
[modifica | modifica sorgente]La caratteristica a mosaico della membrana aiuta a illustrarne la natura. Le proteine integrali e i lipidi esistono nella membrana come molecole separate ma debolmente attaccate. Queste assomigliano alle tessere separate e multicolori di un mosaico e galleggiano, muovendosi un po' l'una rispetto all'altra. La membrana non è come un palloncino, tuttavia, che può espandersi e contrarsi; piuttosto, è piuttosto rigida e può scoppiare se penetrata o se una cellula assorbe troppa acqua. Tuttavia, a causa della sua natura a mosaico, un ago molto sottile può facilmente penetrare una membrana plasmatica senza farla scoppiare e la membrana fluirà e si auto-sigillerà quando si estrae l'ago.
Le caratteristiche a mosaico della membrana spiegano una parte, ma non tutta, della sua fluidità. Ci sono altri due fattori che aiutano a mantenere questa caratteristica fluida. Un fattore è la natura dei fosfolipidi stessi. Gli acidi grassi saturi, nelle code dei fosfolipidi, sono saturati con atomi di idrogeno. Non ci sono doppi legami tra atomi di carbonio adiacenti. Ciò si traduce in code relativamente dritte. Al contrario, gli acidi grassi insaturi non contengono un numero massimo di atomi di idrogeno, ma contengono alcuni doppi legami tra atomi di carbonio adiacenti. Un doppio legame si traduce in una curvatura nella stringa di carbonio di circa 30 gradi (Figura accanto).
Pertanto, se le temperature decrescenti comprimono gli acidi grassi saturi con le loro code dritte, premono l'uno sull'altro, creando una membrana densa e piuttosto rigida. Se gli acidi grassi insaturi vengono compressi, le "pieghe" nelle loro code allontanano le molecole fosfolipidiche adiacenti, mantenendo un certo spazio tra le molecole fosfolipidiche. Questo "spazio di manovra" aiuta a mantenere la fluidità nella membrana a temperature alle quali le membrane con code di acidi grassi saturi nei loro fosfolipidi "si congelerebbero" o si solidificherebbero. La fluidità relativa della membrana è particolarmente importante in un ambiente freddo. Un ambiente freddo di solito comprime le membrane composte in gran parte da acidi grassi saturi, rendendole meno fluide e più suscettibili alla rottura. Molti organismi (i pesci sono un esempio) sono in grado di adattarsi ad ambienti freddi modificando la proporzione di acidi grassi insaturi nelle loro membrane in risposta a temperature più basse.
-
La presenza di acidi grassi saturi e insaturi influisce sulla fluidità della membrana
-
Il colesterolo influisce sulla fluidità della membrana
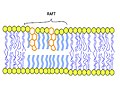
Gli animali hanno un costituente di membrana aggiuntivo che aiuta a mantenere la fluidità. Il colesterolo, che si trova accanto ai fosfolipidi nella membrana, tende a smorzare gli effetti della temperatura sulla membrana. Quindi, questo lipide funziona come un tampone, impedendo alle temperature più basse di inibire la fluidità e impedendo alle temperature più alte di aumentarla troppo. Quindi, il colesterolo estende, in entrambe le direzioni, l'intervallo di temperatura in cui la membrana è opportunamente fluida e di conseguenza funzionale. Il colesterolo svolge anche altre funzioni, come l'organizzazione di cluster di proteine transmembrana in zattere lipidiche (vedi fig. 1B.2) (Le zattere lipidiche sono delle zone della membrana che servono per l'organizzazione e l'assemblaggio di molecole di segnalazione, influenzando fluidità di membrana e regolando il traffico delle proteine di membrana, dei neurotrasmettitori e dei recettori).
| Componenti e funzioni della membrana plasmatica | |
|---|---|
| Componente | Posizione |
| Fosfolipide | Tessuto della membrana principale |
| Colesterolo | Attaccato tra i fosfolipidi e tra i due strati fosfolipidici |
| Proteine integrali (ad esempio, integrine) | Incorporato nello strato/i fosfolipidico/i; può o meno penetrare attraverso entrambi gli strati |
| Proteine periferiche | Sulla superficie interna o esterna del doppio strato fosfolipidico; non incorporato nei fosfolipidi |
| Carboidrati (componenti delle glicoproteine e dei glicolipidi) | Generalmente attaccato alle proteine sullo strato esterno della membrana |
Video su Youtube
[modifica | modifica sorgente]Structure of the Cell Membrane di Nucleus Biology è un bel video che mostra la struttura della membrana in 3D
Inside the Cell Membrane di Amoeba Sisters è un simpatico carone animato che mostra molti concetti relativi alla membrana
Fluid mosaic model of the cell membrane di Joao's Lab è una bella animazione che mostra molti concetti relativi alla membrana
Cell Membrane Structure & Functions || Membrane Lipids, Membrane Proteins and Carbohydrates - bel video, schematico, chiaro
Trasporti di membrana a confronto
[modifica | modifica sorgente]Nello schema seguente si schematizzano le principali caratteristiche del trasporto attivo e passivo

Il trasporto passivo
[modifica | modifica sorgente]Le membrane plasmatiche devono consentire a determinate sostanze di entrare e uscire da una cellula e impedire ad alcuni materiali nocivi di entrare e ad alcuni materiali essenziali di uscire. In altre parole, le membrane plasmatiche sono selettivamente permeabili (semipermeabili): consentono il passaggio di alcune sostanze, ma non di altre. Se perdessero questa selettività, la cellula non sarebbe più in grado di sostenersi e verrebbe distrutta. Alcune cellule richiedono quantità maggiori di sostanze specifiche. Devono avere un modo per ottenere questi materiali dai fluidi extracellulari. Ciò può avvenire passivamente, poiché alcuni materiali si muovono avanti e indietro, oppure la cellula può avere meccanismi speciali che facilitano il trasporto. Alcuni materiali sono così importanti per una cellula che questa spende parte della sua energia, idrolizzando l'adenosina trifosfato (ATP), per ottenerli. I globuli rossi usano parte della loro energia proprio per fare questo. La maggior parte delle cellule spende la maggior parte della propria energia per mantenere uno squilibrio di ioni sodio e potassio tra l'interno e l'esterno della cellula, nonché per la sintesi proteica.
Le forme più dirette di trasporto di membrana sono passive. Il trasporto passivo è un fenomeno naturale e non richiede che la cellula eserciti alcuna delle sue energie per compiere il movimento. Nel trasporto passivo, le sostanze si spostano da un'area di concentrazione più elevata a un'area di concentrazione più bassa. Uno spazio fisico in cui vi è un singolo intervallo di concentrazione di sostanza ha un gradiente di concentrazione .
Permeabilità selettiva
[modifica | modifica sorgente]
Le membrane plasmatiche sono asimmetriche: l'interno della membrana non è identico al suo esterno. C'è una differenza considerevole tra la serie di fosfolipidi e proteine tra i due foglietti che formano una membrana. All'interno della membrana, alcune proteine servono ad ancorare la membrana alle fibre del citoscheletro. Ci sono proteine periferiche all'esterno della membrana che legano gli elementi della matrice extracellulare. I carboidrati, attaccati ai lipidi o alle proteine, sono anche sulla superficie esterna della membrana plasmatica. Questi complessi di carboidrati aiutano la cellula a legare le sostanze necessarie nel fluido extracellulare. Ciò si aggiunge notevolmente alla natura selettiva della membrana plasmatica (Figura accanto).
Ricorda che le membrane plasmatiche sono anfipatiche: hanno regioni idrofile e idrofobiche. Questa caratteristica aiuta a spostare alcuni materiali attraverso la membrana e ostacola il movimento di altri. Il materiale non polare e liposolubile con un basso peso molecolare può facilmente scivolare attraverso il nucleo lipidico idrofobico della membrana. Sostanze come le vitamine liposolubili A, D, E e K attraversano facilmente le membrane plasmatiche nel tratto digerente e in altri tessuti. Anche i farmaci e gli ormoni liposolubili ottengono un facile ingresso nelle cellule e si trasportano facilmente nei tessuti e negli organi del corpo. Le molecole di ossigeno e anidride carbonica non hanno carica e attraversano le membrane per semplice diffusione.
Le sostanze polari presentano problemi per la membrana. Mentre alcune molecole polari si collegano facilmente con l'esterno della cellula, non possono facilmente passare attraverso il nucleo lipidico della membrana plasmatica. Inoltre, mentre i piccoli ioni potrebbero facilmente scivolare attraverso gli spazi nel mosaico della membrana, la loro carica impedisce loro di farlo. Ioni come sodio, potassio, calcio e cloruro devono avere mezzi speciali per penetrare le membrane plasmatiche. Anche gli zuccheri semplici e gli amminoacidi hanno bisogno dell'aiuto di varie proteine transmembrana (canali) per trasportarsi attraverso le membrane plasmatiche.
Diffusione
[modifica | modifica sorgente]La diffusione è un processo passivo di trasporto. Una singola sostanza si sposta da un'area ad alta concentrazione a un'area a bassa concentrazione finché la concentrazione non è uguale in tutto lo spazio. Hai familiarità con la diffusione di sostanze nell'aria. Ad esempio, pensa a qualcuno che apre una bottiglia di ammoniaca in una stanza piena di persone. Il gas di ammoniaca è alla sua massima concentrazione nella bottiglia. La sua concentrazione più bassa è ai bordi della stanza. Il vapore di ammoniaca si diffonderà, o si diffonderà, dalla bottiglia e gradualmente, sempre più persone sentiranno l'odore dell'ammoniaca mentre si diffonde. I materiali si muovono all'interno del citosol della cellula per diffusione e alcuni materiali si muovono attraverso la membrana plasmatica per diffusione ( Figura sotto). La diffusione non consuma energia. Al contrario, i gradienti di concentrazione sono una forma di energia potenziale, che si dissipa quando il gradiente viene eliminato.

Ogni sostanza separata in un mezzo, come il fluido extracellulare, ha il suo gradiente di concentrazione, indipendente dai gradienti di concentrazione di altri materiali. Inoltre, ogni sostanza si diffonderà in base a quel gradiente. All'interno di un sistema, ci saranno diverse velocità di diffusione di varie sostanze nel mezzo.
Fattori che influenzano la diffusione
[modifica | modifica sorgente]Le molecole si muovono costantemente in modo casuale, a una velocità che dipende dalla loro massa, dal loro ambiente e dalla quantità di energia termica che possiedono, che a sua volta è una funzione della temperatura. Questo movimento tiene conto della diffusione delle molecole attraverso qualsiasi mezzo in cui sono localizzate. Una sostanza si muove in qualsiasi spazio disponibile fino a quando non si distribuisce uniformemente in tutto. Dopo che una sostanza si è diffusa completamente attraverso uno spazio, rimuovendo il suo gradiente di concentrazione, le molecole si muoveranno ancora nello spazio, ma non ci sarà alcun movimento netto del numero di molecole da un'area all'altra. Chiamiamo questa mancanza di un gradiente di concentrazione in cui la sostanza non ha alcun movimento netto equilibrio dinamico. Mentre la diffusione andrà avanti in presenza del gradiente di concentrazione di una sostanza, diversi fattori influenzano la velocità di diffusione.
- Estensione del gradiente di concentrazione: maggiore è la differenza di concentrazione, più rapida è la diffusione. Più la distribuzione del materiale si avvicina all'equilibrio, più lenta è la velocità di diffusione.
- Massa delle molecole che diffondono: le molecole più pesanti si muovono più lentamente; quindi, diffondono più lentamente. Il contrario è vero per le molecole più leggere.
- Temperatura: Temperature più elevate aumentano l'energia e quindi il movimento delle molecole, aumentando la velocità di diffusione. Temperature più basse diminuiscono l'energia delle molecole, diminuendo così la velocità di diffusione.
- Densità del solvente: all'aumentare della densità di un solvente, la velocità di diffusione diminuisce. Le molecole rallentano perché hanno più difficoltà a passare attraverso il mezzo più denso. Se il mezzo è meno denso, la diffusione aumenta. Poiché le cellule utilizzano principalmente la diffusione per spostare i materiali all'interno del citoplasma, qualsiasi aumento della densità del citoplasma inibirà il movimento dei materiali. Un esempio di ciò è una persona che soffre di disidratazione. Quando le cellule del corpo perdono acqua, la velocità di diffusione diminuisce nel citoplasma e le funzioni delle cellule si deteriorano. I neuroni tendono a essere molto sensibili a questo effetto. La disidratazione porta spesso a perdita di coscienza e forse coma a causa della diminuzione della velocità di diffusione all'interno delle cellule.
- Solubilità: come abbiamo detto in precedenza, i materiali non polari o liposolubili attraversano le membrane plasmatiche più facilmente rispetto ai materiali polari, consentendo una velocità di diffusione più rapida.
- Area superficiale e spessore della membrana plasmatica: una maggiore area superficiale aumenta la velocità di diffusione; mentre una membrana più spessa la riduce.
- Distanza percorsa: maggiore è la distanza che una sostanza deve percorrere, più lenta è la velocità di diffusione. Ciò pone un limite superiore alle dimensioni delle cellule. Una cellula grande e sferica morirà perché i nutrienti o i rifiuti non possono raggiungere o lasciare il centro della cellula, rispettivamente. Pertanto, le cellule devono essere piccole, come nel caso di molti procarioti, o appiattite, come nel caso di molti eucarioti unicellulari.
Una variante della diffusione è il processo di filtrazione. Nella filtrazione, il materiale si muove secondo il suo gradiente di concentrazione attraverso una membrana. A volte la pressione aumenta la velocità di diffusione, facendo sì che le sostanze filtrino più rapidamente. Ciò avviene nei reni, dove la pressione sanguigna spinge grandi quantità di acqua e sostanze disciolte, o soluti , fuori dal sangue e nei tubuli renali. La velocità di diffusione in questo caso dipende quasi totalmente dalla pressione. Uno degli effetti dell'ipertensione è la comparsa di proteine nelle urine, che una pressione anormalmente alta "spreme".
Trasporto facilitato
[modifica | modifica sorgente]Nel trasporto facilitato , o diffusione facilitata, i materiali si diffondono attraverso la membrana plasmatica con l'aiuto delle proteine di membrana. Esiste un gradiente di concentrazione che consentirebbe a questi materiali di diffondersi nella cellula senza spendere energia cellulare. Tuttavia, questi materiali sono ioni molecolari polari che le parti idrofobiche della membrana cellulare respingono. Le proteine di trasporto facilitato proteggono questi materiali dalla forza repulsiva della membrana, consentendo loro di diffondersi nella cellula.
Il materiale trasportato si lega prima ai recettori proteici o glicoproteici sulla superficie esterna della membrana plasmatica. Ciò consente la rimozione del materiale dal fluido extracellulare di cui la cellula ha bisogno. Le sostanze passano quindi a specifiche proteine integrali che ne facilitano il passaggio. Alcune di queste proteine integrali sono raccolte di foglietti beta-pieghettati che formano un poro o un canale attraverso il doppio strato fosfolipidico. Altre sono proteine trasportatrici che si legano alla sostanza e ne aiutano la diffusione attraverso la membrana.
Canali
[modifica | modifica sorgente]Le proteine integrali coinvolte nel trasporto facilitato sono proteine di trasporto e funzionano come canali per il materiale o come trasportatori. In entrambi i casi, sono proteine transmembrana. I canali sono specifici per la sostanza trasportata. Le proteine canale hanno domini idrofili esposti ai fluidi intracellulari ed extracellulari. Inoltre, hanno un canale idrofilo che fornisce un'apertura idratata attraverso gli strati della membrana I canali ionici sono esempio di canali con trasporto facilitato: quando sono chiusi, nessun ione può attraversarle. Tuttavia, quando un canale si apre, alcuni ioni selezionati diffondono attraverso il canale. Le proteine dei canali sono altamente specifiche, lasciando passare solo uno specifico ione o sottoinsieme di ioni. Il passaggio attraverso il canale consente ai composti polari di evitare lo strato centrale non polare della membrana plasmatica che altrimenti rallenterebbe o impedirebbe il loro ingresso nella cellula. Le acquaporine sono proteine canale che consentono all'acqua di passare attraverso la membrana a una velocità molto elevata.

Le proteine del canale sono sempre aperte oppure sono "gated", ovverosia viene controllata l'apertura del canale. Quando uno ione particolare si lega alla proteina del canale, può controllare l'apertura, oppure possono essere coinvolti altri meccanismi o sostanze. In alcuni tessuti, gli ioni sodio e cloruro passano liberamente attraverso i canali aperti; mentre, in altri tessuti, un gate deve aprirsi per consentire il passaggio. Un esempio di ciò si verifica nel rene, dove ci sono entrambe le forme di canale in parti diverse dei tubuli renali. Le cellule coinvolte nella trasmissione degli impulsi elettrici, come le cellule nervose e muscolari, hanno canali gated per sodio, potassio e calcio nelle loro membrane. L'apertura e la chiusura di questi canali modifica le concentrazioni relative sui lati opposti della membrana di questi ioni, con conseguente facilitazione della trasmissione elettrica lungo le membrane (nel caso delle cellule nervose) o nella contrazione muscolare (nel caso delle cellule muscolari).
Proteine di trasporto
[modifica | modifica sorgente]Un altro tipo di proteina incorporata nella membrana plasmatica è una proteina trasportatrice . Questa proteina lega una sostanza e, quindi, innesca un cambiamento della sua forma, spostando la molecola legata dall'esterno della cellula al suo interno ( Figura sotto); a seconda del gradiente, il materiale può muoversi nella direzione opposta. Le proteine trasportatrici sono in genere specifiche per una singola sostanza. Questa selettività si aggiunge alla selettività complessiva della membrana plasmatica. Gli scienziati comprendono poco l'esatto meccanismo per il cambiamento di forma. Le proteine possono cambiare forma quando i loro legami idrogeno sono interessati, ma questo potrebbe non spiegare completamente questo meccanismo. Ogni proteina trasportatrice è specifica per una sostanza e c'è un numero finito di queste proteine in ogni membrana. Ciò può causare problemi nel trasporto di materiale sufficiente per il corretto funzionamento della cellula. Quando tutte le proteine sono legate ai loro ligandi, sono sature e la velocità di trasporto è al massimo. Aumentare il gradiente di concentrazione a questo punto non si tradurrà in un aumento della velocità di trasporto.

Un esempio di questo processo avviene nel rene. In una parte, il rene filtra glucosio, acqua, sali, ioni e amminoacidi di cui il corpo ha bisogno. Questo filtrato, che include glucosio, viene poi riassorbito in un'altra parte del rene. Poiché esiste solo un numero finito di proteine trasportatrici per il glucosio, se è presente più glucosio di quanto le proteine possano gestire, l'eccesso non viene trasportato e il corpo lo espelle attraverso l'urina. In un individuo diabetico, il termine è "versare glucosio nell'urina". Un diverso gruppo di proteine trasportatrici, proteine di trasporto del glucosio o GLUT, è coinvolto nel trasporto del glucosio e di altri zuccheri esosi attraverso le membrane plasmatiche all'interno del corpo.
Le proteine di canale e di trasporto trasportano il materiale a velocità diverse. Le proteine di canale trasportano molto più rapidamente delle proteine di trasporto. Le proteine di canale facilitano la diffusione a una velocità di decine di milioni di molecole al secondo; mentre le proteine di trasporto lavorano a una velocità di mille o un milione di molecole al secondo.
-
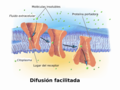
Esempio di diffusione facilitata
-
Schema della diffusione facilitata
-
Diagramma schematico di un canale ionico (in galleria). 1 - domini del canale (tipicamente quattro per canale), 2 - vestibolo esterno, 3 - filtro di selettività , 4 - diametro del filtro di selettività, 5 - sito di fosforilazione , 6 - membrana cellulare
-
Neurone con vari tipi di canali presenti
-
canali ionici
-
Struttura del canale del potassio KcsA
-
Rappresentazione schematica del movimento dell'acqua attraverso il filtro di selettività stretto del canale dell'acquaporina
-
Modello a nastro del trasportatore umano del glucosio GLUT-1
Osmosi
[modifica | modifica sorgente]L'osmosi è il movimento di molecole di acqua libera attraverso una membrana semipermeabile in base al gradiente di concentrazione dell'acqua attraverso la membrana, che è inversamente proporzionale alla concentrazione dei soluti. Mentre la diffusione trasporta materiale attraverso le membrane e all'interno delle cellule, l'osmosi trasporta solo acqua attraverso una membrana e la membrana limita la diffusione dei soluti nell'acqua. Non sorprende che le acquaporine che facilitano il movimento dell'acqua svolgano un ruolo importante nell'osmosi, in modo più evidente nei globuli rossi e nelle membrane dei tubuli renali.
L'osmosi è un caso speciale di diffusione. L'acqua, come altre sostanze, si sposta da un'area ad alta concentrazione di molecole di acqua libera a una a bassa concentrazione di molecole di acqua libera. Una domanda ovvia è: cosa fa muovere l'acqua? Immagina un becher con una membrana semipermeabile che separa i due lati o metà ( Figura 5.11 ). Su entrambi i lati della membrana il livello dell'acqua è lo stesso, ma ci sono diverse concentrazioni di sostanze disciolte, o soluto , che non possono attraversare la membrana (altrimenti il soluto che attraversa la membrana bilancerebbe le concentrazioni su ciascun lato). Se il volume della soluzione su entrambi i lati della membrana è lo stesso, ma le concentrazioni del soluto sono diverse, allora ci sono diverse quantità di acqua, il solvente, su entrambi i lati della membrana.
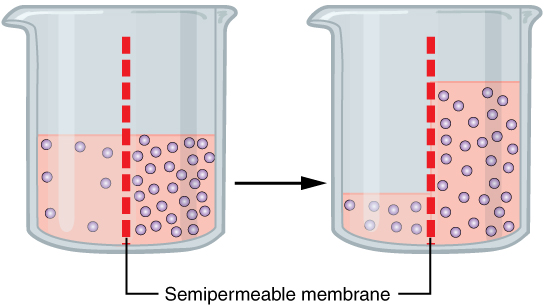
Per illustrare questo, immagina due bicchieri pieni d'acqua. Uno contiene un solo cucchiaino di zucchero; mentre il secondo contiene un quarto di tazza di zucchero. Se il volume totale delle soluzioni in entrambi i bicchieri è lo stesso, quale tazza contiene più acqua? Poiché la grande quantità di zucchero nel secondo bicchiere occupa molto più spazio del cucchiaino di zucchero nel primo, il primo bicchiere contiene più acqua.
Tornando all'esempio del becher, ricorda che ha una miscela di soluti su entrambi i lati della membrana. Un principio di diffusione è che le molecole si muovono e si diffonderanno uniformemente nel mezzo se possono. Tuttavia, solo il materiale in grado di passare attraverso la membrana si diffonderà attraverso di essa. In questo esempio, il soluto non può diffondersi attraverso la membrana, ma l'acqua sì. L'acqua ha un gradiente di concentrazione in questo sistema. Quindi, l'acqua si diffonderà lungo il suo gradiente di concentrazione, attraversando la membrana verso il lato in cui è meno concentrata. Questa diffusione dell'acqua attraverso la membrana, l'osmosi, continuerà finché il gradiente di concentrazione dell'acqua non andrà a zero o finché la pressione idrostatica dell'acqua non bilancerà la pressione osmotica. L'osmosi procede costantemente nei sistemi viventi.
Tonicità
[modifica | modifica sorgente]La tonicità descrive come una soluzione extracellulare può modificare il volume di una cellula influenzando l'osmosi. La tonicità di una soluzione spesso è direttamente correlata all'osmolarità della soluzione. L'osmolarità descrive la concentrazione totale di soluto della soluzione. Una soluzione con bassa osmolarità ha un numero maggiore di molecole d'acqua rispetto al numero di particelle di soluto. Una soluzione con alta osmolarità ha meno molecole d'acqua rispetto alle particelle di soluto. In una situazione in cui una membrana permeabile all'acqua, ma non al soluto, separa due diverse osmolarità, l'acqua si sposterà dal lato della membrana con minore osmolarità (e più acqua) al lato con maggiore osmolarità (e meno acqua). Questo effetto ha senso se si ricorda che il soluto non può muoversi attraverso la membrana e quindi l'unico componente nel sistema che può muoversi, l'acqua, si muove lungo il proprio gradiente di concentrazione. Un'importante distinzione che riguarda i sistemi viventi è che l'osmolarità misura il numero di particelle (che possono essere molecole) in una soluzione. Pertanto, una soluzione torbida con cellule può avere un'osmolarità inferiore rispetto a una soluzione limpida, se la seconda soluzione contiene più molecole disciolte rispetto alle cellule.
Soluzioni ipotoniche
[modifica | modifica sorgente]Gli scienziati usano tre termini, ipotonica, isotonica e ipertonica, per mettere in relazione l'osmolarità della cellula con l'osmolarità del fluido extracellulare che contiene le cellule. In una situazione ipotonica , il fluido extracellulare ha un'osmolarità inferiore rispetto al fluido all'interno della cellula e l'acqua entra nella cellula. (Nei sistemi viventi, il punto di riferimento è sempre il citoplasma, quindi il prefisso ipo - significa che il fluido extracellulare ha una concentrazione di soluto inferiore, o un'osmolarità inferiore, rispetto al citoplasma cellulare.) Significa anche che il fluido extracellulare ha una concentrazione di acqua nella soluzione superiore rispetto alla cellula. In questa situazione, l'acqua seguirà il suo gradiente di concentrazione ed entrerà nella cellula.
Soluzioni ipertoniche
[modifica | modifica sorgente]Per quanto riguarda una soluzione ipertonica , il prefisso iper - si riferisce al fluido extracellulare che ha un'osmolarità maggiore del citoplasma della cellula; pertanto, il fluido contiene meno acqua della cellula. Poiché la cellula ha una concentrazione di acqua relativamente maggiore, l'acqua abbandonerà la cellula.
Soluzioni isotoniche
[modifica | modifica sorgente]In una soluzione isotonica , il fluido extracellulare ha la stessa osmolarità della cellula. Se l'osmolarità della cellula corrisponde a quella del fluido extracellulare, non ci sarà alcun movimento netto di acqua dentro o fuori dalla cellula, sebbene l'acqua continuerà a muoversi dentro e fuori. Le cellule del sangue e le cellule vegetali in soluzioni ipertoniche, isotoniche e ipotoniche assumono aspetti caratteristici ( Figura 5.12 ).
Tonicità nei sistemi viventi
[modifica | modifica sorgente]In un ambiente ipotonico, l'acqua entra in una cellula e la cellula si gonfia. In una condizione isotonica, le concentrazioni relative di soluto e solvente sono uguali su entrambi i lati della membrana. Non c'è movimento netto dell'acqua; quindi, non c'è cambiamento nelle dimensioni della cellula. In una soluzione ipertonica, l'acqua lascia una cellula e la cellula si restringe. Se la condizione ipo- o iper- va in eccesso, le funzioni della cellula vengono compromesse e la cellula può essere distrutta.

Un globulo rosso scoppierà, o si lisa, quando si gonfia oltre la capacità di espansione della membrana plasmatica. Ricordate, la membrana assomiglia a un mosaico, con spazi discreti tra le molecole che la compongono. Se la cellula si gonfia e gli spazi tra i lipidi e le proteine diventano troppo grandi, la cellula si romperà.
Al contrario, quando quantità eccessive di acqua lasciano un globulo rosso, la cellula si restringe o si crena. Ciò ha l'effetto di concentrare i soluti rimasti nella cellula, rendendo il citosol più denso e interferendo con la diffusione all'interno della cellula. La capacità della cellula di funzionare sarà compromessa e potrebbe anche causare la morte della cellula.
Diversi esseri viventi hanno modi per controllare gli effetti dell'osmosi, un meccanismo che chiamiamo osmoregolazione. Alcuni organismi, come piante, funghi, batteri e alcuni protisti, hanno pareti cellulari che circondano la membrana plasmatica e impediscono la lisi cellulare in una soluzione ipotonica. La membrana plasmatica può espandersi solo fino al limite della parete cellulare, quindi la cellula non si lisa. Il citoplasma nelle piante è sempre leggermente ipertonico rispetto all'ambiente cellulare e l'acqua entrerà sempre in una cellula se è disponibile. Questo afflusso di acqua produce pressione di turgore, che irrigidisce le pareti cellulari della pianta ( Figura 5.13 ). Nelle piante non legnose, la pressione di turgore sostiene la pianta. Al contrario, se non si annaffia la pianta, il fluido extracellulare diventerà ipertonico, facendo sì che l'acqua esca dalla cellula. In questa condizione, la cellula non si restringe perché la parete cellulare non è flessibile. Tuttavia, la membrana cellulare si stacca dalla parete e restringe il citoplasma. Chiamiamo questo plasmolisi . In queste condizioni le piante perdono la pressione di turgore e appassiscono ( Figura 5.14 ).

La tonicità è una preoccupazione per tutti gli esseri viventi. Ad esempio, i parameci e le amebe, che sono protisti privi di pareti cellulari, hanno vacuoli contrattili. Questa vescicola raccoglie l'acqua in eccesso dalla cellula e la pompa fuori, impedendo alla cellula di lisarsi mentre assorbe acqua dal suo ambiente ( Figura sotto).

Molti invertebrati marini hanno livelli di sale interni adatti al loro ambiente, il che li rende isotonici con l'acqua in cui vivono. I pesci, tuttavia, devono spendere circa il cinque percento della loro energia metabolica per mantenere l'omeostasi osmotica. I pesci d'acqua dolce vivono in un ambiente ipotonico per le loro cellule. Questi pesci assorbono attivamente il sale attraverso le branchie ed espellono urina diluita per liberarsi dell'acqua in eccesso. I pesci d'acqua salata vivono nell'ambiente inverso, che è ipertonico per le loro cellule, e secernono sale attraverso le branchie ed espellono urina altamente concentrata.
Nei vertebrati, i reni regolano la quantità di acqua nel corpo. Gli osmocettori sono cellule specializzate nel cervello che monitorano la concentrazione di soluti nel sangue. Se i livelli di soluti aumentano oltre un certo intervallo, viene rilasciato un ormone che rallenta la perdita di acqua attraverso i reni e diluisce il sangue a livelli più sicuri. Gli animali hanno anche alte concentrazioni di albumina, che il fegato produce, nel loro sangue. Questa proteina è troppo grande per passare facilmente attraverso le membrane plasmatiche ed è un fattore importante nel controllo delle pressioni osmotiche applicate ai tessuti.
Trasporto attivo
[modifica | modifica sorgente]I meccanismi di trasporto attivi richiedono l'energia della cellula, solitamente sotto forma di adenosina trifosfato (ATP). Se una sostanza deve entrare nella cellula contro il suo gradiente di concentrazione, ovvero se la concentrazione della sostanza all'interno della cellula è maggiore della sua concentrazione nel fluido extracellulare (e viceversa), la cellula deve usare energia per spostare la sostanza. Alcuni meccanismi di trasporto attivi spostano materiali di piccolo peso molecolare, come gli ioni, attraverso la membrana. Altri meccanismi trasportano molecole molto più grandi.
Gradiente elettrochimico
[modifica | modifica sorgente]Abbiamo discusso di semplici gradienti di concentrazione, ovvero le concentrazioni differenziali di una sostanza attraverso uno spazio o una membrana, ma nei sistemi viventi i gradienti sono più complessi. Poiché gli ioni si muovono dentro e fuori dalle cellule e poiché le cellule contengono proteine che non si muovono attraverso la membrana e sono per lo più cariche negativamente, c'è anche un gradiente elettrico, una differenza di carica, attraverso la membrana plasmatica. L'interno delle cellule viventi è elettricamente negativo rispetto al fluido extracellulare in cui sono immerse e, allo stesso tempo, le cellule hanno concentrazioni più elevate di potassio (K + ) e concentrazioni più basse di sodio (Na + ) rispetto al fluido extracellulare. Quindi in una cellula vivente, il gradiente di concentrazione di Na + tende a spingerlo dentro la cellula e il suo gradiente elettrico (uno ione positivo) lo spinge anche verso l'interno, verso l'interno caricato negativamente. Tuttavia, la situazione è più complessa per altri elementi come il potassio. Il gradiente elettrico di K + , uno ione positivo, lo spinge anche dentro la cellula, ma il gradiente di concentrazione di K + spinge K + fuori dalla cellula ( Figura sotto). Chiamiamo gradiente elettrochimico la combinazione del gradiente di concentrazione e della carica elettrica che agisce su uno ione.


Il gradiente protonico fornisce energia per un trasportatore attivo secondario. La pompa protonica crea un gradiente elettrochimico di protoni (ioni idrogeno, H+) utilizzando ATP per guidare il trasporto attivo primario. Questo gradiente consente il cotrasporto/trasporto secondario del saccarosio contro il suo gradiente di concentrazione mentre i protoni scendono lungo il loro gradiente di concentrazione tramite la loro proteina cotrasportatrice di membrana.
Muoversi contro un gradiente
[modifica | modifica sorgente]Per spostare sostanze contro una concentrazione o un gradiente elettrochimico, la cellula deve usare energia. Questa energia deriva dall'ATP generato attraverso il metabolismo della cellula. I meccanismi di trasporto attivi, o pompe , lavorano contro i gradienti elettrochimici. Le piccole sostanze passano costantemente attraverso le membrane plasmatiche. Il trasporto attivo mantiene le concentrazioni di ioni e altre sostanze di cui le cellule viventi hanno bisogno di fronte a questi movimenti passivi. Una cellula può spendere gran parte della sua riserva di energia metabolica per mantenere questi processi. (Un globulo rosso usa la maggior parte della sua energia metabolica per mantenere lo squilibrio tra i livelli di sodio e potassio esterni e interni di cui la cellula ha bisogno.) Poiché i meccanismi di trasporto attivi dipendono dal metabolismo di una cellula per l'energia, sono sensibili a molti veleni metabolici che interferiscono con la riserva di ATP.
Esistono due meccanismi per trasportare materiale di piccolo peso molecolare e piccole molecole. Il trasporto attivo primario sposta gli ioni attraverso una membrana e crea una differenza di carica attraverso quella membrana, che è direttamente dipendente dall'ATP. Il trasporto attivo secondario non richiede direttamente l'ATP: invece, è il movimento del materiale dovuto al gradiente elettrochimico stabilito dal trasporto attivo primario.
Proteine trasportatrici per il trasporto attivo
[modifica | modifica sorgente]Un importante adattamento della membrana per il trasporto attivo è la presenza di proteine trasportatrici specifiche o pompe per facilitare il movimento: ci sono tre tipi di proteine o trasportatori ( Figura sotto). Un uniporto trasporta uno ione o una molecola specifica. Un simporto trasporta due ioni o molecole diversi, entrambi nella stessa direzione. Un antiporto trasporta anche due ioni o molecole diversi, ma in direzioni diverse. Tutti questi trasportatori possono anche trasportare piccole molecole organiche non cariche come il glucosio. Questi tre tipi di proteine trasportatrici sono anche in diffusione facilitata, ma non richiedono ATP per funzionare in quel processo. Alcuni esempi di pompe per il trasporto attivo sono Na + -K + ATPasi, che trasporta ioni sodio e potassio, e H + -K + ATPasi, che trasporta ioni idrogeno e potassio. Entrambe sono proteine trasportatrici antiporto. Altre due proteine trasportatrici sono Ca 2+ ATPasi e H + ATPasi, che trasportano rispettivamente solo ioni calcio e solo ioni idrogeno. Entrambe sono pompe.
Trasporto attivo primario
[modifica | modifica sorgente]Il trasporto attivo primario che sposta il sodio e il potassio consente il trasporto attivo secondario. Quest'ultimo è ancora attivo perché dipende dall'uso di energia del trasporto primario.

La pompa sodio-potassio è un esempio di trasporto attivo primario che sposta gli ioni, in questo caso ioni sodio e potassio, attraverso una membrana contro i loro gradienti di concentrazione. L'energia è fornita dall'idrolisi dell'ATP. Tre ioni sodio vengono spostati fuori dalla cellula per ogni 2 ioni potassio che vengono portati nella cellula. Ciò crea un gradiente elettrochimico che è cruciale per le cellule viventi.
Una delle pompe più importanti nelle cellule animali è la pompa sodio-potassio (Na + -K + ATPasi), che mantiene il gradiente elettrochimico (e le concentrazioni corrette di Na + e K + ) nelle cellule viventi. La pompa sodio-potassio sposta K + nella cellula mentre sposta Na + fuori allo stesso tempo, con un rapporto di tre ioni Na + per ogni due ioni K + spostati dentro. La Na + -K + ATPasi esiste in due forme, a seconda del suo orientamento verso l'interno o l'esterno della cellula e della sua affinità per gli ioni sodio o potassio. Il processo consiste nei seguenti sei passaggi.
- Con l'enzima orientato verso l'interno della cellula, il trasportatore ha un'elevata affinità per gli ioni sodio. Tre ioni si legano alla proteina.
- Il trasportatore proteico idrolizza l'ATP e ad esso si lega un gruppo fosfato a bassa energia.
- Di conseguenza, il trasportatore cambia forma e si riorienta verso l'esterno della membrana. L'affinità della proteina per il sodio diminuisce e i tre ioni sodio lasciano il trasportatore.
- Il cambiamento di forma aumenta l'affinità del trasportatore per gli ioni potassio, e due di tali ioni si legano alla proteina. Successivamente, il gruppo fosfato a bassa energia si stacca dal trasportatore.
- Una volta rimosso il gruppo fosfato e attaccati gli ioni potassio, la proteina trasportatrice si riposiziona verso l'interno della cellula.
- La proteina carrier, nella sua nuova configurazione, ha una minore affinità per il potassio, e i due ioni si spostano nel citoplasma. La proteina ha ora una maggiore affinità per gli ioni sodio, e il processo ricomincia.
Sono accadute diverse cose come risultato di questo processo. A questo punto, ci sono più ioni sodio all'esterno della cellula che all'interno e più ioni potassio all'interno che all'esterno. Per ogni tre ioni sodio che escono, due ioni potassio entrano. Ciò fa sì che l'interno sia leggermente più negativo rispetto all'esterno. Questa differenza di carica è importante per creare le condizioni necessarie per il processo secondario. La pompa sodio-potassio è, quindi, una pompa elettrogenica (una pompa che crea uno squilibrio di carica), creando uno squilibrio elettrico attraverso la membrana e contribuendo al potenziale di membrana.
-
Schema della pompa sodio-potassio
Video
[modifica | modifica sorgente]The Sodium-Potassium Pump - di RicochetScience: video interessante sulla pompa sodio-potassio
Neuronal Signaling and Sodium-Potassium Pump (from PDB-101) di RCSBProteinDataBank (al minuto 5:20): video 3d che prova a mostrare la pompa in modo più realistico
Trasporto attivo secondario (co-trasporto)
[modifica | modifica sorgente]Il trasporto attivo secondario utilizza l'energia cinetica degli ioni sodio per portare altri composti, contro il loro gradiente di concentrazione, nella cellula. Quando le concentrazioni di ioni sodio si accumulano all'esterno della membrana plasmatica a causa del processo di trasporto attivo primario, ciò crea un gradiente elettrochimico. Se esiste una proteina canale ed è aperta, gli ioni sodio si muoveranno lungo il suo gradiente di concentrazione attraverso la membrana. Questo movimento trasporta altre sostanze che devono essere attaccate alla stessa proteina di trasporto affinché gli ioni sodio possano muoversi attraverso la membrana (Figura sotto). Molti amminoacidi, così come il glucosio, entrano in una cellula in questo modo. Questo processo secondario immagazzina anche ioni idrogeno ad alta energia nei mitocondri delle cellule vegetali e animali per produrre ATP. L'energia potenziale che si accumula negli ioni idrogeno immagazzinati si traduce in energia cinetica quando gli ioni attraversano la proteina canale ATP sintasi, e quell'energia converte quindi l'ADP in ATP.

Trasporto massivo: endocitosi
[modifica | modifica sorgente]Oltre a spostare piccoli ioni e molecole attraverso la membrana, le cellule devono anche rimuovere e assorbire molecole e particelle più grandi (vedere la Tabella 5.2 sotto). Alcune cellule sono persino in grado di inglobare interi microrganismi unicellulari. Potresti aver correttamente ipotizzato che quando una cellula assorbe e rilascia particelle grandi, richieda energia. Una particella grande, tuttavia, non può passare attraverso la membrana, nemmeno con l'energia che la cellula fornisce.
L'endocitosi è un tipo di trasporto attivo che sposta particelle, come grandi molecole, parti di cellule e persino cellule intere, in una cellula. Esistono diverse varianti di endocitosi, ma tutte condividono una caratteristica comune: la membrana plasmatica della cellula si invagina, formando una tasca attorno alla particella bersaglio. La tasca si pizzica, con il risultato che la particella contiene se stessa in una vescicola intracellulare appena creata formata dalla membrana plasmatica.

Fagocitosi
[modifica | modifica sorgente]La fagocitosi (la condizione di "mangiare cellule") è il processo mediante il quale una cellula assorbe particelle di grandi dimensioni, come altre cellule o particelle relativamente grandi. Ad esempio, quando i microrganismi invadono il corpo umano, un tipo di globulo bianco, un neutrofilo, rimuoverà gli invasori attraverso questo processo, circondando e inglobando il microrganismo, che il neutrofilo poi distrugge (Figura 21)
In preparazione alla fagocitosi, una porzione della superficie rivolta verso l'interno della membrana plasmatica viene rivestita dalla proteina clatrina , che stabilizza la sezione di questa membrana. La porzione rivestita della membrana si estende quindi dal corpo della cellula e circonda la particella, racchiudendola infine. Una volta che la vescicola contenente la particella è racchiusa all'interno della cellula, la clatrina si stacca dalla membrana e la vescicola si fonde con un lisosoma per scomporre il materiale nel compartimento appena formato (endosoma). Quando i nutrienti accessibili dalla degradazione del contenuto vescicolare sono stati estratti, l'endosoma appena formato si fonde con la membrana plasmatica e rilascia il suo contenuto nel fluido extracellulare. La membrana endosomiale diventa di nuovo parte della membrana plasmatica.
Pinocitosi
[modifica | modifica sorgente]Una variante dell'endocitosi è la pinocitosi . Letteralmente significa "bere le cellule". Scoperta da Warren Lewis nel 1929, questo embriologo e biologo cellulare americano descrisse un processo in base al quale presumeva che la cellula stesse intenzionalmente assorbendo fluido extracellulare. Nella pinocitosi, la membrana cellulare si invagina, circonda un piccolo volume di fluido e si pizzica. In realtà, questo è un processo che assorbe molecole, tra cui l'acqua, di cui la cellula ha bisogno dal fluido extracellulare. La pinocitosi produce una vescicola molto più piccola rispetto alla fagocitosi e la vescicola non ha bisogno di fondersi con un lisosoma ( Figura 21).
Una variante della pinocitosi è la potocitosi . Questo processo utilizza una proteina di rivestimento, la caveolina , sul lato citoplasmatico della membrana plasmatica, che svolge una funzione simile alla clatrina. Le cavità nella membrana plasmatica che formano i vacuoli hanno recettori di membrana e zattere lipidiche oltre alla caveolina. I vacuoli o vescicole formati nelle caveole (singolare caveola) sono più piccoli di quelli nella pinocitosi. La potocitosi porta piccole molecole nella cellula e le trasporta attraverso la cellula per il loro rilascio dall'altro lato, un processo che chiamiamo transcitosi. In alcuni casi, le caveole consegnano il loro carico agli organelli membranosi come l'ER.
Endocitosi mediata dal recettore
[modifica | modifica sorgente]Una variante mirata dell'endocitosi impiega proteine recettrici nella membrana plasmatica che hanno un'affinità di legame specifica per determinate sostanze ( Figura 21).
Nell'endocitosi mediata da recettore , come nella fagocitosi, la clatrina si attacca al lato citoplasmatico della membrana plasmatica. Se l'assorbimento di un composto dipende dall'endocitosi mediata da recettore e il processo è inefficace, il materiale non verrà rimosso dai fluidi tissutali o dal sangue. Invece, rimarrà in quei fluidi e aumenterà di concentrazione. Il fallimento dell'endocitosi mediata da recettore causa alcune malattie umane. Ad esempio, l'endocitosi mediata da recettore rimuove le lipoproteine a bassa densità o LDL (o colesterolo "cattivo") dal sangue. Nella malattia genetica umana ipercolesterolemia familiare, i recettori LDL sono difettosi o completamente assenti. Le persone con questa condizione hanno livelli di colesterolo pericolosi per la vita nel sangue, perché le loro cellule non riescono a eliminare le particelle LDL.
Sebbene l'endocitosi mediata da recettori sia progettata per portare nella cellula sostanze specifiche che normalmente si trovano nel fluido extracellulare, altre sostanze possono entrare nella cellula nello stesso sito. I virus dell'influenza, la difterite e la tossina del colera hanno tutti siti che reagiscono in modo incrociato con i normali siti di legame dei recettori e entrano nelle cellule.
-
Una rappresentazione di vari tipi di Endocitosi
-
For example, coronavirus SARS-CoV-2 binds to the ACE2 receptor of the epithelial cell.
-
Video utili
[modifica | modifica sorgente]13 3 Receptor Mediated Endocytosis di Richard Posner
Endocytosis: Pinocytosis and Phagocytosis | Eating, Digesting and Pooping by the Cell di Nonstop Neuron
Endocytosis and exocytosis di Osmosi
Detailed Animation on Exocytosis di MedEd Mastry
Trasporto massivo: esocitosi
[modifica | modifica sorgente]Il processo inverso di spostamento del materiale in una cellula è il processo di esocitosi. L'esocitosi è l'opposto dei processi di cui abbiamo discusso sopra in quanto il suo scopo è di espellere il materiale dalla cellula nel fluido extracellulare. Il materiale di scarto è avvolto in una membrana e si fonde con l'interno della membrana plasmatica. Questa fusione apre l'involucro membranoso all'esterno della cellula e il materiale di scarto viene espulso nello spazio extracellulare ( Figura sotto ). Altri esempi di cellule che rilasciano molecole tramite esocitosi includono la secrezione di proteine della matrice extracellulare e la secrezione di neurotrasmettitori nella fessura sinaptica da parte di vescicole sinaptiche.

Metodi di trasporto, requisiti energetici e tipi di materiale trasportato
| Metodo di trasporto | Attivo/Passivo | Materiale trasportato |
|---|---|---|
| Diffusione | Passivo | Materiale a basso peso molecolare |
| Osmosi | Passivo | Acqua |
| Trasporto/diffusione facilitata | Passivo | Sodio, potassio, calcio, glucosio |
| Trasporto attivo primario | Attivo | Sodio, potassio, calcio |
| Trasporto attivo secondario | Attivo | Aminoacidi, lattosio |
| Fagocitosi | Attivo | Grandi macromolecole, cellule intere o strutture cellulari |
| Pinocitosi e potocitosi | Attivo | Piccole molecole (liquidi/acqua) |
| Endocitosi mediata dal recettore | Attivo | Grandi quantità di macromolecole |
Energia e metabolismo
[modifica | modifica sorgente]Gli scienziati usano il termine bioenergetica per discutere il concetto di flusso di energia (Figura sotto) attraverso sistemi viventi, come le cellule. I processi cellulari come la costruzione e la scomposizione di molecole complesse avvengono attraverso reazioni chimiche graduali. Alcune di queste reazioni chimiche sono spontanee e rilasciano energia; mentre altre richiedono energia per procedere. Proprio come gli esseri viventi devono consumare continuamente cibo per ricostituire ciò che hanno usato, le cellule devono continuamente ottenere più energia per ricostituire quella che le numerose reazioni chimiche che richiedono energia e che si verificano costantemente utilizzano. Tutte le reazioni chimiche che avvengono all'interno delle cellule, comprese quelle che utilizzano e rilasciano energia, sono il metabolismo della cellula .

Vie metaboliche
[modifica | modifica sorgente]I processi di produzione e scomposizione delle molecole di zucchero illustrano due tipi di percorsi metabolici. Un percorso metabolico è una serie di reazioni biochimiche interconnesse che convertono una o più molecole di substrato, passo dopo passo, attraverso una serie di intermedi metabolici, producendo infine un prodotto o dei prodotti finali. Nel caso del metabolismo dello zucchero, il primo percorso metabolico sintetizzava lo zucchero da molecole più piccole e l'altro percorso scomponeva lo zucchero in molecole più piccole. Gli scienziati chiamano questi due processi opposti, il primo che richiedeva energia e il secondo che produceva energia, rispettivamente percorsi anabolici (costruzione) e catabolici (scomposizione). Di conseguenza, la costruzione (anabolismo) e la degradazione (catabolismo) comprendono il metabolismo.
Percorsi anabolici e catabolici
[modifica | modifica sorgente]I percorsi anabolici richiedono un apporto di energia per sintetizzare molecole complesse da quelle più semplici. La sintesi di zucchero da CO2 è un esempio. Altri esempi sono la sintesi di grandi proteine da blocchi di costruzione di amminoacidi e la sintesi di nuovi filamenti di DNA da blocchi di costruzione di acidi nucleici. Questi processi biosintetici sono fondamentali per la vita della cellula, avvengono costantemente e richiedono energia che l'ATP e altre molecole ad alta energia come NADH (nicotinamide adenina dinucleotide) e NADPH forniscono ( Figura sotto).
L'ATP è una molecola importante che le cellule devono avere sempre in quantità sufficiente. La scomposizione degli zuccheri illustra come una singola molecola di glucosio possa immagazzinare abbastanza energia per produrre una grande quantità di ATP, da 36 a 38 molecole. Questo è un percorso catabolico . I percorsi catabolici comportano la degradazione (o la scomposizione) di molecole complesse in molecole più semplici. L'energia molecolare immagazzinata nei legami delle molecole complesse viene rilasciata nei percorsi catabolici e raccolta in modo tale da poter produrre ATP. Anche altre molecole che immagazzinano energia, come i grassi, si scompongono attraverso reazioni cataboliche simili per rilasciare energia e produrre ATP ( Figura sotto).
È importante sapere che le reazioni chimiche del percorso metabolico non avvengono spontaneamente. Una proteina chiamata enzima facilita o catalizza ogni fase della reazione. Gli enzimi sono importanti per catalizzare tutti i tipi di reazioni biologiche, sia quelle che richiedono energia che quelle che rilasciano energia.

Esempio del metabolismo dei carboidrati
[modifica | modifica sorgente]Il metabolismo dello zucchero (un carboidrato semplice) (reazioni chimiche) è un classico esempio dei numerosi processi cellulari che utilizzano e producono energia. Gli esseri viventi consumano zucchero come principale fonte di energia, perché le molecole di zucchero hanno una notevole energia immagazzinata nei loro legami. La seguente equazione descrive la scomposizione del glucosio, uno zucchero semplice:
I carboidrati consumati hanno origine in organismi fotosintetizzanti come le piante ( Figura sotto). Durante la fotosintesi, le piante usano l'energia della luce solare per convertire il gas di anidride carbonica (CO2) in molecole di zucchero, come il glucosio (C6H12O6). Poiché questo processo comporta la sintesi di una molecola più grande, che immagazzina energia, richiede un apporto di energia per procedere. La seguente equazione (si noti che è l'inverso dell'equazione precedente) descrive la sintesi del glucosio:
Durante le reazioni chimiche della fotosintesi, l'energia è sotto forma di una molecola ad altissima energia che gli scienziati chiamano ATP, o adenosina trifosfato. Questa è la valuta energetica primaria di tutte le cellule. Proprio come il dollaro è la valuta che usiamo per acquistare beni, le cellule usano le molecole di ATP come valuta energetica per svolgere un lavoro immediato. Lo zucchero (glucosio) è immagazzinato come amido o glicogeno. I polimeri che immagazzinano energia come questi si scompongono in glucosio per fornire molecole di ATP.
L'energia solare è necessaria per sintetizzare una molecola di glucosio durante le reazioni di fotosintesi. Nella fotosintesi, l'energia luminosa del sole inizialmente si trasforma in energia chimica che si immagazzina temporaneamente nelle molecole di trasporto energetico ATP e NADPH (nicotinamide adenina dinucleotide fosfato). La fotosintesi utilizza in seguito l'energia immagazzinata in ATP e NADPH per costruire una molecola di glucosio da sei molecole di CO2 . Questo processo è analogo a fare colazione al mattino per acquisire energia per il tuo corpo che puoi utilizzare più tardi nel corso della giornata. In condizioni ideali, è necessaria l'energia da 18 molecole di ATP per sintetizzare una molecola di glucosio durante le reazioni di fotosintesi. Le molecole di glucosio possono anche combinarsi e convertirsi in altri tipi di zucchero. Quando un organismo consuma zuccheri, le molecole di glucosio alla fine si fanno strada nella cellula vivente di ogni organismo. All'interno della cellula, ogni molecola di zucchero si scompone attraverso una serie complessa di reazioni chimiche. L'obiettivo di queste reazioni è raccogliere l'energia immagazzinata all'interno delle molecole di zucchero. L'energia raccolta produce molecole di ATP ad alta energia, che svolgono lavoro, alimentando molte reazioni chimiche nella cellula. La quantità di energia necessaria per produrre una molecola di glucosio da sei molecole di anidride carbonica è di 18 molecole di ATP e 12 molecole di NADPH (ognuna delle quali è energeticamente equivalente a tre molecole di ATP), o un totale di 54 molecole equivalenti necessarie per sintetizzare una molecola di glucosio. Questo processo è un modo fondamentale ed efficiente per le cellule di generare l'energia molecolare di cui hanno bisogno.
Evoluzione delle vie metaboliche
[modifica | modifica sorgente]
La complessità del metabolismo non si limita alla sola comprensione dei percorsi metabolici. La complessità metabolica varia da organismo a organismo. La fotosintesi è il percorso principale in cui gli organismi fotosintetici come le piante (le alghe planctoniche svolgono la maggior parte della fotosintesi globale) raccolgono l'energia del sole e la convertono in carboidrati. Il sottoprodotto della fotosintesi è l'ossigeno, di cui alcune cellule hanno bisogno per svolgere la respirazione cellulare. Durante la respirazione cellulare, l'ossigeno aiuta nella scomposizione catabolica dei composti di carbonio, come i carboidrati. Tra i prodotti ci sono CO2 e ATP. Inoltre, alcuni eucarioti svolgono processi catabolici senza ossigeno (fermentazione); ovvero, svolgono o utilizzano il metabolismo anaerobico.
Gli organismi hanno probabilmente sviluppato un metabolismo anaerobico per sopravvivere (gli organismi viventi sono comparsi circa 3,8 miliardi di anni fa, quando l'atmosfera era carente di ossigeno). Nonostante le differenze tra gli organismi e la complessità del metabolismo, i ricercatori hanno scoperto che tutti i rami della vita condividono alcuni degli stessi percorsi metabolici, il che suggerisce che tutti gli organismi si siano evoluti dallo stesso antico antenato comune ( Figura sopra). Le prove indicano che nel tempo i percorsi si sono divisi, aggiungendo enzimi specializzati per consentire agli organismi di adattarsi meglio al loro ambiente, aumentando così le loro possibilità di sopravvivenza. Tuttavia, il principio di base rimane che tutti gli organismi devono raccogliere energia dal loro ambiente e convertirla in ATP per svolgere le funzioni cellulari.
Tipi di energia
[modifica | modifica sorgente]Definiamo l'energia come la capacità di fare lavoro. Come hai imparato, l'energia esiste in diverse forme. Ad esempio, l'energia elettrica, l'energia luminosa e l'energia termica sono tutti tipi di energia diversi. Mentre questi sono tutti tipi di energia familiari che si possono vedere o sentire, c'è un altro tipo di energia che è molto meno tangibile. Gli scienziati associano questa energia a qualcosa di semplice come un oggetto sopra il terreno. Per apprezzare il modo in cui l'energia fluisce dentro e fuori dai sistemi biologici, è importante capire di più sui diversi tipi di energia che esistono nel mondo fisico.
Energia cinetica
[modifica | modifica sorgente]Quando un oggetto è in movimento, c'è energia. Ad esempio, un aereo in volo produce una notevole energia. Questo perché gli oggetti in movimento sono in grado di attuare un cambiamento o di svolgere un lavoro. Pensa a una palla da demolizione. Anche una palla da demolizione che si muove lentamente può causare danni considerevoli ad altri oggetti. Tuttavia, una palla da demolizione che non è in movimento non è in grado di svolgere un lavoro. L'energia con oggetti in movimento è energia cinetica . Un proiettile in corsa, una persona che cammina, un rapido movimento di molecole nell'aria (che produce calore) e radiazioni elettromagnetiche come la luce hanno tutti energia cinetica.
Energia potenziale
[modifica | modifica sorgente]Cosa succederebbe se sollevassimo quella stessa palla da demolizione immobile due piani sopra un'auto con una gru? Se la palla da demolizione sospesa è immobile, possiamo associarle energia? La risposta è sì. La palla da demolizione sospesa ha energia associata che è fondamentalmente diversa dall'energia cinetica degli oggetti in movimento. Questa forma di energia deriva dal potenziale della palla da demolizione di fare lavoro. Se rilasciassimo la palla, farebbe lavoro. Poiché questo tipo di energia si riferisce al potenziale di fare lavoro, la chiamiamo energia potenziale . Gli oggetti trasferiscono la loro energia tra cinetica e potenziale nel seguente modo: quando la palla da demolizione è sospesa immobile, ha 0 energia cinetica e 100 percento di energia potenziale. Una volta rilasciata, la sua energia cinetica inizia ad aumentare perché aumenta la velocità a causa della gravità. Allo stesso tempo, mentre si avvicina al suolo, perde energia potenziale. Da qualche parte a metà caduta ha il 50 percento di energia cinetica e il 50 percento di energia potenziale. Appena prima di toccare terra, la palla ha quasi perso la sua energia potenziale e ha un'energia cinetica quasi massima. Altri esempi di energia potenziale includono l'energia dell'acqua trattenuta dietro una diga (vedi galleria) o quella di una persona in procinto di lanciarsi con il paracadute da un aereo.
Energia chimica
[modifica | modifica sorgente]Associamo l'energia potenziale non solo alla posizione della materia (come un bambino seduto su un ramo di un albero), ma anche alla sua struttura. Una molla a terra ha energia potenziale se è compressa; così come un elastico teso. L'esistenza stessa delle cellule viventi si basa in gran parte sull'energia potenziale strutturale. A livello chimico, i legami che tengono insieme gli atomi delle molecole hanno energia potenziale. Ricorda che i percorsi cellulari anabolici richiedono energia per sintetizzare molecole complesse da quelle più semplici, e i percorsi catabolici rilasciano energia quando le molecole complesse si rompono. Il fatto che la rottura di certi legami chimici possa rilasciare energia implica che quei legami abbiano energia potenziale. Infatti, c'è energia potenziale immagazzinata nei legami di tutte le molecole di cibo che mangiamo, che alla fine sfruttiamo per l'uso. Questo perché questi legami possono rilasciare energia quando si rompono. Gli scienziati chiamano il tipo di energia potenziale che esiste nei legami chimici che si rilascia quando quei legami si rompono energia chimica ( vedi galleria). L'energia chimica è responsabile della fornitura di energia alle cellule viventi dal cibo. La rottura dei legami molecolari all'interno delle molecole del combustibile determina il rilascio di energia.
-
Le montagne russe sfruttano l'energia potenziale e quella cinetica per funzionare
-
Atomi e molecole possiedono energia cinetica, poiché si muovono
-
Le palle da demolizione sfruttano l'energia potenziale e cinetica
-
Le dighe permettono di sfruttare l'energia potenziale dell'acqua
-
L'acqua in movimento (come nella cascata) possiede energia cinetica
-
La molecola di metano possiede energia chimica
-
Il metano (energia chimica) permette all'autobus di muoversi (energia cinetica)
Laboratorio virtuale
[modifica | modifica sorgente]Visita questo sito e seleziona "Un pendolo semplice" nel menu (sotto "Moto armonico") per vedere l'energia cinetica (K) e potenziale (U) mutevole di un pendolo in movimento.
Reazioni endoergoniche e reazioni esoergoniche
[modifica | modifica sorgente]Se durante una reazione chimica si rilascia energia, il valore risultante dall'equazione di cui sopra sarà un numero negativo. I prodotti della reazione hanno meno energia libera dei reagenti, perché hanno rilasciato energia libera durante la reazione. Gli scienziati chiamano reazioni esoergoniche queste reazioni che rilasciano energia. Pensa: esoergoniche significa che l'energia esce dal sistema. Ci riferiamo anche a queste reazioni come reazioni spontanee, perché possono verificarsi senza aggiungere energia al sistema. Capire quali reazioni chimiche sono spontanee e rilasciano energia libera è estremamente utile per i biologi, perché queste reazioni possono essere sfruttate per svolgere lavoro all'interno della cellula. Dobbiamo fare un'importante distinzione tra il termine spontanea e l'idea di una reazione chimica che si verifica immediatamente. Contrariamente all'uso quotidiano del termine, una reazione spontanea non è una reazione che si verifica all'improvviso o rapidamente. Il ferro arrugginito è un esempio di una reazione spontanea che si verifica lentamente, poco a poco, nel tempo.
Se una reazione chimica richiede un apporto di energia anziché rilasciare energia, allora i prodotti hanno più energia libera dei reagenti. Quindi, possiamo pensare ai prodotti delle reazioni come molecole che immagazzinano energia. Chiamiamo queste reazioni chimiche reazioni endoergoniche e non sono spontanee. Una reazione endoergonica non avrà luogo da sola senza aggiungere energia.
Rivediamo l'esempio della sintesi e della scomposizione della molecola alimentare, il glucosio. Ricorda che costruire molecole complesse, come gli zuccheri, da quelle più semplici è un processo anabolico e richiede energia. Pertanto, le reazioni chimiche coinvolte nei processi anabolici sono reazioni endoergoniche. In alternativa, il processo catabolico di scomposizione dello zucchero in molecole più semplici rilascia energia in una serie di reazioni esoergoniche. Come nell'esempio della ruggine di cui sopra, la scomposizione dello zucchero comporta reazioni spontanee, ma queste reazioni non si verificano istantaneamente. La galleria mostra altri esempi di reazioni endoergoniche ed esoergoniche. Le sezioni successive forniranno maggiori informazioni su cos'altro è necessario per far sì che anche le reazioni spontanee avvengano in modo più efficiente.
-
La decomposizione di materiale organico e un processo esoergonico
-
Un embrione che si sviluppa è un processo endoergonico
-
La demolizione del glucosio è un processo esoergonico
-
La ruggine è un processo esoergonico
-
La fotosintesi è un processo endoergonico
Energia di attivazione
[modifica | modifica sorgente]C'è un altro concetto importante che dobbiamo considerare riguardo alle reazioni endoergoniche ed esoergoniche. Anche le reazioni esoergoniche richiedono una piccola quantità di apporto energetico prima di poter procedere con i loro passaggi di rilascio di energia. Queste reazioni hanno un rilascio netto di energia, ma richiedono comunque un po' di energia iniziale. Gli scienziati chiamano questa piccola quantità di apporto energetico necessaria affinché tutte le reazioni chimiche si verifichino energia di attivazione (o energia libera di attivazione) abbreviata come E A ( Figura sotto).

Perché una reazione che rilascia energia dovrebbe effettivamente richiedere un po' di energia per procedere? Il motivo risiede nei passaggi che si verificano durante una reazione chimica. Durante le reazioni chimiche, alcuni legami chimici si rompono e se ne formano di nuovi. Ad esempio, quando una molecola di glucosio si rompe, i legami tra gli atomi di carbonio della molecola si rompono. Poiché si tratta di legami che immagazzinano energia, rilasciano energia quando si rompono. Tuttavia, per portarli in uno stato che consenta ai legami di rompersi, la molecola deve essere in qualche modo contorta. È necessario un piccolo apporto di energia per raggiungere questo stato contorto. Questo stato contorto è lo stato di transizione , ed è uno stato instabile ad alta energia. Per questo motivo, le molecole reagenti non durano a lungo nel loro stato di transizione, ma procedono molto rapidamente verso i passaggi successivi della reazione chimica. I diagrammi di energia libera illustrano i profili energetici per una data reazione. Che la reazione sia esoergonica o endoergonica determina se i prodotti nel diagramma esisteranno a uno stato di energia inferiore o superiore rispetto sia ai reagenti che ai prodotti. Tuttavia, indipendentemente da questa misura, lo stato di transizione della reazione esiste a uno stato energetico superiore a quello dei reagenti e quindi E A è sempre positivo.
Energia termica (calore)
[modifica | modifica sorgente]
Da dove proviene l'energia di attivazione richiesta dai reagenti chimici? La fonte richiesta dall'energia di attivazione per far procedere le reazioni è in genere l'energia termica (calore) dall'ambiente circostante. L'energia termica (l'energia di legame totale dei reagenti o dei prodotti in una reazione chimica) accelera il movimento della molecola, aumentando la frequenza e la forza con cui si scontrano. Sposta anche leggermente gli atomi e i legami all'interno della molecola, aiutandoli a raggiungere il loro stato di transizione. Per questo motivo, riscaldare un sistema farà sì che i reagenti chimici all'interno di quel sistema reagiscano più frequentemente. Aumentare la pressione su un sistema ha lo stesso effetto. Una volta che i reagenti hanno assorbito abbastanza energia termica dall'ambiente circostante per raggiungere lo stato di transizione, la reazione procederà.
L'energia di attivazione di una particolare reazione determina la velocità con cui procederà. Maggiore è l'energia di attivazione, più lenta è la reazione chimica. L'esempio della ruggine del ferro illustra una reazione intrinsecamente lenta. Questa reazione avviene lentamente nel tempo a causa della sua elevata E A . Inoltre, la combustione di molti combustibili, che è fortemente esoergonica, avverrà a una velocità trascurabile a meno che il calore sufficiente di una scintilla non superi la loro energia di attivazione. Tuttavia, una volta che iniziano a bruciare, le reazioni chimiche rilasciano abbastanza calore per continuare il processo di combustione, fornendo l'energia di attivazione per le molecole di combustibile circostanti. Come queste reazioni al di fuori delle cellule, l'energia di attivazione per la maggior parte delle reazioni cellulari è troppo alta perché l'energia termica possa superarla a velocità efficienti. In altre parole, affinché importanti reazioni cellulari avvengano a velocità apprezzabili (numero di reazioni per unità di tempo), le loro energie di attivazione devono essere abbassate ( Figura accanto). Gli scienziati si riferiscono a questo come catalisi. Questa è una cosa molto buona per quanto riguarda le cellule viventi. Macromolecole importanti, come proteine, DNA e RNA, immagazzinano una notevole quantità di energia e la loro scomposizione è esoergonica. Se le temperature cellulari da sole fornissero abbastanza energia termica per queste reazioni esoergoniche per superare le loro barriere di attivazione, i componenti essenziali della cellula si disintegrerebbero.
Le leggi della termodinamica
[modifica | modifica sorgente]La termodinamica si riferisce allo studio dell'energia e del trasferimento di energia che coinvolge la materia fisica. La materia e il suo ambiente pertinenti a un caso particolare di trasferimento di energia sono classificati come un sistema e tutto ciò che si trova al di fuori di quel sistema è l'ambiente circostante. Ad esempio, quando si riscalda una pentola d'acqua sul fornello, il sistema include il fornello, la pentola e l'acqua. Trasferimenti di energia all'interno del sistema (tra il fornello, la pentola e l'acqua). Esistono due tipi di sistemi: aperto e chiuso. Un sistema aperto è un sistema in cui energia e materia possono trasferirsi tra il sistema e l'ambiente circostante. Il sistema del fornello è aperto perché può perdere calore nell'aria. Un sistema chiuso è un sistema che può trasferire energia ma non materia all'ambiente circostante.
Gli organismi biologici sono sistemi aperti. Scambi di energia tra loro e l'ambiente circostante, poiché consumano molecole che immagazzinano energia e rilasciano energia all'ambiente svolgendo lavoro. Come tutte le cose nel mondo fisico, l'energia è soggetta alle leggi della fisica. Le leggi della termodinamica regolano il trasferimento di energia in e tra tutti i sistemi nell'universo.
La prima legge della termodinamica
[modifica | modifica sorgente]La prima legge della termodinamica riguarda la quantità totale di energia nell'universo. Afferma che questa quantità totale di energia è costante. In altre parole, c'è sempre stata, e ci sarà sempre, esattamente la stessa quantità di energia nell'universo. L'energia esiste in molte forme diverse. Secondo la prima legge della termodinamica, l'energia può trasferirsi da un luogo all'altro o trasformarsi in forme diverse, ma non può essere creata o distrutta. I trasferimenti e le trasformazioni di energia avvengono continuamente intorno a noi. Le lampadine trasformano l'energia elettrica in energia luminosa. Le cucine a gas trasformano l'energia chimica del gas naturale in energia termica. Le piante eseguono una delle trasformazioni energetiche più utili dal punto di vista biologico sulla terra: quella di convertire l'energia della luce solare nell'energia chimica immagazzinata nelle molecole organiche (vedi galleria).
La sfida per tutti gli organismi viventi è quella di ottenere energia dall'ambiente circostante in forme che possano trasferire o trasformare in energia utilizzabile per svolgere un lavoro. Le cellule viventi si sono evolute per affrontare molto bene questa sfida. L'energia chimica immagazzinata nelle molecole organiche come zuccheri e grassi si trasforma attraverso una serie di reazioni chimiche cellulari in energia nelle molecole di ATP. L'energia nelle molecole di ATP è facilmente accessibile per svolgere un lavoro. Esempi dei tipi di lavoro che le cellule devono svolgere includono la costruzione di molecole complesse, il trasporto di materiali, l'alimentazione del movimento di ciglia o flagelli, la contrazione delle fibre muscolari per creare movimento e la riproduzione.
-
Proprietà dei sistemi isolati, chiusi e aperti nello scambio di energia e materia.
-
Il cibo è fonte di energia
-
Il movimento del corpo umano sfrutta l'energia chimica del cibo
-
Le piante sfruttano l'energia luminosa per sintetizzare le molecole chimiche
La seconda legge della termodinamica
[modifica | modifica sorgente]I compiti principali di una cellula vivente, ovvero ottenere, trasformare e utilizzare energia per svolgere un lavoro, possono sembrare semplici. Tuttavia, la seconda legge della termodinamica spiega perché questi compiti sono più difficili di quanto sembrino. Nessuno dei trasferimenti di energia di cui abbiamo parlato, insieme a tutti i trasferimenti e le trasformazioni di energia nell'universo, è completamente efficiente. In ogni trasferimento di energia, una certa quantità di energia viene persa in una forma inutilizzabile. Nella maggior parte dei casi, questa forma è energia termica. Termodinamicamente, gli scienziati definiscono l'energia termica come energia che si trasferisce da un sistema a un altro che non sta svolgendo un lavoro. Ad esempio, quando un aereo vola nell'aria, perde parte della sua energia come energia termica a causa dell'attrito con l'aria circostante. Questo attrito in realtà riscalda l'aria aumentando temporaneamente la velocità delle molecole d'aria. Allo stesso modo, parte dell'energia viene persa come energia termica durante le reazioni metaboliche cellulari. Questo è positivo per le creature a sangue caldo come noi, perché l'energia termica aiuta a mantenere la temperatura corporea. In senso stretto, nessun trasferimento di energia è completamente efficiente, perché parte dell'energia viene persa in una forma inutilizzabile.

Un concetto importante nei sistemi fisici è quello di ordine e disordine (o casualità). Più energia un sistema perde nell'ambiente circostante, meno ordinato e più casuale è il sistema. Gli scienziati chiamano entropia la misura della casualità o del disordine all'interno di un sistema . Un'entropia elevata significa un disordine elevato e una bassa energia ( Figura accanto). Per comprendere meglio l'entropia, pensa alla camera da letto di uno studente. Se non vi venissero immessi né energia né lavoro, la stanza diventerebbe rapidamente disordinata. Esisterebbe in uno stato molto disordinato, uno di alta entropia. L'energia deve essere immessa nel sistema, sotto forma di studente che lavora e mette via tutto, per riportare la stanza a uno stato di pulizia e ordine. Questo stato è uno di bassa entropia. Allo stesso modo, un'auto o una casa devono essere costantemente mantenute con lavoro per mantenerle in uno stato ordinato. Lasciate sole, l'entropia di una casa o di un'auto aumenta gradualmente attraverso la ruggine e la degradazione. Anche le molecole e le reazioni chimiche hanno quantità variabili di entropia. Ad esempio, quando le reazioni chimiche raggiungono uno stato di equilibrio, l'entropia aumenta e, quando le molecole ad alta concentrazione in un punto si diffondono e si espandono, anche l'entropia aumenta.
Pensa a tutti i sistemi fisici in questo modo: gli esseri viventi sono altamente ordinati e richiedono un apporto energetico costante per mantenersi in uno stato di bassa entropia. Quando i sistemi viventi assorbono molecole che immagazzinano energia e le trasformano attraverso reazioni chimiche, perdono una certa quantità di energia utilizzabile nel processo, perché nessuna reazione è completamente efficiente. Producono anche rifiuti e sottoprodotti che non sono fonti di energia utili. Questo processo aumenta l'entropia dell'ambiente circostante il sistema. Poiché tutti i trasferimenti di energia comportano la perdita di una certa energia utilizzabile, la seconda legge della termodinamica afferma che ogni trasferimento o trasformazione di energia aumenta l'entropia dell'universo. Anche se gli esseri viventi sono altamente ordinati e mantengono uno stato di bassa entropia, l'entropia totale dell'universo aumenta costantemente a causa della perdita di energia utilizzabile con ogni trasferimento di energia che si verifica. In sostanza, gli esseri viventi sono in una continua e dura battaglia contro questo costante aumento dell'entropia universale.
Esercizio: trasferimento di energia e entropia risultante
[modifica | modifica sorgente]Imposta un semplice esperimento per comprendere come avviene il trasferimento di energia e come si verifica una variazione di entropia.
- Prendiamo un blocco di ghiaccio. Questa è acqua in forma solida, quindi ha un ordine strutturale elevato. Ciò significa che le molecole non possono muoversi molto e sono in una posizione fissa. La temperatura del ghiaccio è 0°C. Di conseguenza, l'entropia del sistema è bassa.
- Lasciare che il ghiaccio si sciolga a temperatura ambiente. Qual è lo stato attuale delle molecole nell'acqua liquida? Come è avvenuto il trasferimento di energia? L'entropia del sistema è più alta o più bassa? Perché?
- Riscaldare l'acqua fino al punto di ebollizione. Cosa succede all'entropia del sistema quando l'acqua viene riscaldata?
L'ATP (adenosin trifosfato)
[modifica | modifica sorgente]Anche le reazioni esoergoniche che rilasciano energia richiedono una piccola quantità di energia di attivazione per procedere. Tuttavia, considerate le reazioni endoergoniche, che richiedono un apporto energetico molto maggiore, perché i loro prodotti hanno più energia libera rispetto ai loro reagenti. All'interno della cellula, da dove proviene l'energia per alimentare tali reazioni? La risposta sta in una molecola che fornisce energia che gli scienziati chiamano adenosina trifosfato , o ATP . Questa è una molecola piccola e relativamente semplice ( Figura sotto), ma all'interno di alcuni dei suoi legami, contiene il potenziale per una rapida scarica di energia che può essere sfruttata per svolgere il lavoro cellulare. Pensate a questa molecola come alla valuta energetica primaria delle cellule, più o meno nello stesso modo in cui il denaro è la valuta che le persone scambiano per le cose di cui hanno bisogno. L'ATP alimenta la maggior parte delle reazioni cellulari che richiedono energia.

Come suggerisce il nome, l'adenosina trifosfato è composta da adenosina legata a tre gruppi fosfato ( Figura sopra). L'adenosina è un nucleoside costituito dalla base azotata adenina e da uno zucchero a cinque atomi di carbonio, il ribosio. I tre gruppi fosfato, in ordine dal più vicino al più lontano dallo zucchero ribosio, sono alfa, beta e gamma. Insieme, questi gruppi chimici costituiscono una centrale elettrica. Tuttavia, non tutti i legami all'interno di questa molecola esistono in uno stato particolarmente ad alta energia. Entrambi i legami che collegano i fosfati sono legami ugualmente ad alta energia ( legami fosfoanidride ) che, quando vengono spezzati, rilasciano energia sufficiente per alimentare una varietà di reazioni e processi cellulari. Questi legami ad alta energia sono i legami tra il secondo e il terzo (o beta e gamma) gruppo fosfato e tra il primo e il secondo gruppo fosfato. Questi legami sono "ad alta energia" perché i prodotti di tale rottura di legame, adenosina difosfato (ADP) e un gruppo fosfato inorganico (P i ), hanno un'energia libera notevolmente inferiore rispetto ai reagenti: ATP e una molecola d'acqua. Poiché questa reazione avviene utilizzando una molecola d'acqua, è una reazione di idrolisi. In altre parole, l'ATP si idrolizza in ADP nella seguente reazione: ATP → ADP +Pi+ energia gratuita.
Come la maggior parte delle reazioni chimiche, l'idrolisi dell'ATP in ADP è reversibile. La reazione inversa rigenera l'ATP da ADP + P i . Le cellule contano sulla rigenerazione dell'ATP proprio come le persone contano sulla rigenerazione del denaro speso attraverso una sorta di reddito. Poiché l'idrolisi dell'ATP rilascia energia, la rigenerazione dell'ATP deve richiedere un apporto di energia libera. Questa equazione esprime la formazione dell'ATP: ADP + Pi+ energia libera → ATP.

Rimangono due importanti domande riguardo all'uso dell'ATP come fonte di energia. Quanta energia libera viene rilasciata esattamente con l'idrolisi dell'ATP e in che modo questa energia libera svolge un lavoro cellulare? Il ∆G calcolato per l'idrolisi di una mole di ATP in ADP e P i è −7,3 kcal/mole (−30,5 kJ/mol). Poiché questo calcolo è vero in condizioni standard, ci si aspetterebbe che esista un valore diverso in condizioni cellulari. Infatti, il ∆G per l'idrolisi di una mole di ATP in una cellula vivente è quasi il doppio del valore in condizioni standard: –14 kcal/mol (−57 kJ/mol).
L'ATP è una molecola altamente instabile. A meno che non venga rapidamente utilizzata per svolgere un lavoro, l'ATP si dissocia spontaneamente in ADP + P i , e l'energia libera rilasciata durante questo processo viene persa sotto forma di calore. La seconda domanda che abbiamo posto sopra riguarda il modo in cui il rilascio di energia dall'idrolisi dell'ATP esegue un lavoro all'interno della cellula. Ciò dipende da una strategia che gli scienziati chiamano accoppiamento energetico . Le cellule accoppiano la reazione esoergonica dell'idrolisi dell'ATP consentendo loro di procedere. Un esempio di accoppiamento energetico tramite ATP riguarda una pompa ionica transmembrana che è estremamente importante per la funzione cellulare. Questa pompa sodio-potassio (pompa Na + /K + ) spinge il sodio fuori dalla cellula e il potassio dentro la cellula ( Figura sotto). Una grande percentuale dell'ATP di una cellula alimenta questa pompa, perché i processi cellulari portano una notevole quantità di sodio nella cellula e potassio fuori da essa. La pompa lavora costantemente per stabilizzare le concentrazioni cellulari di sodio e potassio. Affinché la pompa compia un ciclo (esportando tre ioni Na+ e importando due ioni K + ), una molecola di ATP deve idrolizzare. Quando l'ATP si idrolizza, il suo fosfato gamma non si allontana semplicemente, ma si trasferisce effettivamente sulla proteina pompa. Gli scienziati chiamano questo processo di legame di un gruppo fosfato a una molecola fosforilazione. Come nella maggior parte dei casi di idrolisi dell'ATP, un fosfato dall'ATP si trasferisce su un'altra molecola. In uno stato fosforilato, la pompa Na + / K + ha più energia libera e viene attivata per subire un cambiamento conformazionale. Questo cambiamento le consente di rilasciare Na + all'esterno della cellula. Quindi lega K + extracellulare , che, attraverso un altro cambiamento conformazionale, fa sì che il fosfato si stacchi dalla pompa. Questo rilascio di fosfato attiva il rilascio di K + all'interno della cellula. In sostanza, l'energia rilasciata dall'idrolisi dell'ATP si accoppia con l'energia richiesta per alimentare la pompa e trasportare gli ioni Na + e K + . L'ATP esegue il lavoro cellulare utilizzando questa forma di base di accoppiamento energetico tramite fosforilazione.


Fosforilazione
[modifica | modifica sorgente]Spesso durante le reazioni metaboliche cellulari, come la sintesi e la degradazione dei nutrienti, alcune molecole devono alterare leggermente la loro conformazione per diventare substrati per la fase successiva nella serie di reazioni. Un esempio è durante le primissime fasi della respirazione cellulare, quando una molecola di glucosio di zucchero si scompone nel processo di glicolisi. Nella prima fase, l'ATP è necessario per fosforilare il glucosio, creando un intermedio ad alta energia ma instabile. Questa reazione di fosforilazione alimenta un cambiamento conformazionale che consente alla molecola di glucosio fosforilata di convertirsi nello zucchero fruttosio fosforilato. Il fruttosio è un intermedio necessario per far procedere la glicolisi. Qui, la reazione esoergonica dell'idrolisi dell'ATP si accoppia con la reazione endoergonica di conversione del glucosio in un intermedio fosforilato nel percorso. Ancora una volta, l'energia rilasciata dalla rottura di un legame fosfato all'interno dell'ATP è stata utilizzata per fosforilare un'altra molecola, creando un intermedio instabile e alimentando un importante cambiamento conformazionale.
La fosforilazione si riferisce all'aggiunta del fosfato (~P) al substrato. Quando il complesso "substrato~P" si rompe, l'energia viene utilizzata per modificare il substrato e convertirlo in un prodotto della reazione. La molecola di ADP e uno ione fosfato libero vengono rilasciati nel mezzo e sono disponibili per il riciclaggio attraverso il metabolismo cellulare.
Fosforilazione a livello del substrato
[modifica | modifica sorgente]Per fosforilazione a livello di substrato si intende la sintesi di ATP in seguito alla fosforilazione di ADP da parte di un certo substrato. Un gruppo fosfato viene rimosso da un reagente intermedio nel percorso e l'energia libera della reazione viene utilizzata per aggiungere il terzo fosfato a una molecola di ADP disponibile, producendo ATP.

Fosforilazione ossidativa
[modifica | modifica sorgente]La maggior parte dell'ATP generato durante il catabolismo del glucosio, tuttavia, deriva da un processo molto più complesso, la chemiosmosi, che avviene nei mitocondri ( Figura sotto) all'interno di una cellula eucariotica o della membrana plasmatica di una cellula procariotica. La chemiosmosi , un processo di produzione di ATP nel metabolismo cellulare, viene utilizzata per generare il 90 percento dell'ATP prodotto durante il catabolismo del glucosio ed è anche il metodo utilizzato nelle reazioni luminose della fotosintesi per sfruttare l'energia della luce solare. La produzione di ATP tramite il processo di chemiosmosi è chiamata fosforilazione ossidativa a causa del coinvolgimento dell'ossigeno nel processo.

Enzimi
[modifica | modifica sorgente]Una sostanza che aiuta una reazione chimica a verificarsi è un catalizzatore, e le molecole speciali che catalizzano le reazioni biochimiche sono enzimi. Quasi tutti gli enzimi sono proteine, composte da catene di amminoacidi, e svolgono il compito critico di abbassare le energie di attivazione delle reazioni chimiche all'interno della cellula. Gli enzimi lo fanno legandosi alle molecole reagenti e trattenendole in modo tale da rendere più facili i processi di rottura e formazione dei legami chimici. È importante ricordare che gli enzimi non cambiano il ∆G della reazione. In altre parole, non cambiano se una reazione è esoergonica (spontanea) o endoergonica. Questo perché non cambiano l'energia libera dei reagenti o dei prodotti. Riducono solo l'energia di attivazione richiesta per raggiungere lo stato di transizione ( Figura sotto).

Sito attivo dell'enzima e specificità del substrato
[modifica | modifica sorgente]I reagenti chimici a cui si lega un enzima sono i substrati dell'enzima . Possono esserci uno o più substrati, a seconda della particolare reazione chimica. In alcune reazioni, un substrato con un singolo reagente si scompone in più prodotti. In altre, due substrati possono unirsi per creare una molecola più grande. Due reagenti possono anche entrare in una reazione, entrambi modificati e lasciare la reazione come due prodotti. La posizione all'interno dell'enzima in cui si lega il substrato è il sito attivo dell'enzima . È qui che avviene l'"azione". Poiché gli enzimi sono proteine, c'è una combinazione unica di residui di amminoacidi (anche catene laterali o gruppi R) all'interno del sito attivo. Proprietà diverse caratterizzano ogni residuo. Questi possono essere grandi o piccoli, debolmente acidi o basici, idrofili o idrofobi, caricati positivamente o negativamente o neutri. La combinazione unica di residui di amminoacidi, le loro posizioni, sequenze, strutture e proprietà, crea un ambiente chimico molto specifico all'interno del sito attivo. Questo ambiente specifico è adatto a legarsi, anche se brevemente, a uno specifico substrato chimico (o substrati). Grazie a questa corrispondenza simile a un puzzle tra un enzima e i suoi substrati (che si adatta per trovare la migliore corrispondenza tra lo stato di transizione e il sito attivo), gli enzimi sono noti per la loro specificità. La "migliore corrispondenza" deriva dalla forma e dall'attrazione del gruppo funzionale dell'amminoacido verso il substrato. Esiste un enzima specificamente abbinato per ogni substrato e, quindi, per ogni reazione chimica; tuttavia, c'è anche flessibilità.
Il fatto che i siti attivi siano così perfettamente adatti a fornire condizioni ambientali specifiche significa anche che sono soggetti a influenze ambientali locali. È vero che aumentare la temperatura ambientale generalmente aumenta le velocità di reazione, catalizzate da enzimi o altro. Tuttavia, aumentare o diminuire la temperatura al di fuori di un intervallo ottimale può influenzare i legami chimici all'interno del sito attivo in modo tale che siano meno adatti a legare i substrati. Le alte temperature alla fine causeranno la denaturazione degli enzimi, come altre molecole biologiche, un processo che modifica le proprietà naturali della sostanza. Allo stesso modo, anche il pH dell'ambiente locale può influenzare la funzione enzimatica. I residui di amminoacidi del sito attivo hanno le loro proprietà acide o basiche che sono ottimali per la catalisi. Questi residui sono sensibili alle variazioni di pH che possono compromettere il modo in cui le molecole del substrato si legano. Gli enzimi sono adatti a funzionare al meglio entro un certo intervallo di pH e, come con la temperatura, valori estremi di pH ambientale (acidi o basici) possono causare la denaturazione degli enzimi.
-
Come la temperatura influenza l'attività di un enzima
-
Schema di funzionamento di un enzima
Adattamento indotto e funzione enzimatica
[modifica | modifica sorgente]Per molti anni, gli scienziati hanno pensato che il legame enzima-substrato avvenisse in un semplice modo "chiave-serratura". Questo modello affermava che l'enzima e il substrato si adattavano perfettamente in un unico passaggio istantaneo. Tuttavia, la ricerca attuale supporta una visione più raffinata che gli scienziati chiamano adattamento indotto ( Figura sotto). Questo modello amplia il modello chiave-serratura descrivendo un'interazione più dinamica tra enzima e substrato. Quando l'enzima e il substrato si uniscono, la loro interazione provoca un leggero spostamento nella struttura dell'enzima che conferma una disposizione di legame ideale tra l'enzima e lo stato di transizione del substrato. Questo legame ideale massimizza la capacità dell'enzima di catalizzare la sua reazione.
Quando un enzima lega il suo substrato, forma un complesso enzima-substrato. Questo complesso abbassa l'energia di attivazione della reazione e ne promuove la rapida progressione in uno dei tanti modi. A un livello di base, gli enzimi promuovono reazioni chimiche che coinvolgono più di un substrato riunendo i substrati in un orientamento ottimale. La regione appropriata (atomi e legami) di una molecola è giustapposta alla regione appropriata dell'altra molecola con cui deve reagire. Un altro modo in cui gli enzimi promuovono la reazione del substrato è creando un ambiente ottimale all'interno del sito attivo affinché la reazione avvenga. Alcune reazioni chimiche potrebbero procedere meglio in un ambiente leggermente acido o non polare. Le proprietà chimiche che emergono dalla particolare disposizione dei residui di amminoacidi all'interno di un sito attivo creano l'ambiente perfetto per la reazione dei substrati specifici di un enzima.
Hai imparato che l'energia di attivazione richiesta per molte reazioni include l'energia coinvolta nella manipolazione o nella leggera contorsione dei legami chimici in modo che possano facilmente rompersi e consentire ad altri di riformarsi. L'azione enzimatica può aiutare questo processo. Il complesso enzima-substrato può abbassare l'energia di attivazione contorcendo le molecole del substrato in modo tale da facilitare la rottura del legame, aiutando a raggiungere lo stato di transizione. Infine, gli enzimi possono anche abbassare le energie di attivazione prendendo parte alla reazione chimica stessa. I residui di amminoacidi possono fornire determinati ioni o gruppi chimici che in realtà formano legami covalenti con le molecole del substrato come passaggio necessario del processo di reazione. In questi casi, è importante ricordare che l'enzima tornerà sempre al suo stato originale al completamento della reazione. Una delle proprietà distintive degli enzimi è che rimangono in ultima analisi invariati dalle reazioni che catalizzano. Dopo che un enzima catalizza una reazione, rilascia il suo/i prodotto/i.

Video
[modifica | modifica sorgente]- BIOLOGIA - Lezione 15 - Gli Enzimi | Metabolismo Cellulare di La Biologia per tutti - video che spiega bene il funzionamento degli enzimi
- A Level Biology Revision "The Induced Fit Model of Enzyme Action" di Freesciencelessons - un video che approfondisce la differenza tra chiave-serratura e adattamento indotto.
-
Il lisozima. Siti di legame in blu, sito catalitico in rosso e substrato peptidoglicano in nero.
-
Fenilalanina idrossilasi
-
Modello con serratura e chiave
-
modello di adattamento indotto
Controllo del metabolismo attraverso la regolazione degli enzimi
[modifica | modifica sorgente]Sembrerebbe ideale avere uno scenario in cui tutti gli enzimi codificati nel genoma di un organismo esistessero in abbondanza e funzionassero in modo ottimale in tutte le condizioni cellulari, in tutte le cellule, in ogni momento. In realtà, questo è ben lungi dall'essere il caso. Una varietà di meccanismi assicura che ciò non accada. Le esigenze e le condizioni cellulari variano da cellula a cellula e cambiano all'interno delle singole cellule nel tempo. Gli enzimi richiesti e le richieste energetiche delle cellule dello stomaco sono diversi da quelli delle cellule di accumulo del grasso, delle cellule della pelle, delle cellule del sangue e delle cellule nervose. Inoltre, una cellula digestiva lavora molto più duramente per elaborare e scomporre i nutrienti durante il periodo che segue da vicino un pasto rispetto a molte ore dopo un pasto. Poiché queste esigenze e condizioni cellulari variano, lo stesso vale per le quantità e la funzionalità dei diversi enzimi.
Poiché le velocità delle reazioni biochimiche sono controllate dall'energia di attivazione e gli enzimi abbassano e determinano le energie di attivazione per le reazioni chimiche, le quantità relative e il funzionamento della varietà di enzimi all'interno di una cellula determinano in ultima analisi quali reazioni procederanno e a quali velocità. Questa determinazione è strettamente controllata. In certi ambienti cellulari, fattori ambientali come pH e temperatura controllano in parte l'attività enzimatica. Esistono altri meccanismi attraverso i quali le cellule controllano l'attività enzimatica e determinano le velocità a cui si verificheranno varie reazioni biochimiche.
Regolazione molecolare degli enzimi
[modifica | modifica sorgente]Gli enzimi possono essere regolati in modi che promuovono o riducono la loro attività. Esistono molti tipi diversi di molecole che inibiscono o promuovono la funzione enzimatica, ed esistono vari meccanismi per farlo. Ad esempio, in alcuni casi di inibizione enzimatica, una molecola inibitrice è abbastanza simile a un substrato da potersi legare al sito attivo e semplicemente impedire al substrato di legarsi. Quando ciò accade, l'enzima viene inibito tramite inibizione competitiva , perché una molecola inibitrice compete con il substrato per il legame al sito attivo ( Figura sotto). D'altro canto, nell'inibizione non competitiva , una molecola inibitrice si lega all'enzima in una posizione diversa dal sito attivo, chiamata sito allosterico, ma riesce comunque a impedire il legame del substrato al sito attivo. Alcune molecole inibitrici si legano agli enzimi in una posizione in cui il loro legame induce un cambiamento conformazionale che riduce l'attività enzimatica poiché non catalizza più efficacemente la conversione del substrato in prodotto.

Alcune molecole inibitrici si legano agli enzimi in una posizione in cui il loro legame induce un cambiamento conformazionale che riduce l'affinità dell'enzima per il suo substrato. Questo tipo di inibizione è un'inibizione allosterica ( Figura 6.18 ). Più di un polipeptide comprende la maggior parte degli enzimi regolati allostericamente, il che significa che hanno più di una subunità proteica. Quando un inibitore allosterico si lega a un enzima, tutti i siti attivi sulle subunità proteiche cambiano leggermente in modo tale da legare i loro substrati con minore efficienza. Esistono attivatori allosterici e inibitori. Gli attivatori allosterici si legano a posizioni su un enzima lontane dal sito attivo, inducendo un cambiamento conformazionale che aumenta l'affinità del/i sito/i attivo/i dell'enzima per il/i suo/i substrato/i.


Cofattori
[modifica | modifica sorgente]Molti enzimi non funzionano in modo ottimale, o addirittura non funzionano affatto, a meno che non siano legati ad altre molecole helper specifiche non proteiche, sia temporaneamente tramite legami ionici o idrogeno, sia in modo permanente tramite legami covalenti più forti. Due tipi di molecole helper sono gli attivatori e i coenzimi . Il legame a queste molecole promuove una conformazione e una funzione ottimali per i rispettivi enzimi. Gli attivatori sono ioni inorganici come ferro (Fe++) e magnesio (Mg++). Un esempio di enzima che richiede uno ione metallico come cofattore è l'enzima che costruisce molecole di DNA, la DNA polimerasi, che richiede uno ione zinco legato (Zn++) per funzionare. I coenzimi sono molecole helper organiche, con una struttura atomica di base composta da carbonio e idrogeno, che sono necessari per l'azione enzimatica. Le fonti più comuni di coenzimi sono le vitamine alimentari ( Figura 6.20 ). Alcune vitamine sono precursori dei coenzimi e altre agiscono direttamente come coenzimi. La vitamina C è un coenzima per più enzimi che prendono parte alla costruzione dell'importante componente del tessuto connettivo, il collagene. Un passaggio importante nella scomposizione del glucosio per produrre energia è la catalisi da parte di un complesso multienzimatico che gli scienziati chiamano piruvato deidrogenasi. La piruvato deidrogenasi è un complesso di diversi enzimi che in realtà richiede un cofattore (uno ione magnesio) e cinque diversi coenzimi organici per catalizzare la sua specifica reazione chimica. Pertanto, la funzione enzimatica è, in parte, regolata da un'abbondanza di vari cofattori e coenzimi, che la dieta della maggior parte degli organismi fornisce.
-
vitamina A (retinolo)
-
Vitamina B1 (Tiamina)
-
B2 - riboflavina
-
B6
-
Acido folico
-
Acido ascorbico (vitamina C)
-
D2 (calciferolo)
-
Vitamina E (tocoferolo)
-
Una bottiglia di integratore vitaminico del complesso B in pillole.
Compartimentazione enzimatica
[modifica | modifica sorgente]Nelle cellule eucariotiche, molecole come gli enzimi sono solitamente compartimentate in organelli diversi. Ciò consente un ulteriore livello di regolazione dell'attività enzimatica. Gli enzimi richiesti solo per determinati processi cellulari sono talvolta ospitati separatamente insieme ai loro substrati, consentendo reazioni chimiche più efficienti. Esempi di questo tipo di regolazione enzimatica basata sulla posizione e sulla prossimità includono gli enzimi coinvolti nelle ultime fasi della respirazione cellulare, che hanno luogo esclusivamente nei mitocondri, e gli enzimi coinvolti nella digestione di detriti cellulari e materiali estranei, situati all'interno dei lisosomi.
Inibizione del feedback nei percorsi metabolici
[modifica | modifica sorgente]Le molecole possono regolare la funzione enzimatica in molti modi. Tuttavia, rimane una domanda importante: cosa sono queste molecole e da dove provengono? Alcune sono cofattori e coenzimi, ioni e molecole organiche, come hai imparato. Quali altre molecole nella cellula forniscono regolazione enzimatica, come modulazione allosterica e inibizione competitiva e non competitiva? La risposta è che un'ampia varietà di molecole può svolgere questi ruoli. Alcune includono farmaci farmaceutici e non farmaceutici, tossine e veleni dall'ambiente. Forse le fonti più rilevanti di molecole regolatrici degli enzimi, rispetto al metabolismo cellulare, sono i prodotti di reazione metabolica cellulare stessi. Nel modo più efficiente ed elegante, le cellule si sono evolute per utilizzare i prodotti delle proprie reazioni per l'inibizione a feedback dell'attività enzimatica. L' inibizione a feedback comporta l'utilizzo di un prodotto di reazione per regolare la propria ulteriore produzione ( Figura sotto). La cellula risponde all'abbondanza di prodotti specifici rallentando la produzione durante le reazioni anaboliche o cataboliche. Tali prodotti di reazione possono inibire gli enzimi che catalizzano la loro produzione attraverso i meccanismi descritti sopra.

La produzione sia di amminoacidi che di nucleotidi è controllata tramite inibizione da feedback. Inoltre, l'ATP è un regolatore allosterico di alcuni degli enzimi coinvolti nella degradazione catabolica dello zucchero, il processo che produce ATP. In questo modo, quando l'ATP è abbondante, la cellula può impedirne l'ulteriore produzione. Ricorda che l'ATP è una molecola instabile che può dissociarsi spontaneamente in ADP e fosfato inorganico. Se in una cellula fosse presente troppo ATP, gran parte di esso andrebbe sprecato. In alternativa, l'ADP funge da regolatore allosterico positivo (un attivatore allosterico) per alcuni degli stessi enzimi che l'ATP inibisce. Quindi, quando i livelli relativi di ADP sono elevati rispetto all'ATP, la cellula viene stimolata a produrre più ATP tramite il catabolismo dello zucchero.
Reazioni redox
[modifica | modifica sorgente]La conversione di energia all'interno di una cellula coinvolge molti percorsi chimici coordinati. La maggior parte di questi percorsi sono combinazioni di reazioni di ossidazione e riduzione, che si verificano contemporaneamente. Una reazione di ossidazione strappa un elettrone da un atomo in un composto, e l'aggiunta di questo elettrone a un altro composto è una reazione di riduzione. Poiché l'ossidazione e la riduzione di solito si verificano insieme, queste coppie di reazioni sono chiamate reazioni di ossidoriduzione o reazioni redox.

Elettroni ed energia
[modifica | modifica sorgente]La rimozione di un elettrone da una molecola (ossidandola) determina una diminuzione dell'energia potenziale nel composto ossidato. Tuttavia, l'elettrone (a volte come parte di un atomo di idrogeno) non rimane non legato nel citoplasma di una cellula. Piuttosto, l'elettrone viene spostato in un secondo composto, riducendo il secondo composto. Lo spostamento di un elettrone da un composto all'altro rimuove parte dell'energia potenziale dal primo composto (il composto ossidato) e aumenta l'energia potenziale del secondo composto (il composto ridotto). Il trasferimento di elettroni tra molecole è importante perché la maggior parte dell'energia immagazzinata negli atomi e utilizzata per alimentare le funzioni delle celle è sotto forma di elettroni ad alta energia. Il trasferimento di energia sotto forma di elettroni ad alta energia consente alla cellula di trasferire e utilizzare l'energia in modo incrementale, in piccoli pacchetti piuttosto che in un'unica, distruttiva esplosione. Questo capitolo si concentra sull'estrazione di energia dal cibo; vedrai che mentre segui il percorso dei trasferimenti, stai seguendo il percorso degli elettroni che si muovono attraverso i percorsi metabolici.
Portatori di elettroni
[modifica | modifica sorgente]Nei sistemi viventi, una piccola classe di composti funziona come navette elettroniche: legano e trasportano elettroni ad alta energia tra composti in percorsi biochimici. I principali trasportatori di elettroni che prenderemo in considerazione derivano dal gruppo della vitamina B e sono derivati dei nucleotidi. Questi composti possono essere facilmente ridotti (ovvero accettano elettroni) o ossidati (perdono elettroni). Il nicotinamide adenina dinucleotide (NAD) ( Figura 7.3 ) deriva dalla vitamina B 3 , niacina. NAD + è la forma ossidata della molecola; NADH è la forma ridotta della molecola dopo che ha accettato due elettroni e un protone (che insieme sono l'equivalente di un atomo di idrogeno con un elettrone in più). Nota che se un composto ha una "H" su di esso, è generalmente ridotto (ad esempio, NADH è la forma ridotta di NAD).
Il NAD + può accettare elettroni da una molecola organica secondo l'equazione generale: RH + NAD+ --> NADH + R+

Quando vengono aggiunti elettroni a un composto, questo viene ridotto . Un composto che ne riduce un altro è chiamato agente riducente. Nell'equazione precedente, RH è un agente riducente e NAD + viene ridotto a NADH. Quando vengono rimossi elettroni da un composto, questo viene ossidato . Un composto che ne ossida un altro è chiamato agente ossidante. Nell'equazione precedente, NAD + è un agente ossidante e RH viene ossidato a R.
Allo stesso modo, il flavin adenin dinucleotide (FAD+ ) deriva dalla vitamina B2 , detta anche riboflavina. La sua forma ridotta è FADH2 . Una seconda variante del NAD, il NADP, contiene un gruppo fosfato extra. Sia il NAD+ che il FAD+ sono ampiamente utilizzati nell'estrazione di energia dagli zuccheri e il NADP svolge un ruolo importante nelle reazioni anaboliche e nella fotosintesi nelle piante.
-
Struttura completa del NAD+
-
Struttura del FAD
-
Funzionamento del FAD
-
Il NADP è simile al NAD ma si trova nelle piante
Il metabolismo del glucosio
[modifica | modifica sorgente]Come hai letto, quasi tutta l'energia utilizzata dalle cellule viventi arriva loro nei legami dello zucchero glucosio. La glicolisi è il primo passaggio nella scomposizione del glucosio per estrarre energia per il metabolismo cellulare. Infatti, quasi tutti gli organismi viventi eseguono la glicolisi come parte del loro metabolismo. Il processo non utilizza direttamente l'ossigeno e quindi è definito anaerobico . La glicolisi avviene nel citoplasma sia delle cellule procariotiche che eucariotiche. Il glucosio entra nelle cellule eterotrofiche in due modi. Un metodo è attraverso il trasporto attivo secondario in cui il trasporto avviene contro il gradiente di concentrazione del glucosio. L'altro meccanismo utilizza un gruppo di proteine integrali chiamate proteine GLUT , note anche come proteine trasportatrici del glucosio. Questi trasportatori aiutano nella diffusione facilitata del glucosio.
La glicolisi inizia con la struttura ad anello a sei atomi di carbonio di una singola molecola di glucosio e termina con due molecole di uno zucchero a tre atomi di carbonio chiamato piruvato . La glicolisi consiste di due fasi distinte. La prima parte del percorso della glicolisi intrappola la molecola di glucosio nella cellula e usa energia per modificarla in modo che la molecola di zucchero a sei atomi di carbonio possa essere divisa uniformemente nelle due molecole a tre atomi di carbonio. La seconda parte della glicolisi estrae energia dalle molecole e la immagazzina sotto forma di ATP e NADH (ricorda: questa è la forma ridotta di NAD).

Prima metà della glicolisi (fasi che richiedono energia)
[modifica | modifica sorgente]Fase 1. La prima fase della glicolisi ( Figura sotto) è catalizzata dall'esochinasi, un enzima con ampia specificità che catalizza la fosforilazione di zuccheri a sei atomi di carbonio. L'esochinasi fosforila il glucosio usando l'ATP come fonte del fosfato, producendo glucosio-6-fosfato, una forma più reattiva di glucosio. Questa reazione impedisce alla molecola di glucosio fosforilata di continuare a interagire con le proteine GLUT e non può più lasciare la cellula perché il fosfato caricato negativamente non gli consentirà di attraversare l'interno idrofobico della membrana plasmatica.
Fase 2. Nella seconda fase della glicolisi, un'isomerasi converte il glucosio-6-fosfato in uno dei suoi isomeri, il fruttosio-6-fosfato (questo isomero ha un fosfato attaccato nella posizione del sesto carbonio dell'anello). Un'isomerasi è un enzima che catalizza la conversione di una molecola in uno dei suoi isomeri. (Questo cambiamento da fosfoglucosio a fosfofruttosio consente l'eventuale scissione dello zucchero in due molecole a tre atomi di carbonio.)
Fase 3. La terza fase è la fosforilazione del fruttosio-6-fosfato, catalizzata dall'enzima fosfofruttochinasi. Una seconda molecola di ATP dona un fosfato ad alta energia al fruttosio-6-fosfato, producendo fruttosio-1,6-bisfosfato. In questo pathway, la fosfofruttochinasi è un enzima limitante la velocità. È attivo quando la concentrazione di ADP è elevata; è meno attivo quando i livelli di ADP sono bassi e la concentrazione di ATP è elevata. Quindi, se c'è "sufficiente" ATP nel sistema, il pathway rallenta. Questo è un tipo di inibizione del prodotto finale, poiché l'ATP è il prodotto finale del catabolismo del glucosio.
Fase 4. I fosfati ad alta energia appena aggiunti destabilizzano ulteriormente il fruttosio-1,6-bisfosfato. La quarta fase della glicolisi impiega un enzima, l'aldolasi, per scindere il fruttosio-1,6-bisfosfato in due isomeri a tre atomi di carbonio: diidrossiacetone fosfato e gliceraldeide-3-fosfato.
Fase 5. Nella quinta fase, un'isomerasi trasforma il diidrossiacetone-fosfato nel suo isomero, la gliceraldeide-3-fosfato. Quindi, il percorso continuerà con due molecole di una gliceraldeide-3-fosfato. A questo punto del percorso, c'è un investimento netto di energia da due molecole di ATP nella scomposizione di una molecola di glucosio.

Seconda metà della glicolisi (fasi di rilascio di energia)
[modifica | modifica sorgente]Finora, la glicolisi è costata alla cellula due molecole di ATP e ha prodotto due piccole molecole di zucchero a tre atomi di carbonio. Entrambe queste molecole procederanno attraverso la seconda metà del percorso e verrà estratta energia sufficiente per ripagare le due molecole di ATP utilizzate come investimento iniziale e produrre un profitto per la cellula di due molecole di ATP aggiuntive e due molecole di NADH ancora più energetiche.
Fase 6. La sesta fase della glicolisi ( Figura sopra) ossida lo zucchero (gliceraldeide-3-fosfato), estraendo elettroni ad alta energia, che vengono raccolti dal trasportatore di elettroni NAD + , producendo NADH. Lo zucchero viene quindi fosforilato dall'aggiunta di un secondo gruppo fosfato, producendo 1,3-bisfosfoglicerato. Si noti che il secondo gruppo fosfato non richiede un'altra molecola di ATP.
Figura 7.9 La seconda metà della glicolisi comporta la fosforilazione senza investimento di ATP (fase 6) e produce due molecole di NADH e quattro molecole di ATP per glucosio.
Anche qui c'è un potenziale fattore limitante per questo percorso. La continuazione della reazione dipende dalla disponibilità della forma ossidata del trasportatore di elettroni, NAD + . Quindi, il NADH deve essere continuamente ossidato di nuovo in NAD + per continuare questo passaggio. Se il NAD + non è disponibile, la seconda metà della glicolisi rallenta o si ferma. Se l'ossigeno è disponibile nel sistema, il NADH verrà ossidato facilmente, anche se indirettamente, e gli elettroni ad alta energia dall'idrogeno rilasciato in questo processo saranno utilizzati per produrre ATP. In un ambiente senza ossigeno, un percorso alternativo (fermentazione) può fornire l'ossidazione del NADH in NAD + .
Fase 7. Nella settima fase, catalizzata dalla fosfoglicerato chinasi (un enzima chiamato così per la reazione inversa), l'1,3-bisfosfoglicerato dona un fosfato ad alta energia all'ADP, formando una molecola di ATP. (Questo è un esempio di fosforilazione a livello di substrato.) Un gruppo carbonilico sull'1,3-bisfosfoglicerato viene ossidato a un gruppo carbossilico e si forma il 3-fosfoglicerato.
Fase 8. Nell'ottava fase, il gruppo fosfato rimanente nel 3-fosfoglicerato si sposta dal terzo al secondo atomo di carbonio, producendo 2-fosfoglicerato (un isomero del 3-fosfoglicerato). L'enzima che catalizza questa fase è una mutasi (isomerasi).
Fase 9. L'enolasi catalizza la nona fase. Questo enzima fa sì che il 2-fosfoglicerato perda acqua dalla sua struttura; questa è una reazione di disidratazione, che porta alla formazione di un doppio legame che aumenta l'energia potenziale nel legame fosfato rimanente e produce fosfoenolpiruvato (PEP).
Fase 10. L'ultimo passaggio della glicolisi è catalizzato dall'enzima piruvato chinasi (l'enzima in questo caso prende il nome dalla reazione inversa della conversione del piruvato in PEP) e determina la produzione di una seconda molecola di ATP tramite fosforilazione a livello del substrato e del composto acido piruvico (o la sua forma di sale, piruvato). Molti enzimi nei percorsi enzimatici prendono il nome dalle reazioni inverse, poiché l'enzima può catalizzare sia reazioni dirette che inverse (queste potrebbero essere state descritte inizialmente dalla reazione inversa che avviene in vitro, in condizioni non fisiologiche).
Video utili
[modifica | modifica sorgente]BIOLOGIA - Lezione 16 - La Glicolisi | Metabolismo Cellulare
Risultati della glicolisi
[modifica | modifica sorgente]
La glicolisi inizia con il glucosio e produce due molecole di piruvato, quattro nuove molecole di ATP e due molecole di NADH. (Nota: due molecole di ATP vengono utilizzate nella prima metà del percorso per preparare l'anello a sei atomi di carbonio per la scissione, quindi la cellula ha un guadagno netto di due molecole di ATP e due molecole di NADH per il suo utilizzo). Se la cellula non riesce a catabolizzare ulteriormente le molecole di piruvato, raccoglierà solo due molecole di ATP da una molecola di glucosio. I globuli rossi maturi dei mammiferi non hanno mitocondri e quindi non sono in grado di respirazione aerobica, il processo in cui gli organismi convertono l'energia in presenza di ossigeno, e la glicolisi è la loro unica fonte di ATP. Se la glicolisi viene interrotta, queste cellule perdono la loro capacità di mantenere le loro pompe sodio-potassio e alla fine muoiono.
L'ultimo passaggio della glicolisi non si verificherà se la piruvato chinasi, l'enzima che catalizza la formazione del piruvato, non è disponibile in quantità sufficienti. In questa situazione, l'intero percorso della glicolisi procederà, ma solo due molecole di ATP saranno prodotte nella seconda metà. Quindi, la piruvato chinasi è un enzima che limita la velocità della glicolisi.
Ossidazione del piruvato e ciclo dell'acido citrico
[modifica | modifica sorgente]
Se l'ossigeno è disponibile, la respirazione aerobica andrà avanti. Nelle cellule eucariotiche, le molecole di piruvato prodotte alla fine della glicolisi vengono trasportate nei mitocondri, che sono i siti della respirazione cellulare. Lì, il piruvato viene trasformato in un gruppo acetile che verrà raccolto e attivato da un composto vettore chiamato coenzima A (CoA). Il composto risultante è chiamato acetil CoA . Il CoA è derivato dalla vitamina B5, acido pantotenico. L'acetil CoA può essere utilizzato in vari modi dalla cellula, ma la sua funzione principale è quella di trasportare il gruppo acetile derivato dal piruvato alla fase successiva del percorso nel catabolismo del glucosio.
Scomposizione del piruvato
[modifica | modifica sorgente]
Affinché il piruvato, il prodotto della glicolisi, possa entrare nel percorso successivo, deve subire diversi cambiamenti. La conversione è un processo in tre fasi. Entrando nella matrice mitocondriale, un complesso multienzimatico (Piruvato deidrogenasi) converte il piruvato in acetil CoA. Nel processo, viene rilasciata anidride carbonica e si forma una molecola di NADH
Fase 1. Un gruppo carbossilico viene rimosso dal piruvato, rilasciando una molecola di anidride carbonica nel mezzo circostante. Questa reazione crea un gruppo idrossietilico a due atomi di carbonio legato all'enzima (piruvato deidrogenasi). Dobbiamo notare che questo è il primo dei sei atomi di carbonio della molecola di glucosio originale a essere rimosso. (Questa fase procede due volte perché ci sono due molecole di piruvato prodotte alla fine della glicole per ogni molecola di glucosio metabolizzata anaerobicamente; quindi, due dei sei atomi di carbonio saranno stati rimossi alla fine di entrambe le fasi.)
Fase 2. Il gruppo idrossietilico viene ossidato a un gruppo acetile e gli elettroni vengono catturati da NAD + , formando NADH. Gli elettroni ad alta energia di NADH saranno utilizzati in seguito per generare ATP.
Fase 3. Il gruppo acetile legato all'enzima viene trasferito al CoA, producendo una molecola di acetil CoA.
Ciclo dell'acido citrico
[modifica | modifica sorgente]In presenza di ossigeno, l'acetil CoA rilascia il suo gruppo acetile (2C) a una molecola a quattro atomi di carbonio, l'ossalacetato, per formare il citrato, una molecola a sei atomi di carbonio con tre gruppi carbossilici; questo percorso raccoglierà il resto dell'energia estraibile da quella che è iniziata come una molecola di glucosio e rilascerà le restanti quattro molecole di CO 2 . Questo singolo percorso è chiamato con nomi diversi: ciclo dell'acido citrico (per il primo intermedio formato, l'acido citrico o citrato, quando l'acetato si unisce all'ossalacetato), ciclo TCA (perché l'acido citrico o citrato e l'isocitrato sono acidi tricarbossilici) e ciclo di Krebs, da Hans Krebs, che per primo identificò i passaggi del percorso negli anni '30 nei muscoli del volo dei piccioni.

Come la conversione del piruvato in acetil CoA, il ciclo dell'acido citrico avviene nella matrice dei mitocondri. Quasi tutti gli enzimi del ciclo dell'acido citrico sono solubili, con la sola eccezione dell'enzima succinato deidrogenasi, che è incorporato nella membrana interna del mitocondrio. A differenza della glicolisi, il ciclo dell'acido citrico è un ciclo chiuso: l'ultima parte del percorso rigenera il composto utilizzato nel primo passaggio. Gli otto passaggi del ciclo sono una serie di reazioni di redox, disidratazione, idratazione e decarbossilazione che producono due molecole di anidride carbonica, una GTP/ATP e i trasportatori ridotti NADH e FADH2. Questo è considerato un percorso aerobico perché il NADH e il FADH 2 prodotti devono trasferire i loro elettroni al percorso successivo nel sistema, che utilizzerà l'ossigeno. Se questo trasferimento non avviene, non si verificano nemmeno i passaggi di ossidazione del ciclo dell'acido citrico. Si noti che il ciclo dell'acido citrico produce direttamente pochissimo ATP e non consuma direttamente ossigeno.
Fasi del ciclo dell'acido citrico
[modifica | modifica sorgente]Fase 1. Prima della prima fase, si verifica una fase di transizione durante la quale l'acido piruvico viene convertito in acetil CoA. Quindi, inizia la prima fase del ciclo: questa fase di condensazione combina il gruppo acetile a due atomi di carbonio con una molecola di ossalacetato a quattro atomi di carbonio per formare una molecola di citrato a sei atomi di carbonio. Il CoA è legato a un gruppo solfidrilico (-SH) e si diffonde via per combinarsi infine con un altro gruppo acetile. Questa fase è irreversibile perché è altamente esoergonica. La velocità di questa reazione è controllata dal feedback negativo e dalla quantità di ATP disponibile. Se i livelli di ATP aumentano, la velocità di questa reazione diminuisce. Se l'ATP è scarso, la velocità aumenta.
Fase 2. Nella seconda fase, il citrato perde una molecola d'acqua e ne guadagna un'altra mentre il citrato viene convertito nel suo isomero, l'isocitrato.
Fase 3. Nella fase tre, l'isocitrato viene ossidato, producendo una molecola a cinque atomi di carbonio, α-chetoglutarato, insieme a una molecola di CO 2 e due elettroni, che riducono NAD + a NADH. Questa fase è anche regolata dal feedback negativo di ATP e NADH e da un effetto positivo di ADP.
Fase 4. Le fasi tre e quattro sono entrambe fasi di ossidazione e decarbossilazione, che come abbiamo visto, rilasciano elettroni che riducono NAD + a NADH e rilasciano gruppi carbossilici che formano molecole di CO2 . L'alfa-chetoglutarato è il prodotto della fase tre e un gruppo succinilico è il prodotto della fase quattro. Il CoA si lega al gruppo succinilico per formare succinil CoA. L'enzima che catalizza la fase quattro è regolato dall'inibizione del feedback di ATP, succinil CoA e NADH.
Fase 5. Nella fase cinque, un gruppo carbossilico viene sostituito al coenzima A e si forma un legame ad alta energia. Questa energia viene utilizzata nella fosforilazione a livello del substrato (durante la conversione del gruppo succinilico in succinato) per formare guanosina trifosfato (GTP) o ATP. Esistono due forme dell'enzima, chiamate isoenzimi, per questa fase, a seconda del tipo di tessuto animale in cui si trovano. Una forma si trova nei tessuti che utilizzano grandi quantità di ATP, come il cuore e il muscolo scheletrico. Questa forma produce ATP. La seconda forma dell'enzima si trova nei tessuti che hanno un numero elevato di percorsi anabolici, come il fegato. Questa forma produce GTP. GTP è energeticamente equivalente ad ATP; tuttavia, il suo utilizzo è più limitato. In particolare, la sintesi proteica utilizza principalmente GTP.
Fase 6. La fase sei è un processo di deidrogenazione che converte il succinato in fumarato. Due atomi di idrogeno vengono trasferiti al FAD, riducendolo a FADH 2 . (Nota: l'energia contenuta negli elettroni di questi idrogeni è insufficiente per ridurre il NAD + ma adeguata per ridurre il FAD.) A differenza del NADH, questo trasportatore rimane attaccato all'enzima e trasferisce gli elettroni direttamente alla catena di trasporto degli elettroni. Questo processo è reso possibile dalla localizzazione dell'enzima che catalizza questa fase all'interno della membrana interna del mitocondrio.
Fase 7. L'acqua viene aggiunta per idratazione al fumarato durante la fase sette e viene prodotto il malato. L'ultima fase del ciclo dell'acido citrico rigenera l'ossalacetato ossidando il malato. Un'altra molecola di NADH viene quindi prodotta nel processo.
Collegamento all'apprendimento
[modifica | modifica sorgente]Guarda qui un'animazione del ciclo dell'acido citrico .
Prodotti del ciclo dell'acido citrico
[modifica | modifica sorgente]Due atomi di carbonio entrano nel ciclo dell'acido citrico da ogni gruppo acetile, che rappresentano quattro dei sei atomi di carbonio di una molecola di glucosio. Due molecole di anidride carbonica vengono rilasciate a ogni giro del ciclo; tuttavia, queste non contengono necessariamente gli atomi di carbonio aggiunti più di recente. I due atomi di carbonio acetile verranno infine rilasciati nei giri successivi del ciclo; quindi, tutti e sei gli atomi di carbonio della molecola di glucosio originale vengono infine incorporati nell'anidride carbonica. Ogni giro del ciclo forma tre molecole di NADH e una molecola di FADH 2 . Questi trasportatori si collegheranno all'ultima parte della respirazione aerobica, la catena di trasporto degli elettroni, per produrre molecole di ATP. Un GTP o ATP viene anche prodotto in ogni ciclo. Molti dei composti intermedi nel ciclo dell'acido citrico possono essere utilizzati nella sintesi di amminoacidi non essenziali; pertanto, il ciclo è anfibolico (sia catabolico che anabolico).
| Descrizione | Reagenti | Prodotti |
|---|---|---|
| La somma di tutte le reazioni nel ciclo dell'acido citrico è: | Acetil-CoA + 3 NAD+ + FAD + GDP + Pi + 2 H2O | → CoA-SH + 3 NADH + FADH2 + 3 H+ + GTP + 2 CO2 |
| Combinando le reazioni che avvengono durante l' ossidazione del piruvato con quelle che avvengono durante il ciclo dell'acido citrico, si ottiene la seguente reazione complessiva di ossidazione del piruvato: | Ione piruvato + 4 NAD+ + FAD + GDP + Pi + 2 H2O | → 4 NADH + FADH 2 + 4 H+ + GTP + 3 CO2 |
| Combinando la reazione di cui sopra con quelle che si verificano nel corso della glicolisi , si ottiene la seguente reazione complessiva di ossidazione del glucosio (escluse le reazioni nella catena respiratoria): | Glucosio + 10 NAD+ + 2 FAD + 2 ADP + 2 GDP + 4 Pi + 2 H2O | → 10 NADH + 2 FADH 2 + 10 H+ + 2 ATP + 2 GTP + 6 CO2 |
Le reazioni di cui sopra sono bilanciate se Pi rappresenta lo ione H2PO 4 − , ADP e GDP rispettivamente gli ioni ADP2− e GDP2− , e ATP e GTP rispettivamente gli ioni ATP3− e GTP3− .
Si stima che il numero totale di molecole di ATP ottenute dopo l'ossidazione completa di un glucosio nella glicolisi, nel ciclo dell'acido citrico e nella fosforilazione ossidativa sia compreso tra 30 e 38.
Fosforilazione ossidativa
[modifica | modifica sorgente]Hai appena letto di due percorsi nel catabolismo del glucosio, la glicolisi e il ciclo dell'acido citrico, che generano ATP. Tuttavia, la maggior parte dell'ATP generato durante il catabolismo aerobico del glucosio non viene generata direttamente da questi percorsi. Invece, deriva da un processo che inizia spostando gli elettroni attraverso una serie di trasportatori di elettroni che subiscono reazioni redox. Questo processo fa sì che gli ioni idrogeno si accumulino all'interno dello spazio intermembranoso. Pertanto, si forma un gradiente di concentrazione in cui gli ioni idrogeno diffondono dallo spazio intermembranoso nella matrice mitocondriale passando attraverso l'ATP sintasi. La corrente di ioni idrogeno alimenta l'azione catalitica dell'ATP sintasi, che fosforila l'ADP, producendo ATP.
Catena di trasporto degli elettroni
[modifica | modifica sorgente]La catena di trasporto degli elettroni ( Figura sotto) è l'ultimo componente della respirazione aerobica ed è l'unica parte del metabolismo del glucosio che utilizza l'ossigeno atmosferico. L'ossigeno si diffonde continuamente nei tessuti delle piante (tipicamente attraverso gli stomi), così come nei funghi e nei batteri; tuttavia, negli animali, l'ossigeno entra nel corpo attraverso una varietà di sistemi respiratori. Il trasporto degli elettroni è una serie di reazioni redox che assomigliano a una staffetta o a una brigata di secchi in quanto gli elettroni vengono passati rapidamente da un componente all'altro, fino al punto finale della catena in cui gli elettroni riducono l'ossigeno molecolare e, insieme ai protoni associati, producono acqua. Ci sono quattro complessi composti da proteine, etichettati da I a IV nella Figura sotto, e l'aggregazione di questi quattro complessi, insieme ai trasportatori di elettroni mobili e accessori associati, è chiamata catena di trasporto degli elettroni . La catena di trasporto degli elettroni è presente con copie multiple nella membrana mitocondriale interna degli eucarioti e all'interno della membrana plasmatica dei procarioti.

Complesso I
[modifica | modifica sorgente]Innanzitutto, due elettroni vengono trasportati al primo complesso tramite NADH. Questo complesso, etichettato I , è composto da flavina mononucleotide (FMN) e una proteina contenente ferro-zolfo (Fe-S). FMN, che deriva dalla vitamina B 2 (detta anche riboflavina), è uno dei diversi gruppi prostetici o cofattori nella catena di trasporto degli elettroni. Un gruppo prostetico è una molecola non proteica necessaria per l'attività di una proteina. I gruppi prostetici sono molecole organiche o inorganiche, non peptidiche legate a una proteina che ne facilitano la funzione. I gruppi prostetici includono coenzimi, che sono i gruppi prostetici degli enzimi. L'enzima nel complesso I è NADH deidrogenasi ed è composto da 44 catene polipeptidiche separate. Il complesso I può pompare quattro ioni idrogeno attraverso la membrana dalla matrice nello spazio intermembrana, ed è in questo modo che il gradiente di ioni idrogeno viene stabilito e mantenuto tra i due compartimenti separati dalla membrana mitocondriale interna.
Q e Complesso II
[modifica | modifica sorgente]Il complesso II riceve direttamente FADH2 , che non passa attraverso il complesso I. Il composto che collega il primo e il secondo complesso al terzo è l'ubiquinone B. La molecola Q è liposolubile e si muove liberamente attraverso il nucleo idrofobico della membrana. Una volta ridotto (QH2 ), l'ubiquinone consegna i suoi elettroni al complesso successivo nella catena di trasporto degli elettroni. Q riceve gli elettroni derivati da NADH dal complesso I e gli elettroni derivati da FADH 2 dal complesso II. Questo enzima e FADH 2 formano un piccolo complesso che consegna gli elettroni direttamente alla catena di trasporto degli elettroni, bypassando il primo complesso. Poiché questi elettroni bypassano e quindi non energizzano la pompa protonica nel primo complesso, vengono prodotte meno molecole di ATP dagli elettroni FADH 2. Il numero di molecole di ATP ottenute alla fine è direttamente proporzionale al numero di protoni pompati attraverso la membrana mitocondriale interna.
Complesso III
[modifica | modifica sorgente]Il terzo complesso è composto da citocromo b, un'altra proteina Fe-S, un centro Rieske (centro 2Fe-2S) e proteine del citocromo c. Questo complesso è anche chiamato citocromo ossidoreduttasi. Le proteine del citocromo hanno un gruppo prostetico di eme. La molecola di eme è simile all'eme nell'emoglobina, ma trasporta elettroni, non ossigeno. Di conseguenza, lo ione ferro al suo interno viene ridotto e ossidato mentre passa gli elettroni, fluttuando tra diversi stati di ossidazione: Fe ++ (ridotto) e Fe +++ (ossidato). Le molecole di eme nei citocromi hanno caratteristiche leggermente diverse a causa degli effetti delle diverse proteine che si legano a loro, conferendo caratteristiche leggermente diverse a ciascun complesso. Il complesso III pompa protoni attraverso la membrana e passa i suoi elettroni al citocromo c per il trasporto al quarto complesso di proteine ed enzimi. (Il citocromo c riceve elettroni da Q; tuttavia, mentre Q trasporta coppie di elettroni, il citocromo c può accettarne solo uno alla volta.)
Complesso IV
[modifica | modifica sorgente]Il quarto complesso è composto dalle proteine del citocromo c, a e a 3 . Questo complesso contiene due gruppi eme (uno in ciascuno dei due citocromi, a e a 3 ) e tre ioni rame (una coppia di Cu A e un Cu B nel citocromo a 3 ). I citocromi tengono una molecola di ossigeno molto stretta tra gli ioni ferro e rame finché l'ossigeno non viene completamente ridotto dall'acquisizione di due elettroni. L'ossigeno ridotto quindi raccoglie due ioni idrogeno dal mezzo circostante per produrre acqua (H2O). La rimozione degli ioni idrogeno dal sistema contribuisce al gradiente ionico che costituisce la base per il processo di chemiosmosi.
Chemiosmosi
[modifica | modifica sorgente]Nella chemiosmosi, l'energia libera dalla serie di reazioni redox appena descritte viene utilizzata per pompare ioni idrogeno (protoni) attraverso la membrana mitocondriale. La distribuzione non uniforme degli ioni H + attraverso la membrana stabilisce sia la concentrazione che i gradienti elettrici (quindi, un gradiente elettrochimico), a causa della carica positiva degli ioni idrogeno e della loro aggregazione su un lato della membrana.
Se la membrana fosse continuamente aperta alla semplice diffusione da parte degli ioni idrogeno, gli ioni tenderebbero a diffondersi di nuovo nella matrice, spinti dalle concentrazioni che producono il loro gradiente elettrochimico. Ricorda che molti ioni non possono diffondersi attraverso le regioni non polari delle membrane fosfolipidiche senza l'ausilio di canali ionici. Analogamente, gli ioni idrogeno nello spazio della matrice possono passare attraverso la membrana mitocondriale interna solo tramite una proteina di membrana integrale chiamata ATP sintasi ( vedi in galleria ). Questa proteina complessa agisce come un piccolo generatore, fatto girare dalla forza degli ioni idrogeno che si diffondono attraverso di essa, lungo il loro gradiente elettrochimico. La rotazione di parti di questa macchina molecolare facilita l'aggiunta di un fosfato all'ADP, formando ATP, utilizzando l'energia potenziale del gradiente di ioni idrogeno .
L'ATP sintasi è una macchina molecolare complessa che utilizza un gradiente protonico (H + ) per formare ATP da ADP e fosfato inorganico (Pi)
-
Complesso I
-
Complesso II
-
Complesso II nel dettaglio
-
Ubiquinone ossidato
-
Complesso III
-
Complesso III nel dettaglio
-
Citocromo C
-
Complesso IV
-
Schema del complesso IV che agisce da pompa protonica
-
Schema generale
-
Schema della chemiosmosi
-
Schema dell'ATP-sintasi
-
Animazione 3d dell'ATP-sintasi
-
Struttura 3d dell'ATP-sintasi
-
Chemiosmosi
Video utili
[modifica | modifica sorgente]- Electron transport chain di Harvard Online - bellissimo video 3d sulla catena di trasporto e fosforilazione ossidativa
- BIOLOGIA - Lezione 19 - Fosforilazione Ossidativa | Metabolismo Cellulare di La Biologia per tutti
Il dinitrofenolo (DNP) è un "disaccoppiante" che rende la membrana mitocondriale interna "permeabile" ai protoni. È stato utilizzato fino al 1938 come farmaco per la perdita di peso. Quale effetto ti aspetteresti che il DNP avesse sul cambiamento del pH attraverso la membrana mitocondriale interna? Perché pensi che potrebbe essere un farmaco efficace per la perdita di peso?
La chemiosmosi viene utilizzata per generare il 90 percento dell'ATP prodotto durante il catabolismo aerobico del glucosio; è anche il metodo utilizzato nelle reazioni luminose della fotosintesi per sfruttare l'energia della luce solare nel processo di fotofosforilazione. Ricordiamo che la produzione di ATP tramite il processo di chemiosmosi nei mitocondri è chiamata fosforilazione ossidativa. Il risultato complessivo di queste reazioni è la produzione di ATP dall'energia degli elettroni rimossi dagli atomi di idrogeno. Questi atomi erano originariamente parte di una molecola di glucosio. Alla fine del percorso, gli elettroni vengono utilizzati per ridurre una molecola di ossigeno in ioni ossigeno. Gli elettroni extra sull'ossigeno attraggono ioni idrogeno (protoni) dal mezzo circostante e si forma acqua. Pertanto, l'ossigeno è l'accettore di elettroni finale nella catena di trasporto degli elettroni.
Esercizio
[modifica | modifica sorgente]Il cianuro inibisce la citocromo c ossidasi, un componente della catena di trasporto degli elettroni. Se si verifica un avvelenamento da cianuro, ti aspetteresti che il pH dello spazio intermembrana aumentasse o diminuisse? Quale effetto avrebbe il cianuro sulla sintesi di ATP?
Rendimento ATP
[modifica | modifica sorgente]Il numero di molecole di ATP generate dal catabolismo del glucosio varia. Ad esempio, il numero di ioni idrogeno che i complessi della catena di trasporto degli elettroni possono pompare attraverso la membrana varia tra le specie. Un'altra fonte di varianza deriva dal trasporto di elettroni attraverso le membrane dei mitocondri. (Il NADH generato dalla glicolisi non può entrare facilmente nei mitocondri.) Quindi, gli elettroni vengono raccolti all'interno dei mitocondri da NAD + o FAD + . Come hai imparato in precedenza, queste molecole FAD + possono trasportare meno ioni; di conseguenza, vengono generate meno molecole di ATP quando FAD + agisce da trasportatore. NAD + è utilizzato come trasportatore di elettroni nel fegato e FAD + agisce nel cervello.
Un altro fattore che influenza la resa delle molecole di ATP generate dal glucosio è il fatto che i composti intermedi in questi percorsi sono utilizzati anche per altri scopi. Il catabolismo del glucosio si collega ai percorsi che costruiscono o scompongono tutti gli altri composti biochimici nelle cellule e il risultato è un po' più disordinato rispetto alle situazioni ideali descritte finora. Ad esempio, gli zuccheri diversi dal glucosio vengono immessi nel percorso glicolitico per l'estrazione di energia. Inoltre, gli zuccheri a cinque atomi di carbonio che formano gli acidi nucleici sono realizzati da intermedi nella glicolisi. Alcuni amminoacidi non essenziali possono essere realizzati da intermedi sia della glicolisi che del ciclo dell'acido citrico. Anche i lipidi, come colesterolo e trigliceridi, sono realizzati da intermedi in questi percorsi e sia gli amminoacidi che i trigliceridi vengono scomposti per produrre energia attraverso questi percorsi. Nel complesso, nei sistemi viventi, questi percorsi di catabolismo del glucosio estraggono circa il 34 percento dell'energia contenuta nel glucosio, mentre il resto viene rilasciato sotto forma di calore.
Le fermentazioni
[modifica | modifica sorgente]Nella respirazione aerobica, l'accettore finale di elettroni è una molecola di ossigeno, O2 . Se si verifica la respirazione aerobica, verrà prodotto ATP utilizzando l'energia degli elettroni ad alta energia trasportati da NADH o FADH2 alla catena di trasporto degli elettroni. Se non si verifica la respirazione aerobica, il NADH deve essere riossidato a NAD + per essere riutilizzato come trasportatore di elettroni affinché il percorso glicolitico continui. Come si fa? Alcuni sistemi viventi utilizzano una molecola organica come accettore finale di elettroni. I processi che utilizzano una molecola organica per rigenerare NAD + da NADH sono collettivamente denominati fermentazione . Al contrario, in alcuni sistemi viventi, la catena di trasporto degli elettroni (ETC) utilizza una molecola inorganica come accettore finale di elettroni, che è chiamata respirazione cellulare anaerobica . Entrambi i processi consentono agli organismi di convertire l'energia per il loro utilizzo in assenza di ossigeno. Entrambi i metodi sono anaerobici, in cui gli organismi convertono l'energia per il loro utilizzo in assenza di ossigeno.
Respirazione cellulare anaerobica
[modifica | modifica sorgente]
Alcuni procarioti, tra cui alcune specie nei domini Bacteria e Archaea, utilizzano la respirazione anaerobica. Ad esempio, un gruppo di archei chiamati metanogeni riduce l'anidride carbonica in metano per ossidare il NADH. Questi microrganismi si trovano nel terreno e nei tratti digestivi dei ruminanti, come mucche e pecore. Allo stesso modo, i batteri solfato-riduttori, la maggior parte dei quali sono anaerobici, riducono il solfato in idrogeno solforato per rigenerare il NAD + dal NADH.
I batteri solfato riduttori sono la causa della colorazione nera dei sedimenti acquatici anossici , ad esempio sedimenti di fango provenienti da stagni e laghi (vedi foto a lato)
Fermentazione dell'acido lattico
[modifica | modifica sorgente]Il metodo di fermentazione utilizzato dagli animali e da alcuni batteri, come quelli presenti nello yogurt, è la fermentazione dell'acido lattico ( Figura sotto). Questo tipo di fermentazione è utilizzato di routine nei globuli rossi dei mammiferi, che non hanno mitocondri, e nei muscoli scheletrici che hanno un apporto di ossigeno insufficiente per consentire alla respirazione aerobica di continuare (vale a dire, nei muscoli utilizzati fino al punto di affaticamento). Nei muscoli, l'accumulo di acido lattico deve essere rimosso dalla circolazione sanguigna e quando l'acido lattico perde un idrogeno, il lattato risultante viene portato al fegato per un ulteriore metabolismo. Le reazioni chimiche della fermentazione dell'acido lattico sono le seguenti:
Acido piruvico + NADH ↔ acido lattico + NAD+
L'enzima utilizzato in questa reazione è la lattato deidrogenasi (LDH). La reazione può procedere in entrambe le direzioni, ma la reazione da sinistra a destra è inibita dalle condizioni acide. Un tempo si riteneva che tale accumulo di acido lattico causasse rigidità muscolare, affaticamento e indolenzimento, sebbene ricerche più recenti contestino questa ipotesi. Una volta che l'acido lattico è stato rimosso dal muscolo e fatto circolare nel fegato, può essere riconvertito in acido piruvico e ulteriormente catabolizzato per produrre energia.

Il tremetolo, un veleno metabolico presente nella pianta di serpentaria bianca, impedisce il metabolismo del lattato. Quando le mucche mangiano questa pianta, il tremetolo si concentra nel latte che producono. Gli esseri umani che consumano il latte possono ammalarsi gravemente. I sintomi di questa malattia, che includono vomito, dolore addominale e tremori, peggiorano dopo l'esercizio fisico. Perché pensi che sia così?
Fermentazione alcolica
[modifica | modifica sorgente]
Un altro processo di fermentazione familiare è la fermentazione alcolica ( Figura accanto), che produce etanolo. La prima reazione chimica della fermentazione alcolica è la seguente (la CO2 non partecipa alla seconda reazione):
acido piruvico +H+→CO2+ acetaldeide + NADH +H+→ etanolo + NAD+
La prima reazione è catalizzata dalla piruvato decarbossilasi, un enzima citoplasmatico, con un coenzima di tiamina pirofosfato (TPP, derivato dalla vitamina B1 e chiamato anche tiamina). Un gruppo carbossilico viene rimosso dall'acido piruvico, rilasciando anidride carbonica come gas. La perdita di anidride carbonica riduce la dimensione della molecola di un atomo di carbonio, producendo acetaldeide. La seconda reazione è catalizzata dall'alcol deidrogenasi per ossidare NADH a NAD + e ridurre l'acetaldeide ad etanolo. La fermentazione dell'acido piruvico da parte del lievito produce l'etanolo presente nelle bevande alcoliche. La tolleranza all'etanolo del lievito è variabile, variando da circa il 5 al 21 percento, a seconda del ceppo di lievito e delle condizioni ambientali.
Collegamenti metabolici
[modifica | modifica sorgente]
Hai imparato a conoscere il catabolismo del glucosio, che fornisce energia alle cellule viventi. Ma gli esseri viventi consumano composti organici diversi dal glucosio per nutrirsi. Come fa un panino al tacchino a finire come ATP nelle tue cellule? Ciò accade perché tutti i percorsi catabolici per carboidrati, proteine e lipidi alla fine si collegano alla glicolisi e ai percorsi del ciclo dell'acido citrico (vedi Figura accanto). I percorsi metabolici dovrebbero essere pensati come porosi e interconnessi, ovvero le sostanze entrano da altri percorsi e gli intermedi escono per altri percorsi. Questi percorsi non sono sistemi chiusi! Molti dei substrati, degli intermedi e dei prodotti in un percorso particolare sono reagenti in altri percorsi.
Collegamenti di altri zuccheri al metabolismo del glucosio
[modifica | modifica sorgente]Il glicogeno , un polimero del glucosio, è una molecola di riserva di energia negli animali. Quando è presente una quantità adeguata di ATP, il glucosio in eccesso viene immagazzinato come glicogeno sia nelle cellule epatiche che in quelle muscolari. Il glicogeno verrà idrolizzato in monomeri di glucosio 1-fosfato (G-1-P) se i livelli di zucchero nel sangue scendono. La presenza di glicogeno come fonte di glucosio consente di produrre ATP per un periodo di tempo più lungo durante l'esercizio. Il glicogeno viene scomposto in glucosio-1-fosfato (G-1-P) e convertito in glucosio-6-fosfato (G-6-P) sia nelle cellule muscolari che in quelle epatiche, e questo prodotto entra nel percorso glicolitico.
Il saccarosio è un disaccaride con una molecola di glucosio e una molecola di fruttosio legate insieme con un legame glicosidico. Il fruttosio è uno dei tre monosaccaridi "dietetici", insieme al glucosio e al galattosio (parte del disaccaride dello zucchero del latte lattosio), che vengono assorbiti direttamente nel flusso sanguigno durante la digestione. Il catabolismo sia del fruttosio che del galattosio produce lo stesso numero di molecole di ATP del glucosio.

Collegamenti delle proteine al metabolismo del glucosio
[modifica | modifica sorgente]Le proteine vengono idrolizzate da una varietà di enzimi nelle cellule. Nella maggior parte dei casi, gli amminoacidi vengono riciclati nella sintesi di nuove proteine. Tuttavia, se ci sono amminoacidi in eccesso o se il corpo è in uno stato di fame, alcuni amminoacidi verranno deviati nei percorsi del catabolismo del glucosio ( Figura 52). È molto importante notare che ogni amminoacido deve avere il suo gruppo amminico rimosso prima di entrare in questi percorsi. Il gruppo amminico viene convertito in ammoniaca. Nei mammiferi, il fegato sintetizza l'urea da due molecole di ammoniaca e una molecola di anidride carbonica. Pertanto, l'urea è il principale prodotto di scarto nei mammiferi, prodotto dall'azoto originario degli amminoacidi, e lascia il corpo nelle urine. Va notato che gli amminoacidi possono essere sintetizzati dagli intermedi e dai reagenti nel ciclo della respirazione cellulare.

Collegamenti tra metabolismo dei lipidi e del glucosio
[modifica | modifica sorgente]I lipidi collegati al percorso del glucosio includono colesterolo e trigliceridi. Il colesterolo è un lipide che contribuisce alla flessibilità della membrana cellulare ed è un precursore degli ormoni steroidei. La sintesi del colesterolo inizia con gruppi acetilici e procede in una sola direzione. Il processo non può essere invertito.
I trigliceridi, creati dal legame tra glicerolo e tre acidi grassi, sono una forma di riserva energetica a lungo termine negli animali. Gli animali possono produrre la maggior parte degli acidi grassi di cui hanno bisogno. I trigliceridi possono essere sia prodotti che scomposti attraverso parti dei percorsi del catabolismo del glucosio. Il glicerolo può essere fosforilato a glicerolo-3-fosfato, che continua attraverso la glicolisi. Gli acidi grassi vengono catabolizzati in un processo chiamato beta-ossidazione, che avviene nella matrice dei mitocondri e converte le loro catene di acidi grassi in unità a due atomi di carbonio di gruppi acetilici. I gruppi acetilici vengono raccolti dal CoA per formare acetil CoA che procede nel ciclo dell'acido citrico (Fig. 52).
La fotosintesi
[modifica | modifica sorgente]I processi metabolici in tutti gli organismi, dai batteri agli esseri umani, richiedono energia. Per ottenere questa energia, molti organismi accedono all'energia immagazzinata mangiando, cioè ingerendo altri organismi. Ma da dove ha origine l'energia immagazzinata nel cibo? Tutta questa energia può essere ricondotta alla fotosintesi.
La fotosintesi è essenziale per tutta la vita sulla terra; sia le piante che gli animali dipendono da essa. È l'unico processo biologico in grado di catturare l'energia che ha origine dalla luce solare e convertirla in composti chimici (carboidrati) che ogni organismo utilizza per alimentare il proprio metabolismo. È anche una fonte di ossigeno necessaria per molti organismi viventi. In breve, l'energia della luce solare viene "catturata" per energizzare gli elettroni, la cui energia viene poi immagazzinata nei legami covalenti delle molecole di zucchero. Quanto sono stabili e duraturi questi legami covalenti? L'energia estratta oggi dalla combustione di carbone e prodotti petroliferi rappresenta l'energia della luce solare catturata e immagazzinata dalla fotosintesi 350-200 milioni di anni fa durante il periodo carbonifero.
Le piante, le alghe e un gruppo di batteri chiamati cianobatteri sono gli unici organismi in grado di effettuare la fotosintesi ( Figura 8.2 ). Poiché utilizzano la luce per produrre il proprio cibo, sono chiamati fotoautotrofi (letteralmente, "autoalimentati tramite luce"). Altri organismi, come animali, funghi e la maggior parte degli altri batteri, sono definiti eterotrofi ("altri alimentatori"), perché devono fare affidamento sugli zuccheri prodotti dagli organismi fotosintetici per il loro fabbisogno energetico. Un terzo gruppo molto interessante di batteri sintetizza gli zuccheri, non utilizzando l'energia della luce solare, ma estraendo energia da composti chimici inorganici. Per questo motivo, sono chiamati chemioautotrofi .
-
a: piante
-
b: alghe
-
c: cianobatteri
-
Fumarola oceanica con batteri termofili
-
Organismi che vivono grazie ai batteri
-
Batterio termofilo
-
Batterio chemiosintetico
Galleria. I fotoautotrofi, tra cui (a) piante, (b) alghe e (c) cianobatteri, sintetizzano i loro composti organici tramite fotosintesi, utilizzando la luce solare come fonte di energia. I cianobatteri e le alghe planctoniche possono crescere su aree enormi nell'acqua, a volte ricoprendo completamente la superficie. In una (d) bocca di mare profondo, i chemioautotrofi, come questi (e) batteri termofili, catturano energia dai composti inorganici per produrre composti organici. L'ecosistema che circonda le bocche ha una vasta gamma di animali, come vermi tubicoli, crostacei e polpi che ricavano energia dai batteri.
L'importanza della fotosintesi non è solo la capacità di catturare l'energia della luce solare. Dopotutto, una lucertola che prende il sole in una giornata fredda può usare l'energia del sole per riscaldarsi in un processo chiamato termoregolazione comportamentale . Al contrario, la fotosintesi è fondamentale perché si è evoluta come un modo per immagazzinare l'energia dalla radiazione solare (la parte "foto-") in energia nei legami carbonio-carbonio delle molecole di carboidrati (la parte "-sintesi"). Questi carboidrati sono la fonte di energia che gli eterotrofi usano per alimentare la sintesi di ATP tramite respirazione. Pertanto, la fotosintesi alimenta il 99 percento degli ecosistemi della Terra. Quando un predatore di vertice, come un lupo, preda un cervo ( Figura sotto), il lupo si trova alla fine di un percorso energetico che è andato dalle reazioni nucleari sulla superficie del sole, alla luce visibile, alla fotosintesi, alla vegetazione, al cervo e infine al lupo.

Strutture principali e sintesi della fotosintesi
[modifica | modifica sorgente]La fotosintesi è un processo in più fasi che richiede specifiche lunghezze d'onda di luce solare visibile, anidride carbonica (che ha un basso contenuto energetico) e acqua come substrati ( Figura sotto). Una volta completato il processo, rilascia ossigeno e produce gliceraldeide-3-fosfato (G3P), così come semplici molecole di carboidrati (ad alto contenuto energetico) che possono poi essere convertite in glucosio, saccarosio o una qualsiasi delle decine di altre molecole di zucchero. Queste molecole di zucchero contengono energia e il carbonio energizzato di cui tutti gli esseri viventi hanno bisogno per sopravvivere.


Sebbene l'equazione sembri semplice, i numerosi passaggi che avvengono durante la fotosintesi sono in realtà piuttosto complessi. Prima di apprendere i dettagli di come i fotoautotrofi trasformano la luce solare in cibo, è importante familiarizzare con le strutture coinvolte.
Strutture fotosintetiche di base
[modifica | modifica sorgente]Nelle piante, la fotosintesi avviene generalmente nelle foglie, che sono composte da diversi strati di cellule. Il processo di fotosintesi avviene in uno strato intermedio chiamato mesofillo . Lo scambio di gas di anidride carbonica e ossigeno avviene attraverso piccole aperture regolate chiamate stomi (singolare: stoma), che svolgono anche un ruolo nella regolazione dello scambio di gas e dell'equilibrio idrico. Gli stomi sono in genere situati sulla parte inferiore della foglia, il che aiuta a ridurre al minimo la perdita di acqua dovuta alle alte temperature sulla superficie superiore della foglia. Ogni stoma è fiancheggiato da cellule di guardia che regolano l'apertura e la chiusura degli stomi gonfiandosi o restringendosi in risposta ai cambiamenti osmotici.
In tutti gli eucarioti autotrofi, la fotosintesi avviene all'interno di un organello chiamato cloroplasto . Per le piante, le cellule contenenti cloroplasti esistono principalmente nel mesofillo. I cloroplasti hanno un involucro a doppia membrana (composto da una membrana esterna e una membrana interna) e derivano ancestralmente da antichi cianobatteri liberi. All'interno del cloroplasto ci sono strutture impilate a forma di disco chiamate tilacoidi . Incorporata nella membrana tilacoide c'è la clorofilla, un pigmento (molecola che assorbe la luce) responsabile dell'interazione iniziale tra luce e materiale vegetale, e numerose proteine che costituiscono la catena di trasporto degli elettroni. La membrana tilacoide racchiude uno spazio interno chiamato lume tilacoide . Come mostrato nella Figura 8.6 , una pila di tilacoidi è chiamata granum , e lo spazio pieno di liquido che circonda il granum è chiamato stroma o “letto” (da non confondere con lo stoma o “bocca”, un’apertura sull’epidermide della foglia).

-
Cloroplasti nelle cellule di un muschio
-
Schema 3d di un cloroplasto
-
Nei cloroplasti si intravedono i tilacoidi
-
Cloroplasto di lattuga al microscopio a trasmissione
-
(dettaglio)
Le due parti della fotosintesi
[modifica | modifica sorgente]La fotosintesi avviene in due fasi sequenziali: le reazioni dipendenti dalla luce e le reazioni indipendenti dalla luce. Nelle reazioni dipendenti dalla luce , l'energia della luce solare viene assorbita dalla clorofilla e tale energia viene convertita in energia chimica immagazzinata. Nelle reazioni indipendenti dalla luce , l'energia chimica raccolta durante le reazioni dipendenti dalla luce guida l'assemblaggio di molecole di zucchero dall'anidride carbonica. Pertanto, sebbene le reazioni indipendenti dalla luce non utilizzino la luce come reagente, richiedono i prodotti delle reazioni dipendenti dalla luce per funzionare. Inoltre, tuttavia, diversi enzimi delle reazioni indipendenti dalla luce vengono attivati dalla luce. Le reazioni dipendenti dalla luce utilizzano determinate molecole per immagazzinare temporaneamente l'energia: queste sono chiamate trasportatori di energia . I trasportatori di energia che spostano l'energia dalle reazioni dipendenti dalla luce a quelle indipendenti dalla luce possono essere considerati "pieni" perché sono ricchi di energia. Dopo che l'energia è stata rilasciata, i trasportatori di energia "vuoti" tornano alla reazione dipendente dalla luce per ottenere più energia. La figura sotto illustra i componenti all'interno del cloroplasto dove avvengono le reazioni dipendenti e indipendenti dalla luce.

Che cosa è l'energia luminosa?
[modifica | modifica sorgente]Come può l'energia luminosa essere usata per produrre cibo? Quando una persona accende una lampada, l'energia elettrica diventa energia luminosa. Come tutte le altre forme di energia cinetica, la luce può viaggiare, cambiare forma ed essere sfruttata per svolgere lavoro. Nel caso della fotosintesi, l'energia luminosa viene convertita in energia chimica, che i fotoautotrofi usano per costruire molecole di carboidrati di base. Tuttavia, gli autotrofi usano solo alcune lunghezze d'onda specifiche della luce solare.
Il sole emette un'enorme quantità di radiazione elettromagnetica (energia solare in uno spettro che va dai raggi gamma molto corti alle onde radio molto lunghe). Gli esseri umani possono vedere solo una piccola frazione di questa energia, che chiamiamo "luce visibile". Il modo in cui viaggia l'energia solare è descritto come onde. Gli scienziati possono determinare la quantità di energia di un'onda misurandone la lunghezza d'onda (le lunghezze d'onda più corte sono più potenti di quelle più lunghe), ovvero la distanza tra punti di cresta consecutivi di un'onda. Pertanto, una singola onda viene misurata da due punti consecutivi, ad esempio da cresta a cresta o da avvallamento a avvallamento (vedi galleria).
La luce visibile costituisce solo uno dei tanti tipi di radiazione elettromagnetica emessa dal sole e da altre stelle. Gli scienziati differenziano i vari tipi di energia radiante del sole all'interno dello spettro elettromagnetico. Lo spettro elettromagnetico è la gamma di tutte le possibili frequenze di radiazione. La differenza tra le lunghezze d'onda è correlata alla quantità di energia da esse trasportata.
Ogni tipo di radiazione elettromagnetica viaggia a una lunghezza d'onda specifica. Più è lunga la lunghezza d'onda, meno energia trasporta. Le onde corte e strette trasportano più energia. Questo può sembrare illogico, ma pensatelo in termini di un pezzo di corda pesante in movimento. Ci vuole poco sforzo da parte di una persona per muovere una corda in onde lunghe e larghe. Per far muovere una corda in onde corte e strette, una persona dovrebbe applicare molta più energia.
Lo spettro elettromagnetico mostra diversi tipi di radiazioni elettromagnetiche provenienti dal sole, tra cui raggi X e raggi ultravioletti (UV). Le onde ad alta energia possono penetrare i tessuti e danneggiare le cellule e il DNA, il che spiega perché sia i raggi X che i raggi UV possono essere dannosi per gli organismi viventi.
-
La luce del Sole è fatta di onde elettromagnetiche
-
spettro elettromagnetico
-
proprietà dello spettro elettromagnetico
-
L'atmosfera lascia passare principalmente il visibile, sfruttato dalla fotosintesi
-
L'atmosfera terrestre blocca parzialmente o totalmente alcune lunghezze d'onda della radiazione elettromagnetica, ma nella luce visibile è per lo più trasparente
Assorbimento della luce
[modifica | modifica sorgente]L'energia luminosa avvia il processo di fotosintesi quando i pigmenti assorbono specifiche lunghezze d'onda di luce visibile. I pigmenti organici, sia nella retina umana che nel tilacoide dei cloroplasti, hanno una gamma ristretta di livelli di energia che possono assorbire. Livelli di energia inferiori a quelli rappresentati dalla luce rossa non sono sufficienti per elevare un elettrone orbitale a uno stato eccitato (quantico). Livelli di energia superiori a quelli della luce blu strapperanno fisicamente le molecole, in un processo chiamato sbiancamento. I nostri pigmenti retinici possono "vedere" (assorbire) solo lunghezze d'onda comprese tra 700 nm e 400 nm di luce, uno spettro che è quindi chiamato luce visibile. Per le stesse ragioni, le piante, le molecole di pigmento assorbono solo luce nell'intervallo di lunghezze d'onda compreso tra 700 nm e 400 nm; i fisiologi vegetali si riferiscono a questo intervallo per le piante come radiazione fotosinteticamente attiva.
La luce visibile percepita dagli esseri umani come luce bianca in realtà esiste in un arcobaleno di colori. Alcuni oggetti, come un prisma o una goccia d'acqua, disperdono la luce bianca per rivelare i colori all'occhio umano. La porzione di luce visibile dello spettro elettromagnetico mostra l'arcobaleno di colori, con il viola e il blu che hanno lunghezze d'onda più corte e quindi energia più elevata. All'altra estremità dello spettro, verso il rosso, le lunghezze d'onda sono più lunghe e hanno energia più bassa.

Capire i pigmenti
[modifica | modifica sorgente]Esistono diversi tipi di pigmenti, e ognuno assorbe solo specifiche lunghezze d'onda (colori) della luce visibile. I pigmenti riflettono o trasmettono le lunghezze d'onda che non possono assorbire, facendoli apparire come una miscela dei colori della luce riflessa o trasmessa.
Le clorofille e i carotenoidi sono le due principali classi di pigmenti fotosintetici presenti nelle piante e nelle alghe; ogni classe ha diversi tipi di molecole di pigmento. Ci sono cinque principali clorofille: a , b , c e d e una molecola correlata presente nei procarioti chiamata batterioclorofilla . La clorofilla a e la clorofilla b si trovano nei cloroplasti delle piante superiori e saranno al centro della seguente discussione.
Con decine di forme diverse, i carotenoidi sono un gruppo di pigmenti molto più ampio. I carotenoidi presenti nella frutta, come il rosso del pomodoro (licopene), il giallo dei semi di mais (zeaxantina) o l'arancione della buccia d'arancia (β-carotene), vengono utilizzati come pubblicità per attrarre i dispersori di semi. Nella fotosintesi, i carotenoidi funzionano come pigmenti fotosintetici che sono molecole molto efficienti per lo smaltimento dell'energia in eccesso. Quando una foglia è esposta al sole pieno, le reazioni dipendenti dalla luce sono necessarie per elaborare un'enorme quantità di energia; se tale energia non viene gestita correttamente, può causare danni significativi. Pertanto, molti carotenoidi risiedono nella membrana tilacoide, assorbono l'energia in eccesso e dissipano in modo sicuro tale energia sotto forma di calore.
Ogni tipo di pigmento può essere identificato dal modello specifico di lunghezze d'onda che assorbe dalla luce visibile: questo è definito spettro di assorbimento . Il grafico nella Figura sotto mostra gli spettri di assorbimento per la clorofilla a , la clorofilla b e un tipo di pigmento carotenoide chiamato β-carotene (che assorbe la luce blu e verde). Nota come ogni pigmento abbia un set distinto di picchi e depressioni, rivelando un modello di assorbimento altamente specifico. La clorofilla a assorbe lunghezze d'onda da entrambe le estremità dello spettro visibile (blu e rosso), ma non il verde. Poiché il verde viene riflesso o trasmesso, la clorofilla appare verde. I carotenoidi assorbono nella regione blu a lunghezza d'onda corta e riflettono le lunghezze d'onda più lunghe del giallo, del rosso e dell'arancione.

Molti organismi fotosintetici hanno una miscela di pigmenti e, utilizzando questi pigmenti, l'organismo può assorbire energia da una gamma più ampia di lunghezze d'onda. Non tutti gli organismi fotosintetici hanno pieno accesso alla luce solare. Alcuni organismi crescono sott'acqua, dove l'intensità e la qualità della luce diminuiscono e cambiano con la profondità. Altri organismi crescono in competizione per la luce. Le piante sul suolo della foresta devono essere in grado di assorbire qualsiasi briciolo di luce che passa, perché gli alberi più alti assorbono la maggior parte della luce solare e disperdono la radiazione solare rimanente (foto in galleria).
Quando studiano un organismo fotosintetico, gli scienziati possono determinare i tipi di pigmenti presenti generando spettri di assorbimento. Uno strumento chiamato spettrofotometro può distinguere quali lunghezze d'onda della luce una sostanza può assorbire. Gli spettrofotometri misurano la luce trasmessa e calcolano da essa l'assorbimento. Estraendo i pigmenti dalle foglie e inserendo questi campioni in uno spettrofotometro, gli scienziati possono identificare quali lunghezze d'onda della luce un organismo può assorbire. Altri metodi per l'identificazione dei pigmenti vegetali includono vari tipi di cromatografia che separano i pigmenti in base alle loro affinità relative alle fasi solide e mobili.
-
Le piante che comunemente crescono all'ombra si sono adattate a bassi livelli di luce modificando le concentrazioni relative dei loro pigmenti di clorofilla
-
Spettro di assorbimento della clorofilla a e b
Come funzionano le reazioni dipendenti dalla luce
[modifica | modifica sorgente]La funzione complessiva delle reazioni dipendenti dalla luce è quella di convertire l'energia solare in energia chimica sotto forma di NADPH e ATP. Questa energia chimica supporta le reazioni indipendenti dalla luce e alimenta l'assemblaggio delle molecole di zucchero. Le reazioni dipendenti dalla luce sono illustrate nella Figura 8.16 . I complessi proteici e le molecole di pigmento lavorano insieme per produrre NADPH e ATP. La numerazione dei fotosistemi deriva dall'ordine in cui sono stati scoperti, non dall'ordine del trasferimento di elettroni.

Il passaggio effettivo che converte l'energia luminosa in energia chimica avviene in un complesso multiproteico chiamato fotosistema , di cui due tipi sono incorporati nella membrana tilacoide: il fotosistema II (PSII) e il fotosistema I (PSI) ( Figura sotto). I due complessi differiscono in base a ciò che ossidano (ovvero, la fonte di fornitura di elettroni a bassa energia) e a ciò che riducono (il luogo in cui forniscono i loro elettroni energizzati).

Entrambi i fotosistemi hanno la stessa struttura di base; un certo numero di pigmenti antenna a cui sono legate le molecole di clorofilla circondano il centro di reazione dove avviene la fotochimica. Ogni fotosistema è servito dal complesso di raccolta della luce , che passa l'energia dalla luce solare al centro di reazione; è costituito da più pigmenti antenna che contengono una miscela di 300-400 molecole di clorofilla a e b , nonché altri pigmenti come i carotenoidi. L'assorbimento di un singolo fotone o di una quantità distinta o "pacchetto" di luce da parte di una qualsiasi delle clorofille spinge quella molecola in uno stato eccitato. In breve, l'energia luminosa è stata ora catturata dalle molecole biologiche ma non è ancora immagazzinata in alcuna forma utile. L'energia viene trasferita da clorofilla a clorofilla fino a quando alla fine (dopo circa un milionesimo di secondo), viene consegnata al centro di reazione. Fino a questo punto, solo l'energia è stata trasferita tra molecole, non elettroni.
Il centro di reazione contiene una coppia di molecole di clorofilla a con una proprietà speciale. Queste due clorofille possono subire ossidazione in seguito a eccitazione; possono effettivamente cedere un elettrone in un processo chiamato fotoatto . È in questa fase del centro di reazione durante la fotosintesi che l'energia luminosa viene convertita in un elettrone eccitato. Tutte le fasi successive comportano il trasferimento di quell'elettrone sul trasportatore di energia NADPH per la consegna al ciclo di Calvin dove l'elettrone viene depositato sul carbonio per l'immagazzinamento a lungo termine sotto forma di carboidrato. PSII e PSI sono due componenti principali della catena di trasporto degli elettroni fotosintetici , che include anche il complesso del citocromo . Il complesso del citocromo, un enzima composto da due complessi proteici, trasferisce gli elettroni dalla molecola trasportatrice plastochinone (Pq) alla proteina plastocianina (Pc), consentendo così sia il trasferimento di protoni attraverso la membrana tilacoide sia il trasferimento di elettroni da PSII a PSI.

Il centro di reazione del PSII (chiamato P680 ) fornisce i suoi elettroni ad alta energia, uno alla volta, all'accettore primario di elettroni e attraverso la catena di trasporto degli elettroni (Pq al complesso del citocromo alla plastocianina) al PSI. L'elettrone mancante del P680 viene sostituito estraendo un elettrone a bassa energia dall'acqua; quindi, l'acqua viene "scissa" durante questa fase della fotosintesi e il PSII viene nuovamente ridotto dopo ogni fotoatto. La scissione di una molecola di H 2 O rilascia due elettroni, due atomi di idrogeno e un atomo di ossigeno. Tuttavia, la scissione di due molecole è necessaria per formare una molecola di gas diatomico O 2 . Circa il 10 percento dell'ossigeno viene utilizzato dai mitocondri nella foglia per supportare la fosforilazione ossidativa. Il resto sfugge all'atmosfera dove viene utilizzato dagli organismi aerobici per supportare la respirazione.
Quando gli elettroni si muovono attraverso le proteine che risiedono tra PSII e PSI, perdono energia. Questa energia viene utilizzata per spostare gli atomi di idrogeno dal lato stromale della membrana al lume tilacoide. Questi atomi di idrogeno, più quelli prodotti dalla scissione dell'acqua, si accumulano nel lume tilacoide e saranno utilizzati per sintetizzare ATP in una fase successiva. Poiché gli elettroni hanno perso energia prima del loro arrivo a PSI, devono essere rienergizzati da PSI, quindi un altro fotone viene assorbito dall'antenna PSI. Tale energia viene trasmessa al centro di reazione PSI (chiamato P700 ). P700 viene ossidato e invia un elettrone ad alta energia a NADP + per formare NADPH. Pertanto, PSII cattura l'energia per creare gradienti protonici per produrre ATP e PSI cattura l'energia per ridurre NADP + in NADPH. I due fotosistemi lavorano di concerto, in parte, per garantire che la produzione di NADPH sia più o meno uguale alla produzione di ATP. Esistono altri meccanismi per mettere a punto quel rapporto in modo che corrisponda esattamente alle esigenze energetiche in continuo cambiamento del cloroplasto.
Generazione di un vettore energetico: ATP
[modifica | modifica sorgente]Come nello spazio intermembrana dei mitocondri durante la respirazione cellulare, l'accumulo di ioni idrogeno all'interno del lume tilacoide crea un gradiente di concentrazione . La diffusione passiva di ioni idrogeno da alta concentrazione (nel lume tilacoide) a bassa concentrazione (nello stroma) viene sfruttata per creare ATP, proprio come nella catena di trasporto degli elettroni della respirazione cellulare. Gli ioni accumulano energia a causa della diffusione e perché hanno tutti la stessa carica elettrica, respingendosi a vicenda.
Per rilasciare questa energia, gli ioni idrogeno si riverseranno attraverso qualsiasi apertura, in modo simile all'acqua che esce da un buco in una diga. Nel tilacoide, quell'apertura è un passaggio attraverso un canale proteico specializzato chiamato ATP-sintasi. L'energia rilasciata dal flusso di ioni idrogeno consente all'ATP sintasi di legare un terzo gruppo fosfato all'ADP, che forma una molecola di ATP ( Figura sopra). Il flusso di ioni idrogeno attraverso l'ATP sintasi è chiamato chemiosmosi perché gli ioni si spostano da un'area ad alta concentrazione a un'area a bassa concentrazione attraverso una struttura semipermeabile del tilacoide.
Dopo che l'energia del sole è stata convertita in energia chimica e temporaneamente immagazzinata in molecole di ATP e NADPH, la cellula ha il carburante necessario per costruire molecole di carboidrati per l'immagazzinamento di energia a lungo termine. I prodotti delle reazioni dipendenti dalla luce, ATP e NADPH, hanno durate di vita nell'ordine di milionesimi di secondo, mentre i prodotti delle reazioni indipendenti dalla luce (carboidrati e altre forme di carbonio ridotto) possono sopravvivere quasi indefinitamente. Le molecole di carboidrati prodotte avranno una struttura portante di atomi di carbonio. Ma da dove proviene il carbonio? Proviene dall'anidride carbonica, il gas che è un prodotto di scarto della respirazione in microbi, funghi, piante e animali.
Il ciclo di Calvin
[modifica | modifica sorgente]Nelle piante, l'anidride carbonica (CO 2 ) entra nelle foglie attraverso gli stomi, dove si diffonde su brevi distanze attraverso gli spazi intercellulari fino a raggiungere le cellule del mesofillo. Una volta nelle cellule del mesofillo, la CO 2 si diffonde nello stroma del cloroplasto, il sito delle reazioni della fotosintesi indipendenti dalla luce. Queste reazioni hanno in realtà diversi nomi associati a loro. Un altro termine, ciclo di Calvin , prende il nome dall'uomo che lo scoprì e perché queste reazioni funzionano come un ciclo. Altri lo chiamano ciclo di Calvin-Benson per includere il nome di un altro scienziato coinvolto nella sua scoperta. Il nome più obsoleto è "reazione oscura", perché la luce non è richiesta direttamente ( Figura 8.18 ). Tuttavia, il termine reazione oscura può essere fuorviante perché implica erroneamente che la reazione si verifica solo di notte o è indipendente dalla luce, motivo per cui la maggior parte degli scienziati e degli insegnanti non lo usa più.

Le reazioni indipendenti dalla luce del ciclo di Calvin possono essere organizzate in tre fasi fondamentali: fissazione, riduzione e rigenerazione.
Fase 1: Fissazione
[modifica | modifica sorgente]Nello stroma, oltre alla CO2 , sono presenti altri due componenti per avviare le reazioni indipendenti dalla luce: un enzima chiamato ribulosio-1,5-bisfosfato carbossilasi/ossigenasi (RuBisCO) e tre molecole di ribulosio bisfosfato (RuBP), come mostrato nella Figura 8.19 . RuBP ha cinque atomi di carbonio, affiancati da due fosfati.
Connessione visiva
[modifica | modifica sorgente]Figura 8.19 Il ciclo di Calvin ha tre fasi. Nella fase 1, l'enzima RuBisCO incorpora l'anidride carbonica in una molecola organica, 3-PGA. Nella fase 2, la molecola organica viene ridotta utilizzando elettroni forniti da NADPH. Nella fase 3, RuBP, la molecola che avvia il ciclo, viene rigenerata in modo che il ciclo possa continuare. Viene incorporata solo una molecola di anidride carbonica alla volta, quindi il ciclo deve essere completato tre volte per produrre una singola molecola di G3P a tre atomi di carbonio e sei volte per produrre una molecola di glucosio a sei atomi di carbonio. Credito: Rao, A., Ryan, K., Tag, A., Fletcher, S. e Hawkins, A. Department of Biology, Texas A&M University.
Quale delle seguenti affermazioni è vera?
- Nella fotosintesi, ossigeno, anidride carbonica, ATP e NADPH sono reagenti. G3P e acqua sono prodotti.
- Nella fotosintesi, clorofilla, acqua e anidride carbonica sono reagenti. G3P e ossigeno sono prodotti.
- Nella fotosintesi, acqua, anidride carbonica, ATP e NADPH sono reagenti. RuBP e ossigeno sono prodotti.
- Nella fotosintesi, l'acqua e l'anidride carbonica sono reagenti. Il G3P e l'ossigeno sono prodotti.
RuBisCO catalizza una reazione tra CO 2 e RuBP. Per ogni molecola di CO 2 che reagisce con una RuBP, si formano due molecole di un altro composto, l'acido 3-fosfoglicerico (3-PGA). Il PGA ha tre atomi di carbonio e un fosfato. Ogni giro del ciclo coinvolge solo una RuBP e un'anidride carbonica e forma due molecole di 3-PGA. Il numero di atomi di carbonio rimane lo stesso, poiché gli atomi si muovono per formare nuovi legami durante le reazioni (3 atomi di C da 3CO 2 + 15 atomi di C da 3RuBP = 18 atomi di C in 6 molecole di 3-PGA). Questo processo è chiamato fissazione del carbonio , perché la CO 2 viene "fissata" da una forma inorganica in molecole organiche.
Fase 2: Riduzione
[modifica | modifica sorgente]ATP e NADPH vengono utilizzati per convertire le sei molecole di 3-PGA in sei molecole di una sostanza chimica chiamata gliceraldeide 3-fosfato (G3P). Questa è una reazione di riduzione perché comporta l'acquisizione di elettroni da parte di 3-PGA. (Ricorda che una riduzione è l'acquisizione di un elettrone da parte di un atomo o di una molecola.) Vengono utilizzate sei molecole sia di ATP che di NADPH. Per l'ATP, l'energia viene rilasciata con la perdita dell'atomo di fosfato terminale, convertendolo in ADP; per il NADPH, vengono persi sia l'energia che un atomo di idrogeno, convertendolo in NADP + . Entrambe queste molecole ritornano alle reazioni dipendenti dalla luce vicine per essere riutilizzate e rienergizzate.
Fase 3: Rigenerazione
[modifica | modifica sorgente]È interessante notare che, a questo punto, solo una delle molecole di G3P abbandona il ciclo di Calvin e viene inviata al citoplasma per contribuire alla formazione di altri composti necessari alla pianta. Poiché il G3P esportato dal cloroplasto ha tre atomi di carbonio, ci vogliono tre "giri" del ciclo di Calvin per fissare abbastanza carbonio netto da esportare un G3P. Ma ogni giro produce due G3P, quindi tre giri producono sei G3P. Uno viene esportato mentre le restanti cinque molecole di G3P rimangono nel ciclo e vengono utilizzate per rigenerare RuBP, il che consente al sistema di prepararsi per la fissazione di più CO 2. Altre tre molecole di ATP vengono utilizzate in queste reazioni di rigenerazione.
Connessione Evoluzione
[modifica | modifica sorgente]Fotosintesi
[modifica | modifica sorgente]Durante l'evoluzione della fotosintesi, si è verificato un importante cambiamento dal tipo di fotosintesi batterica che coinvolge solo un fotosistema ed è tipicamente anossigenica (non genera ossigeno) alla moderna fotosintesi ossigenica (genera ossigeno), che impiega due fotosistemi. Questa moderna fotosintesi ossigenica è utilizzata da molti organismi, dalle foglie tropicali giganti della foresta pluviale alle minuscole cellule cianobatteriche, e il processo e i componenti di questa fotosintesi rimangono in gran parte gli stessi. I fotosistemi assorbono la luce e utilizzano catene di trasporto degli elettroni per convertire l'energia nell'energia chimica di ATP e NADH. Le successive reazioni indipendenti dalla luce assemblano quindi le molecole di carboidrati con questa energia.
Nel caldo torrido e secco del deserto, le piante devono conservare e usare ogni goccia d'acqua per sopravvivere. Poiché gli stomi devono aprirsi per consentire l'assorbimento di CO2 , l'acqua fuoriesce dalla foglia durante la fotosintesi attiva. Le piante del deserto hanno sviluppato processi per conservare l'acqua e affrontare condizioni difficili. I meccanismi per catturare e immagazzinare la CO2 consentono alle piante di adattarsi a vivere con meno acqua. Alcune piante come i cactus ( Figura sotto ) possono preparare materiali per la fotosintesi durante la notte tramite un processo temporaneo di fissazione/immagazzinamento del carbonio, perché l'apertura degli stomi in questo momento conserva l'acqua grazie alle temperature più fresche. Durante il giorno i cactus usano la CO2 catturata per la fotosintesi e mantengono chiusi i loro stomi.

Il flusso di energia
[modifica | modifica sorgente]Che l'organismo sia un batterio, una pianta o un animale, tutti gli esseri viventi accedono all'energia scomponendo carboidrati e altre molecole organiche ricche di carbonio. Ma se le piante producono molecole di carboidrati, perché dovrebbero scomporle, soprattutto quando è stato dimostrato che il gas che gli organismi rilasciano come "prodotto di scarto" (CO2 ) agisce come substrato per la formazione di altro cibo nella fotosintesi? Ricorda, gli esseri viventi hanno bisogno di energia per svolgere le funzioni vitali. Inoltre, un organismo può produrre il proprio cibo o mangiarne un altro: in entrambi i casi, il cibo deve comunque essere scomposto. Infine, nel processo di scomposizione del cibo, chiamato respirazione cellulare, gli eterotrofi rilasciano l'energia necessaria e producono "rifiuti" sotto forma di gas CO2 .
Tuttavia, in natura, non esiste nulla come lo “spreco”. Ogni singolo atomo di materia ed energia viene conservato, riciclato più e più volte all’infinito. Le sostanze cambiano forma o si spostano da un tipo di molecola all’altro, ma i loro atomi costituenti non scompaiono mai (vedi immagine sotto della giraffa)
In realtà, la CO2 non è una forma di rifiuto più di quanto l'ossigeno sia uno spreco per la fotosintesi. Entrambi sono sottoprodotti di reazioni che passano ad altre reazioni. La fotosintesi assorbe l'energia luminosa per costruire carboidrati nei cloroplasti e la respirazione cellulare aerobica rilascia energia usando l'ossigeno per metabolizzare i carboidrati nel citoplasma e nei mitocondri. Entrambi i processi usano catene di trasporto degli elettroni per catturare l'energia necessaria per guidare altre reazioni. Questi due potenti processi, la fotosintesi e la respirazione cellulare, funzionano in armonia biologica e ciclica per consentire agli organismi di accedere all'energia che sostiene la vita e che ha origine a milioni di miglia di distanza in una stella ardente che gli umani chiamano sole.


-
Schema energetico della fase luminosa
-
Ciclo di Calvin
-
L'equazione generale del ciclo di Calvin (i cerchi neri rappresentano gli atomi di carbonio)
Altri risorse
[modifica | modifica sorgente]Pagina di approfondimento su alcuni aspetti del metabolismo