Chimica per il liceo/Il laboratorio di chimica
Il laboratorio di chimica delle scuole superiori è un locale adibito alla realizzazione di esperienze di chimica, in genere non particolarmente complesse né pericolose.
Nel locale però si trovano anche strumenti e sostanze chimiche che possono comportare dei rischi, per cui bisogna, prima di partecipare ad una attività in laboratorio, effettuare una formazione specifica sulla sicurezza nel laboratorio di chimica.
La struttura generale
[modifica | modifica sorgente]Il laboratorio contiene in genere varie attrezzature:
- banco da lavoro, che ha i bordi rialzati per evitare la dispersione di liquidi, e ha al suo interno rubinetti per l'acqua, e attacchi per il gas e la corrente elettrica. Lungo il bancone si individuano delle postazioni da lavoro, dove si lavorerà in piccoli gruppi. Ogni postazione avrà a disposizione (idealmente) una presa elettrica e un attacco del gas.
- armadi per la vetreria ed altre attrezzature
- speciali armadi con aspira-vapori per stoccare le sostanze chimiche
- almeno una cappa aspirante per effettuare esperienze che emettono vapori pericolosi
- lavandino per il lavaggio e la pulizia dei materiali
- contenitori speciali per il conferimento di rifiuti chimici pericolosi
- Cappa aspirante: è un piccolo banco da lavoro rinchiuso in una cappa aspirante; serve per effettuare esperienze che sviluppano vapori tossici/irritanti.
- Frigorifero: serve per conservare prodotti deperibili.
- Dispositivi di sicurezza: estintore, kit pronto soccorso, lavaocchi e/o doccia di emergenza
-
Laboratorio chimico di un liceo
-
Postazione di lavoro di un laboratorio di chimica delle scuole superiori
-
Il bancone di un laboratorio di chimica
-
La cappa aspirante del laboratorio di chimica
-
La vetreria e i relativi accessori sono stoccati in un apposito armadio (laboratorio di chimica)
-
armadi aspiranti nel laboratorio di chimica
-
Il frigorifero nel laboratorio di chimica
-
Un lavandino del laboratorio di chimica
-
Un lavaocchi per lavare gli occhi in una situazione di emergenza
Gli strumenti
[modifica | modifica sorgente]Si precisa che tutta la vetreria utilizzata in un laboratorio di chimica è formata da vetri speciali resistenti alla corrosione di sostanze chimiche e in genere resistenti al calore. Talvolta si utilizzano contenitori di plastica.
Contenitori per fare e osservare reazioni chimiche
[modifica | modifica sorgente]- Becher: sono contenitori versatili in vetro resistente al calore, di diversi volumi, è un contenitore spesso utilizzato per fare reazioni chimiche, ma si usano anche per altri scopi.
- Provetta: è un contenitore a forma di tubo allungato, resistente al calore, permette di osservare facilmente le reazioni chimiche pur utilizzando piccole quantità di reagenti. Vengono in genere inserite in appositi porta-provette, poiché non si reggono in piedi da sole. Se necessario si possono tappare.
- Beuta: contenitore a forma conica, di diversi volumi, resistente al calore. Viene utilizzato in alternativa al becher quando è necessario tappare il contenitore. Può essere anche utilizzato per conservare per brevi periodi sostanze o miscugli.
-
Becher di varie capacità
-
Provette
-
Provette
-
Beute di varie capacità
Strumenti per miscelare
[modifica | modifica sorgente]- bacchetta di vetro: è una semplice bacchettina che permette di mescolare efficacemente i miscugli.
- miscelatore magnetico: le piastre riscaldanti possono avere anche la funzione di agitatore magnetico, in pratica fanno girare un piccolo campo magnetico e se si mettono delle barrette magnetiche all'interno del contenitore posato sulla piastra, queste girano e mescolano il contenuto; la velocità di rotazione può essere regolata.
-
Bacchetta di vetro
-
Piastra elettrica che fa anche da miscelatore magnetico (stirrer)
-
Agitatore magnetico in azione
Contenitori per conservare sostanze e miscugli
[modifica | modifica sorgente]Talvolta c'è la necessità di conservare delle sostanze/miscugli ottenuti da una reazione o da utilizzare per una attività futura. Vediamo i principali contenitori.
- Matraccio: il matraccio è lo strumento utilizzato per creare e conservare soluzioni a concentrazione nota con buona precisione. Ha una base a forma di pallone con fondo piatto e un collo stretto e lungo con una tacca che indica con precisione un certo volume. Possiede un tappo a tenuta ermetica in modo da poter conservare con sicurezza e per lungo tempo le sostanze contenute.
- Cilindri, provette, becher, beute: un po' tutti i contenitori si possono utilizzare per conservare sostanze per un breve tempo, si possono chiudere con pellicola o parafilm. Beute e provette si possono chiudere con tappo di gomma.
-
Matracci di vari volumi
-
Il matraccio ha una tacca che indica il volume della portata
Strumenti per misurare volumi di liquidi
[modifica | modifica sorgente]- Cilindro graduato: è un cilindro con delle tacche e permette di misurare volumi di liquidi con una buona precisione. Ne esistono di varie portate e sensibilità. Non sono resistenti al calore. La lettura va fatta nella parte centrale (quella più bassa) del menisco.
- Pipetta graduata: sono strumenti di piccola portata ma di elevata sensibilità. Ne esistono di varie grandezze e possono essere azionate in vario modo: il sistema più diffuso è un aspiratore detto propipetta o porcellino.
-
Cilindri graduati di diversi volumi
-
Cilindri graduati di diversi volumi
-
La lettura va fatta all'altezza della superficie inferiore del menisco
-
Pipetta graduata
-
Propipetta
-
La pipetta Pasteur è un contagocce e non misura volumi
Strumenti per misurare altri parametri
[modifica | modifica sorgente]- Bilancia da laboratorio: è una bilancia elettronica, di elevata sensibilità; serve per misurare le masse.
- Cronometro: per misurare ia durata di un fenomeno.
- Termometro: digitale o analogico, serve per misurare la temperatura.
- Piaccametro: serve per misurare il pH
-
Bilancia digitale da laboratorio
-
Cronometro
-
Il termometro usato nei laboratori di chimica
-
Piaccametro digitale
Strumenti per riscaldare
[modifica | modifica sorgente]- Piastra riscaldante: è una piastra elettrica, può avere la temperatura regolabile e un agitatore magnetico. Bisogna fare attenzione quando si usa poiché la piastra calda è indistinguibile da quella fredda.
- Becco bunsen: è un semplice bruciatore a gas, con valvola di sicurezza. Si può regolare la quantità di aria e di gas immessi in modo da ottenere diversi tipi di fiamme (riducente o ossidante). Bisogna fare attenzione al rischio ustioni e incendio. Si usa assieme ad un treppiede con retina per appoggiare sopra gli oggetti da riscaldare (becher ad esempio).
-
Piastra riscaldante (che è anche miscelatore)
-
Becco bunsen
-
A seconda della quantità d'aria immessa cambia la fiamma
-
Pinza di legno per sostenere la provetta da riscaldare
Strumenti per la separazione di miscugli
[modifica | modifica sorgente]- Distillatore: serve per separare soluzioni liquide. è formato da un bollitore che porta ad ebollizione la miscela, un tubo che raccoglie i vapori (della sostanza più volatile) e un dispositivo che raffredda i vapori in modo da condensarli ed ottenere così il componente a maggiore volatilità (anche se in realtà si ottiene una soluzione).
- Carta da filtro e imbuto: l'imbuto viene appeso ad un sostegno metallico, viene inserita la carta da filtro e sotto viene posizionato un becher. Utilizzato per separare miscugli eterogenei di solidi e liquidi (es. acqua e sabbia).
- Centrifuga: usata per separare miscugli eterogenei che si separerebbero anche per decantazione; in pratica si accelera la decantazione.
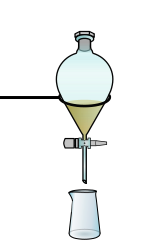
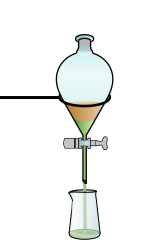
- Imbuto separatore: è un particolare contenitore a forma di pallone chiuso con un rubinetto ad una estremità, serve per separare liquidi immiscibili
-
Schema di un distillatore semplice
-
imbuto e filtro
-
Centrifuga
-
Imbuto separatore con tre liquidi immiscibili
Strumenti per la misurazione del pH
[modifica | modifica sorgente]- Cartina tornasole: è una semplice cartina da immergere nella soluzione, questa si colora e si confronta con una scala di colori, con relativo pH, presente nella scatola.
- Piaccametro: strumento digitale che permette di misurare con precisione il pH. Deve essere opportunamente tarato con una soluzione tampone.
- Indicatori di pH: particolari sostanze chimiche che assumono particolari colori o cambiano di colore a determminati pH. Ad esempio la fenolftaleina.
-
La cartina tornasole è usata per la misurazione del pH
-
Piaccametro
-
Fenolftaleina a pH 9
Accessori
[modifica | modifica sorgente]- Spatole: hanno varie forme, servono per prelevare sostanze solide dai rispettivi contenitori; possono anche essere usate per mescolare.
- Pinzette: dritte o a punta ricurva, servono per afferrare piccoli oggetti.
- Pinza in legno per provette: serve per tenere una provetta quando si mette sulla fiamma di un becco bunsen.
- Cutter o bisturi: serve per tagliare.
- Vetrino da orologio: è un piccolo contenitore aperto, utile per contenere piccole quantità di sostanze, da utilizzare nelle esperienze.
- Mortaio e pestello: per sminuzzare, polverizzare.
- Pipetta Pasteur (contagocce): serve per spostare, versare piccole quantità di liquidi
- Sostegni di metallo: serve per appendere: imbuti, burette, provette, termometri.
- Parafilm: serve per coprire abbastanza ermeticamente contenitori aperti che non si possono chiudere con un tappo.
- Pennarello: serve per scrivere sui contenitori, soprattutto se devono essere conservati per un certo tempo (una alternativa è penna e scotch di carta)
-
Vetrino da orologio
-
Pipetta pasteur (contagocce)
-
Parafilm
-
Parafilm applicato
-
Sostegni metallici per il laboratorio di chimica
-
Mortaio e pestello usati nel laboratorio di chimica
-
Spatole usate nel laboratorio di chimica
-
Pinzette usate nel laboratorio di chimica
-
Propipette di vario tipo per il laboratorio di chimica
-
Treppiede da usare col becco bunsen
Le sostanze chimiche
[modifica | modifica sorgente]Le sostanze chimiche che possono essere usare in un laboratorio sono moltissime. Non vanno MAI assaggiate, ingerite, annusate. Qui si riportano quelle più frequentemente utilizzate.
Acidi
[modifica | modifica sorgente]Sono sostanze pericolose, in quanto corrosive, irritanti e danneggiano la cute. Vanno manipolati con cautela, soprattutto se sono forti e/o concentrati. In caso di contatto lavarsi abbondantemente con acqua. Quelli più comunemente usati sono:
- acido cloridrico, solforico, nitrico, fosforico: acidi forti e pericolosi, da manipolare con cautela.
- acido acetico: pericoloso se utilizzato concentrato
-
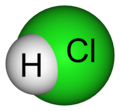
Acido cloridrico
-
La formula dell'acido cloridrico HCl
-
Acido solforico
-
Acido nitrico
Basi
[modifica | modifica sorgente]Come gli acidi, sono sostanze pericolose, in quanto corrosive, irritanti e danneggiano la cute. Vanno manipolati con cautela, soprattutto se sono di tipo forte e/o concentrati. In caso di contatto lavarsi abbondantemente con acqua. Le basi più comunemente usate sono:
- idrossido di sodio: si presenta come un sale bianco, ma spesso viene usato già in soluzione
- ammoniaca: dall'odore caratteristico e irritante.
- ipoclorito di sodio (candeggina): dall'odore caratteristico
-
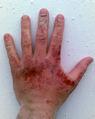
Ustione da soda caustica
-
Ammoniaca
-
Candeggina (soluzione 2,6% di ipoclorito di sodio)
Sali e altri composti
[modifica | modifica sorgente]Ne esistono di vari tipi (ossidi, idrossidi, sali binari, sali ternari), alcuni sono abbastanza innocui, altri sono pericolosi e vanno manipolati con attenzione. Non vanno mai ingeriti o assaggiati. Quelli più comunemente usati sono:
- cloruro di sodio: innocuo
- bicarbonato di sodio: abbastanza innocuo
- carbonato di calcio: innocuo
- cloruro di potassio
- solfato di rame
Composti organici
[modifica | modifica sorgente]Sono sostanze spesso cancerogene e perciò vanno utilizzate con prudenza, sotto cappa aspirante. Le più utilizzate sono:
- Idrocarburi: benzene, tetracloruro di carbonio, pentano, cicloesano: sono tutti cancerogeni.
- Alcoli: etanolo, propanolo, butanolo: non particolarmente pericolosi.
Elementi
[modifica | modifica sorgente]Si usano per lo più in granuli o in polvere o in lastrine, ad esempio:
- lastrina di magnesio
- ferro, rame, zinco in polvere
- zinco e rame in lastrine
- sodio in pezzi sotto petrolio (per evitare che si ossidi)
- Iodio: in granuli
La sicurezza
[modifica | modifica sorgente]Vedi la pagina dedicata
Approfondimento sull'uso di particolari strumenti
[modifica | modifica sorgente]L'imbuto separatore
[modifica | modifica sorgente]
L'imbuto separatore è un attrezzo da laboratorio chimico, utilizzato per estrazioni liquide, ovvero per le separazioni di miscele di liquidi con l'ausilio di una fase solvente, composta anch'essa da due differenti liquidi aventi densità diverse.
Viene utilizzato per estrarre sostanze da una soluzione: viene aggiunto un solvente che scioglie meglio la sostanza da estrarre, ma non è miscibile nella soluzione precedente. Dopo ripetute agitazioni, separazione delle fasi, drenaggio e aggiunta di solvente fresco, la sostanza da estrarre si arricchisce del nuovo solvente. (secondo il principio il simile scioglie il simile) Questa estrazione liquido-liquido , conosciuta nel gergo di laboratorio come “ shake out ”.
L'imbuto separatore ha una forma conica sormontata da una semisfera; in alto presenta un'imboccatura in vetro smerigliato di dimensioni standard (di modo tale da poter essere tappato all'occorrenza con un tappo smerigliato), mentre in basso presenta un tubo lungo e stretto, chiuso da un rubinetto in teflon o vetro. Solitamente, questi strumenti sono costruiti in pyrex, data l'inerzia chimica e la resistenza al calore di questo vetro. .
A questo punto, dato il diverso peso specifico delle due fasi solventi, si depositeranno all'interno del pallone senza miscelarsi tra loro; solitamente, la maggior parte dei solventi organici hanno una densità minore dell'acqua, quindi saranno la parte superiore della miscela stessa, mentre la parte inferiore sarà il solvente acquoso.
-
1. L'imbuto separatore viene agganciato ad un anello di supporto e riempito tramite un imbuto. Innanzitutto viene riempita la soluzione da separare (materiale estratto). Viene quindi aggiunto il solvente (estraente).
-
2. L'imbuto separatore è chiuso con un tappo adatto.
-
3. Ora è possibile rimuovere l'imbuto separatore dall'anello del supporto. L'imbuto separatore è posizionato in modo che la macinatura sia sul fondo e l'uscita sia diretta lontano dalla faccia. Il tappo è fissato a mano. Ora è possibile agitare brevemente l'imbuto separatore.
-
4. Successivamente, l'imbuto separatore deve essere sfiatato aprendo lentamente il rubinetto.
-
5. Dopo aver richiuso il rubinetto, è possibile agitare più vigorosamente l'imbuto separatore.
-
6. Dovresti quindi sfogarti di nuovo. Il processo di agitazione e sfiato deve essere ripetuto finché la pressione non si accumula più.
-
7. Successivamente è possibile riposizionare l'imbuto separatore nell'anello del supporto. Ora aspettiamo che si formino due fasi.
-
8. Quando le fasi si saranno formate è possibile rimuovere il tappo.
-
9. Le fasi vengono ora riempite individualmente in recipienti separati. Se necessario, l'intero processo deve essere ripetuto più volte con solvente fresco (estraente).
Il distillatore
[modifica | modifica sorgente]Il distillatore, o alambicco, è un apparecchio che consente la separazione di una miscela tramite l'evaporazione di uno o più componenti. La sua invenzione è attribuita al chimico islamico Jabir ibn Hayyan (tra l'VIII secolo ed il IX secolo). La distillazione viene usata sia per separare miscele complesse ottenendo in uscita 2 o più componenti, sia per purificare singole sostanze ottenendo in uscita una sostanza pura e uno scarto contenente le impurezze presenti nel componente iniziale.
Una tipica apparecchiatura di laboratorio per la distillazione è costituita dalle seguenti parti:
- un becco di Bunsen con cui si scalda la miscela da separare;
- un pallone (o caldaia) per contenere il liquido da distillare;
- una colonna di distillazione
- un tubo che convoglia i vapori al condensatore in cui vengono raffreddati;
- un termometro, montato in cima al tubo per misurare la temperatura dei vapori che vanno nel condensatore;
- uno o più palloni, o beute, per la raccolta delle varie frazioni del distillato.
In genere, si riscalda il liquido in caldaia fino all'ebollizione. Quando il termometro, il cui bulbo è posto all'altezza dell'entrata del condensatore, misura la temperatura di ebollizione del composto desiderato, si cambia pallone o beuta di raccolta in cui si raccoglie tutta la frazione che condensa a quella temperatura. Una volta che la temperatura dei vapori supera il punto di ebollizione del composto da distillare, si interrompe il riscaldamento: i liquidi più altobollenti rimarranno in caldaia e formeranno la "coda di distillazione".
È una tecnica nota sin dal Medioevo, applicata inizialmente alla produzione di bevande alcoliche. Successivamente è stata applicata in numerosi processi chimici, tra cui la separazione del petrolio grezzo nei suoi diversi componenti (detta "topping").
Il termometro
[modifica | modifica sorgente]- a mercurio: la variazione di temperatura modifica il volume del mercurio
- a gas:misura la temperatura attraverso la variazione di volume o di pressione di un gas contenuto. I termometri a gas sono molto precisi.
- digitale: usufruisce dei sensori elettrici per il calcolo della temperatura
Il Cronometro
[modifica | modifica sorgente]- Un cronometro è uno strumento che misura il tempo progettato per avere elevata accuratezza e precisione.
- Ha due pulsanti principali: uno per far partire il tempo e uno per stopparlo e resettarlo
- L'unità di misura è il secondo e la sua sensibilità è di solito il millesimo di secondo
Il cronometro viene utilizzato soprattutto nell’ambito sportivo. I cronometri sportivi sono progettati in genere per misurare il tempo a partire da un istante zero corrispondente all'inizio della gara. L'avvio e l'arresto del cronometro possono essere effettuati manualmente agendo su pulsanti oppure automaticamente. Quest'ultima soluzione, che elimina il ritardo umano, è indispensabile nelle gare di velocità, dove la vittoria o il superamento di un record sono a volte determinati dai centesimi di secondo.
Agitatore elettromagnetico
[modifica | modifica sorgente]L'agitatore elettromagnetico è uno degli strumenti di base di qualsiasi laboratorio scientifico. Viene utilizzato solitamente per mescolare efficacemente, senza l'ausilio di aste ed agitatori esterni, un solvente e uno o più soluti, o anche dei reagenti, mediante la rotazione di un'ancoretta magnetica sul fondo di un contenitore sul quale agisce un campo magnetico. La dimensione e la forma dell'ancoretta magnetica determinano l'efficacia dell'agitazione stessa a parità di velocità di agitazione. La velocità di agitazione viene solitamente regolata mediante un microprocessore ad impulsi che consente di ottenere un'ottima progressione della velocità. È opportuno quindi scegliere l'ancoretta magnetica più adeguata
in relazione alla quantità e qualità di liquido in lavorazione nonché al tipo di contenitore utilizzato. Gli agitatori magnetici spesso sono anche dotati di riscaldamento per mezzo di una resistenza elettrica posta sotto il piano d'appoggio. Le temperature che possono essere raggiunte variano da poche decine di gradi fino a 300 °C a seconda della qualità professionale dello strumento. Anche le dimensioni possono variare ed in alcuni casi si costruiscono appositamente agitatori magnetici di grosse dimensioni per contenitori di 30 o 50 litri.
Becco di Bunsen
[modifica | modifica sorgente]Il becco di Bunsen è un bruciatore a gas usato in chimica. Prende il nome da Robert Wilhelm Bunsen, il chimico e fisico tedesco al quale è erroneamente attribuita l'invenzione. Il becco di Bunsen brucia un flusso continuo di gas senza rischio che la fiamma abbia un ritorno nel tubo e giunga fino alla bombola. In genere il bruciatore usa gas naturale o, in alternativa, gas di petrolio liquefatto. Il becco di Bunsen è composto da uno zoccolo con il tubo da cui giunge il combustibile gassoso, che presenta all'estremità finale un beccuccio, e da un tubo verticale, all'imboccatura del quale viene acceso il gas. Il tubo verticale è forato in due punti per l'accesso dell'aria ed è ricoperto da un manicotto, anch'esso munito di due buchi: ruotando il manicotto si può regolare quanto i suoi buchi coincidano con quelli del tubo. In questo modo è possibile avere una maggiore o minore quantità di aria aspirata e quindi ottenere una fiamma di diversa natura, ossidante (colore blu) o riducente (colore arancio, usata anche per rendere visibile la fiamma libera quando non si usa l'apparecchio). La portata del gas è regolata invece da un'apposita vite. La fiamma raggiunge la temperatura anche di 1410 °C, pari a 1683.15 K, quando è ossidante, e si divide in diverse zone a seconda della temperatura: la base della fiamma che raggiunge i 300 °C, la zona di fusione (che si ritrova a circa 2/3 dell'altezza della fiamma) che raggiunge i 1410 °C. Al giorno d'oggi il becco di Bunsen è stato sostituito in molti utilizzi da riscaldatori elettrici che hanno il vantaggio di essere più sicuri, facilmente controllabili e di non emettere prodotti di combustione che potrebbero interagire con le reazioni. Viste le alte temperature che raggiunge bisogna stare attenti a non ustionarsi.
Approfondimento sull'uso di particolari sostanze
[modifica | modifica sorgente]Cloruro di sodio
[modifica | modifica sorgente]
Il cloruro di sodio(39.337% di sodio e 60,663% di cloro) è il sale sodico ed è il costituente principale del comune sale da cucina. A temperatura ambiente si presenta come un solido cristallino incolore e con un odore e un sapore caratteristici. I suoi cristalli hanno un reticolo cubico ai cui vertici si alternano ioni sodio Na+ e ioni cloruro Cl− Il cloruro di sodio si trova abbondantemente in natura. La maggior parte è disciolta in acqua, a formare acqua marina; in parte si trova come minerale allo stato solido in giacimenti di terraferma (in questo caso prende il nome di "salgemma"). I processi di produzione variano a seconda della forma in cui il cloruro di sodio è disponibile. è un esaltatore di sapidità ed è un ingrediente molto usato in cucina. ed è ampiamente sfruttato nell'industria conserviera sia come ingrediente sia come mezzo di conservazione dei cibi. Quest'ultima proprietà è dovuta all'effetto disidratante che il sale ha sui materiali con cui viene a contatto, da cui estrae l'acqua per osmosi. è anche un reagente usato in chimica, ad esempio per migliorare la precipitazione dei prodotti al termine di una saponificazione. Un uso importante nell'industria chimica è come materia prima negli impianti cloro-soda, in cui viene eseguita l'elettrolisi della salamoia di cloruro di sodio per ottenere cloro gassoso, idrogeno e soda caustica, tutte materie prime fondamentali per l'industria chimica. trova impiego anche come anti-gelo.
Idrossido di sodio
[modifica | modifica sorgente]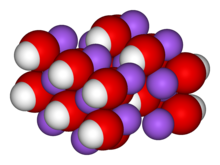
L'idrossido di sodio è una base minerale forte, solido a temperatura ambiente, estremamente igroscopico e deliquescente,venduto a perle biancastre ( o perline, pasticche) a forma di goccia; la sua formula chimica è NaOH. È molto solubile in acqua (oltre 1 kg per litro a 20 °C) ed abbastanza solubile in etanolo (139 g/l). La sua dissoluzione è accompagnata da un consistente sviluppo di calore; nel caso dell'etanolo o di altri solventi organici, tale calore può persino far infiammare i vapori del solvente. Viene conservato in recipienti sigillati perché igroscopico (tende ad assorbire l'umidità dell'aria) e perché reagisce facilmente con l'anidride carbonica dell'aria trasformandosi in idrogenocarbonato di sodio e carbonato di sodio; il fenomeno prende il nome di carbonatazione. Nell'industria chimica, è un reagente di ampio impiego; è utilizzato nella sintesi di coloranti, detergenti e saponi, nella fabbricazione della carta e nel trattamento delle fibre del cotone, nonché nella produzione dell'ipoclorito di sodio (la comune candeggina) e di altri sali sodici, quali il fosfato ed il solfuro. A livello domestico trova uso sotto forma di soluzione acquosa nei prodotti per sciogliere i grumi di prodotti organici che a volte otturano gli scarichi dei lavelli; va comunque maneggiato con una certa cautela, dato che provoca ustioni per contatto con la pelle e cecità per contatto con gli occhi. Serve anche, opportunamente diluito con acqua non dura e miscelato con grassi animali o vegetali, per preparare saponi artigianali ecologici
Acido cloridrico
[modifica | modifica sorgente]L'acido cloridrico è un idracido di formula HCl. È un acido minerale forte (ovvero si ionizza completamente in soluzione acquosa) monoprotico (cioè ogni sua molecola,dissociandosi, libera un solo ione idrogeno), ed è il principale costituente del succo gastrico, oltre a essere un reagente comunemente usato nell'industria. L'acido cloridrico, in soluzione acquosa, è uno dei liquidi più corrosivi esistenti, quindi deve essere maneggiato con attenzione. Si presenta gassoso a temperatura ambiente, incolore, dall'odore e dall'azione irritante. Viene ad esempio impiegato nel trattamento di minerali e di fosfati grezzi, compare nei processi industriali organici in veste di reagente o di sottoprodotto, viene usato nel decapaggio (operazione chimica effettuata per eliminare strati superficiali di un materiale tramite soluzioni di acido o alcali) e nel trattamento superficiale dei metalli.
Acido solforico
[modifica | modifica sorgente]L'acido solforico è un acido minerale forte, liquido a temperatura ambiente, oleoso, incolore e inodore; la sua formula chimica è H2SO4.I suoi sali vengono chiamati solfati. Un solfato molto comune è il gesso. In soluzione acquosa concentrata è noto anche con il nome di vetriolo. Solubile in acqua e in etanolo,in forma concentrata può causare gravi ustioni per contatto con la pelle. L'acido solforico ha numerose applicazioni, sia a livello di laboratorio che industriale. Tra queste si annoverano: la produzione di fertilizzanti, il trattamento dei minerali, la sintesi chimica, la raffinazione del petrolio ed il trattamento delle acque di scarico. È altresì l'acido contenuto nelle batterie per autoveicoli.
Cloruro di ferro
[modifica | modifica sorgente]
Il cloruro di ferro, o meglio detto come cloruro ferrico, è il sale di ferro dell'acido cloridrico. A temperatura ambiente si presenta come un solido giallo-bruno dall'odore di cloro. È un composto nocivo, irritante e corrode molti metalli. Il cloruro di ferro è un sale binario con formula FeCI3. Il cloruro ferrico esiste sia nella forma anidra FeCl3 che in varie forme idrate, tra le quali la più importante è quella esaidrata FeCl3 x 6H2O. Il cloruro ferrico può essere preparato sciogliendo la limatura di ferro nell'acido cloridico, ossidando la soluzione di cloruro ferroso così ottenuta con cloro oppure con acido nitrico ed evaporando.
Cloruro di calcio
[modifica | modifica sorgente]Il cloruro di calcio è un sale binario con formula chimica CaCl2 È un composto ionico formato dal catione e da due anioni. Il cloruro di calcio si presenta come una massa porosa bianca deliquescente; allo stato anidro lo si ottiene per disidratazione dell'idrato. Il sale idrato è molto diffuso in natura quale componente di minerali, acqua di mare, sorgenti salate, ecc. Il cloruro di calcio è solubile in alcool etilico, col quale forma il composto CaCl2 x 3C2H6O. il cloruro di calcio in massa spugnosa o fuso può essere impiegato anche per tenere asciutti ambienti limitati come essiccatori, per seccare diversi gas e per liberare alcuni liquidi organici dall'acqua disciolta. Le soluzioni acquose trovano impiego per bagni incongelabili, per esempio nella produzione del ghiaccio artificiale.
Idrossido di potassio
[modifica | modifica sorgente]L'idrossido di potassio o detto anche potassa caustica, è un composto corrosivo con formula chimica KOH. La sua dissoluzione in acqua è un processo fortemente esotermico, pertanto nella preparazione di una sua soluzione è d'obbligo aggiungere KOH e non vice versa. In tal modo si evita la formazione di pericolosi schizzi corrosivi. La maggior parte della produzione di idrossido di potassio viene assorbita dall'industria dei saponi e di vetri difficilmente fusibili. L'idrossido di potassio costituisce la sostanza fondamentale per molte industrie chimiche.
Bicarbonato di potassio
[modifica | modifica sorgente]Il bicarbonato di potassio (o idrogenocarbonato di potassio) è un sale di potassio dell'acido carbonico. A temperatura ambiente si presenta come un solido bianco inodore. È prodotto dalla reazione fra carbonato di potassio, biossido di carbonio e acqua: K2CO3 + CO2 + H2O → 2kHCO3 bicarbonato di potassio si trova molto raramente in natura, nel minerale kalicinite.
Acido fosforico
[modifica | modifica sorgente]L'acido fosforico, o acido ortofosforico, è un acido inorganico con la formula H3PO4. L'acido ortofosforico è un acido inorganico, corrosivo ma non tossico. Se puro, a temperatura e pressione ambiente è solido e fonde a 42,35°C in un liquido incolore viscoso. La maggior parte dell'acido fosforico prodotto è destinato alla produzione di fertilizzanti fosfatici; è inoltre una materia prima per la produzione di detergenti. Trova impiego come additivo nell'industria alimentare, in special modo nelle bevande gassate come correttore di acidità, ma non senza controversie riguardanti i suoi effetti sulla salute. L'additivo, infatti, essendo un composto chimico prodotto in massa, è disponibile a prezzi molto bassi ed in grandi quantità. L'acido fosforico è usato anche nell'odontoiatria come soluzione per pulire ed irruvidire la superficie dei denti, nelle zone in cui applicare otturazioni o apparecchi odontoiatrici. Di solito viene commercializzato in forma di soluzione acquosa concentrata fino all'80%, perché è difficile ottenerlo puro.
Acido nitrico
[modifica | modifica sorgente]L'acido nitrico è un acido minerale forte, nonché un forte agente ossidante. Liquido a temperatura ambiente, incolore quando molto puro (giallo chiaro altrimenti) e dal tipico odore irritante; la sua formula chimica è HNO3 (un atomo di idrogeno, un atomo di azoto e tre di ossigeno). I suoi sali vengono chiamati nitrati e sono pressoché tutti solubili in acqua. In soluzione concentrata (> 68%) viene detto fumante, per via della tendenza a rilasciare vapori rossastri di diossido di azoto (NO2). L'acido nitrico è uno dei principali acidi inorganici prodotti dall'industria chimica. Nel 2006 ne sono state prodotte più di 7 miliardi di tonnellate. La maggior parte dell'acido nitrico (circa il 75%) è utilizzato per la sintesi di nitrato d'ammonio , NH4NO3, usato principalmente per la produzione di fertilizzanti. Trova inoltre uso in metallurgia e nella raffinazione dei metalli, data la sua capacità di reagire con la maggior parte di essi. In miscela 1:3 con acido cloridrico concentrato forma la cosiddetta acqua regia.
Approfondimento su contenitori, reattori, miscelatori, staffe, altro
[modifica | modifica sorgente]Provette
[modifica | modifica sorgente]La provetta è un recipiente a forma di tubo di piccola dimensione di vetro o di materiale plastico chiuso sul fondo. Il fondo è arrotondato tranne che per le provette da centrifuga che sono più spesse e hanno il fondo conico. La provetta serve per analizzare le diverse sostanze e per fare reazioni chimiche. Le provette più comuni per ricerca sono in vetro chiaro, lunghe circa 80-100 mm e con un diametro di circa 8-18 mm, ma ne esistono di diverse misure e materiali a seconda dell'uso. Le provette usate per il prelievo di sangue sottovuoto sono in materiale plastico PET perché il vetro si può rompere durante la centrifugazione. Le provette sono generalmente usate nei laboratorî chimici per mettere tra loro piccole quantità di sostanze, usato e biologici per mettere in contatto tra loro piccole quantità di sostanze, per riscaldarle o per effettuare colture di microrganismi; la provetta viene usata anche per la fecondazione artificiale. Se si utilizzano sostanze tossiche o irritanti è opportuno utilizzare i dispositivi di protezione personale come i guanti o il camice.
Contagocce
[modifica | modifica sorgente]La pipetta Pasteur è un attrezzo ideato da Louis Pasteur, normalmente denominato contagocce; essa è formata da un tubicino vitreo abbastanza sottile sulla cui sommità, più larga rispetto alla parte inferiore che è quasi un capillare, si trova una tettarella in gomma. Il funzionamento della pipetta Pasteur consiste nello schiacciare la tettarella in modo da provocare l'uscita dell'aria contenuta nel tubicino, e nell' immergere quest'ultimo nel liquido, conservando compressa la parte in gomma: rilasciandola si provocherà uno scompenso di pressione per effetto del quale il liquido salirà nel tubicino e non potrà più uscirne fino a quando la tettarella non sarà nuovamente schiacciata. Malgrado la sua semplicità di utilizzo, la pipetta Pasteur non può essere adoperata come strumento di precisione se è priva di una scala graduata, ma vi sono anche quelle graduate. Essa è spesso utilizzata con funzione qualitativa e non quantitativa in cui è importante solo la natura dei reagenti e non la loro quantità di sostanza.
Pallone
[modifica | modifica sorgente]Il pallone è un recipiente utilizzato in chimica per la distillazione e come contenitore in cui eseguire reazioni. Viene anche utilizzato in laboratorio per raccogliere sostanze allo stato gassoso, grazie alla sua forma che meglio sopporta la pressione. Non serve a misurare volumi di acqua in quanto non è graduato. Ha la base sferica ed il collo cilindrico, ed esistono palloni a più colli comunemente da due o da tre. I più comuni sono in vetro chiaro e sono graduati. Le dimensioni, sia del collo che della base, possono variare. Il collo ha un diametro che va da 1 cm fino a 3 cm. La base può contenere da pochi ml fino a diversi litri.
Approfondimento sugli strumenti per misurare i volumi
[modifica | modifica sorgente]Cilindro graduato
[modifica | modifica sorgente]Il cilindro graduato è uno strumento per le misure di volume (generalmente di liquidi, ma può essere utilizzato anche per sabbie, farine, ecc.) usato da chimici e biologi in diverse attività di laboratorio. Si tratta di un tubo con un'estremità chiusa dotata di supporto e l'altra aperta con un piccolo beccuccio per facilitare le operazioni di travaso. Tutti i cilindri graduati indicano (generalmente alla loro base) l'unità di misura utilizzata. Lungo il tubo vi sono delle tacche numerate. Il volume del liquido in esso contenuto è pari alla quantità indicata a fianco dell'ultima tacca raggiunta dal liquido stesso. Cosicché, se ad esempio il liquido raggiunge la tacca contrassegnata con 7 in un cilindro indicante come unità di misura cL, avremo che il volume relativo è pari a 7 centilitri, ovvero 7 centesimi di litro. Il cilindro graduato è fatto generalmente di vetro borosilicato o polipropilene o polimetilpentene e per la sua praticità, semplicità ed economicità è molto utilizzato nei laboratori scolastici. Ne esistono anche varianti incamiciate, nella cui camicia far scorrere liquidi (generalmente acqua) a temperatura controllata, per poter effettuare misure di densità tramite densimetro a temperature esattamente
Becher
[modifica | modifica sorgente]becher è un diffuso strumento in vetro utilizzato nei laboratori chimici generalmente come recipiente. È generalmente di vetro o di vetro borosilicato che permette l'utilizzo a temperature elevate. Sono diffusi anche becher in materie plastiche come il polipropilene o il polimetilpentene. È di forma cilindrica con un beccuccio, di varia capacità e generalmente si trova tarato o graduato, anche se, a causa del diametro piuttosto grande, le graduazioni vengono utilizzate solo a scopo indicativo.
Serve soprattutto a raccogliere liquidi, sciogliere sostanze e creare soluzioni.
Il nome becher deriva dal termine tedesco Becher che indica un contenitore cilindrico.
Pallone
[modifica | modifica sorgente]Il pallone è un recipiente utilizzato in chimica per la distillazione e come contenitore in cui eseguire reazioni. Viene anche utilizzato in laboratorio per raccogliere sostanze allo stato gassoso, grazie alla sua forma che meglio sopporta la pressione. Ha la base sferica ed il collo cilindrico, ed esistono palloni a più colli,comunemente da due o da tre. I più comuni sono in vetro chiaro e sono graduati. Le dimensioni, sia del collo che della base, possono variare. Il collo ha un diametro che va da 1 cm fino a 3 cm. La base può contenere da pochi ml fino a diversi litri.
Matraccio
[modifica | modifica sorgente]Il matraccio è un contenitore, generalmente di vetro, di forma sferica oppure conica e fondo piano, di diversa capacità, usato nelle operazioni di chimica. Il matraccio tronco-conico è noto anche con il nome di beuta. Essi possono essere anche tarati, cioè contenere ad una data temperatura un volume determinato di liquido.
Provvisti di tappo ermetico, sono contenitori il cui volume è fisso ed indicato da una tacca sul collo. Vengono usati per la preparazione di soluzioni a titolo noto. Vengono utilizzati anche per diluire campioni ad un volume esatto desiderato nella chimica analitica quantitativa. Le capacità più comuni dei matracci sono: 50, 100, 200, 250, 500 e 1000 millilitri, ma ne esistono sia di più capienti, che di enormemente più capienti.
Sono tarati per "riempimento" e generalmente, oltre al volume di taratura, vengono indicate sul matraccio la tolleranza di misura del volume (accuratezza, osensibilità) e la temperatura alla quale la taratura è stata effettuata (normalmente 20°C).
Per portare a volume la soluzione in un matraccio occorre riempirlo fino a quando il menisco inferiore della soluzione di riempimento diventa tangente alla tacca di misura tracciata sul collo del matraccio stesso.
Beuta
[modifica | modifica sorgente]La forma e il collo stretto permettono di agitarne il contenuto senza spanderlo, caratteristica che la rende di uso ottimale nell'ambito delle titolazioni .In microbiologia sono utilizzate nella produzione di colture microbiche. Le beute possono essere comodamente tappate utilizzando una pellicola o un tappo di gomma Generalmente è prodotta in vetro chiaro, ma ne esistono anche in vetro scuro o materiale plastico. Le beute in vetro Pyrex possono essere poste a riscaldare in contatto con la fiamma di un becco Bunsen, utilizzando un treppiede.
Buretta
[modifica | modifica sorgente]La buretta è uno strumento di misura utilizzato nei laboratori chimici per il dosaggio accurato di volumi dei liquidi.Viene utilizzata di solito nelle titolazioni ed in prove sperimentali, nelle quali sia necessario dosare un liquido. È formata da un tubo di vetro graduato ,ad una estremità è presente un'apertura dall'altra un rubinetto. Da una parte è presente la gradazione.Le burette sono classificate per accuratezza: una buretta di classe A è accurata fino ad 1/20 di millilitro (±0,05 mL), mentre una di classe B è accurata fino al 1/10 di millilitro.
La buretta viene "avvinata" con la soluzione che si andrà ad immettere nella buretta. Si procede poi con il riempimento, caricando la buretta dall'alto, spesso tenendola inclinata per far scorrere il liquido in modo che non si catturino bolle d'aria al suo interno. Nel restringimento in fondo alla buretta possono formarsi bolle d'aria che è necessario eliminare.si procede quindi all'azzeramento della buretta. Deve poi essere posizionata in verticale e fissata con l'apposito sostegno. Agendo sul rubinetto si eroga un volume di liquido esattamente misurato. Questo deve essere azionato con la mano sinistra mentre con la destra si maneggia il contenitore che riceve il liquido, sostenendolo e facendolo oscillare per facilitare il mescolamento. Dopo ogni utilizzo deve essere lavata accuratamente e fatta asciugare per bene, smontando il rubinetto se necessari.
Pipette graduate
[modifica | modifica sorgente]La pipetta è uno strumento da laboratorio mediante il quale è possibile prelevare quantità definite o non definite di un liquido. Ne esistono di varie forme e dimensioni e possono essere in materiale plastico o in vetro Le pipette graduate, presentano una scala graduata che permette di misurare la quantità esatta di liquido prelevato. Nella misura è prevista dal costruttore una tolleranza, o errore sistematico, che ne inficia la precisione e che è funzione di vari fattori, come il grado di precisione della scala graduata, la capienza della pipetta, la tipologia di materiale usato. La lettura della misura sulla scala graduata va inoltre incontro ad un errore dovuto alla precisione dell'operatore, sebbene siano state convenzionalmente adottate delle convenzionali modalità di lettura della scala (la cosiddetta lettura del menisco). Le pipette classiche di vetro esistono principalmente di 3 tipi: graduata come quella nella foto, tarata a scolamento e tarata a 2 tacche. Le pipette tarate non presentano la graduazione, ma solo l'indicazione della portata massima: sono del tipo "a scolamento" se il volume (portata) è compreso tra la tacca e la punta, sono del tipo tarata "a due tacche" se il volume (portata) è compresa tra la tacca e una seconda tacca a 1-2 cm dalla punta. Questo genere di pipette necessitano, per il loro funzionamento, di particolari aspiratori/dosatori, che si applicano sull'estremità superiore dello strumento. Tra essi, il più diffuso è stato a lungo la pompetta a tre valvole (chiamata anche Palla di Peleo, "propipetta" o "porcellino"), che ancora si trova in molti laboratori. Da qualche anno sono stati introdotti in commercio degli aspiratori più funzionali, che vanno rimpiazzando le pompette sopracitate. In biologia cellulare vengono utilizzate delle pipette automatiche per volumi di liquido molto piccoli dell'ordine del microlitro( μL), chiamate appunto micropipette