Chimica organica/Amminoacidi
Descrizione generale
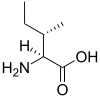
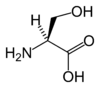
[modifica | modifica sorgente]Dal punto di vista chimico un amminoacido è una molecola contenente sia una funzione amminica che una acida, comunemente rappresentata da un gruppo carbossilico. In biochimica, e in gran parte di questo testo, con il termine di amminoacido ci si riferisce agli α-amminoacidi, la cui formula generale è

|

|
Dove la catena indicata con la "R", detta catena laterale, determina il nome di fantasia dell'amminoacido. Ad esempio, quando la catena laterale è rappresentata da un CH3 l'amminoacido si chiama alanina. La prolina rappresenta una eccezione rispetto alla formula generale proposta poiché il gruppo NH2 è sostituito dalla chiusura a ciclo del gruppo "R". La lettera α si riferisce al fatto che il carbonio che regge il gruppo amminico è direttamente legato al gruppo carbossilico. Se si frapponese un ulteriore carbonio si parlerebbe di β-amminoacidi. Gli α-amminoacidi differiscono per la catena R unita al carbonio α, detta catena laterale, che può essere polare, non polare, caratterizzata da un anello aromatico o da altri gruppi funzionali. Gli amminoacidi possono formare catene polimeriche, i peptidi, che prendono il nome di proteine se costituite da almeno 50-100 residui amminoacidici. L'ordine con il quale appaiono all'interno delle proteine è codificato, per 20 di questi, detti standard o proteogenici, a livello genetico. Altri amminoacidi facenti parte delle proteine sono formati a partire da quelli codificati. Altri ancora non entrano a far parte delle proteine, ma rivestono altri importanti ruoli metabolici. Le prossime 3 sezioni descrivono gli amminoacidi facenti parte di questi 3 gruppi.
Chiralità degli amminoacidi
[modifica | modifica sorgente]| Gli amminoacidi, con l'eccezione della glicina, esistono come coppia di enantiomeri, identificati con D e L, come gli zuccheri. Le proteine sono solitamente formate da L amminoacidi. gli amminoacidi D si trovano in alcune proteine prodotte da alcuni microrganismi marini.[1]
È utile ripetere che L e D non si riferiscono alla attività ottica degli amminoacidi, ma a quella degli enantiomeri della gliceraldeide caratterizzati dalla loro stessa chiralità. Poiché la S-Gliceraldeide è levogira e la R-gliceraldeide è destrogira, gli amminoacidi S sono definiti L, gli R sono definiti D.
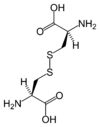
La non sistematicità della nomenclatura D-L da problemi nel caso della cisteina. Lo zolfo presente nella sua catena laterale, per le regole della priorità di Chan Ingold e Prelog, fa si che la lettera D identifichi l'enantiomero S, la lettera L identifica quello R. |
|
Struttura degli amminoacidi ...
[modifica | modifica sorgente]... proteici codificati nel DNA
[modifica | modifica sorgente]Le tabelle seguenti descrivono i 20 amminoacidi codificati nel codice genetico al fine della sintesi proteica, suddividendoli in base al tipo di catena legata al carbonio alfa. Di ciascuno sono specificati, oltre al nome,
- il simbolo convenzionale ad una lettera
- il simbolo convenzionale a tre lettere
- il peso molecolare in Dalton
- il punto isoelettrico (pI)
- la costante di dissociazione acida del gruppo carbossilico (pK1)
- la costante di dissociazione acida del sale del gruppo amminico (pK2)
- la costante di dissociazione acida del gruppo R (pKr), dove applicabile
Per l'essere umano l'OMS considera essenziali, cioè da introdurre con la dieta, alcuni degli amminoacidi descritti di seguito. Questi saranno evidenziati con l'apice "e"
| Catena contenente S (Neutri, polari o apolari) | |||
|---|---|---|---|

|

| ||
| Nome | L-Cisteina | L-Metionina e | |
| Abbr | (Cys / C) | (Met / M) | |
| Massa | 121.16 | 149.21 | |
| PI | 5.05 | 5.74 | |
| pK1 | 1.92 | 2.13 | |
| pK2 | 10.70 | 9.28 | |
| pKr | 8.37 | ||
| Note | Polare | Apolare | |
... proteici non codificati nel DNA
[modifica | modifica sorgente]Alcuni amminoacidi sono presenti nelle proteine ma non codificati nel codice genetico, poiché sintetizzati dopo la costruzione della catena poliammidica. La tabella sotto ne riporta le caratteristiche
... non proteici
[modifica | modifica sorgente]In natura si contano ad oggi circa 200 aminoacidi, oltre ai 20 codificati nel DNA e a quelli più o meno comuni presenti nelle proteine. Essi sono comunque estremamente importanti poiché
- precursori o intermedi del metabolismo
- parte di macromolecole importanti non proteiche
- agenti chimici per la trasmissione dell'impulso nervoso
- presenti nelle piante
La tabella sotto ne riporta le caratteristiche di alcuni

|

|

| |||||||||
| Nome | L-Omocisteina | L-Citrullina | L-Tiroxina | β-Alanina | (GABA) Acido-γ- Amminobutirrico |
acido (2S)-2amino- esa-4,5-dienoico | |||||
L'acido (2S)-2amino-esa-4,5-dienoico è una delle tossine prodotte dai funghi della famiglia delle Amanitacee. Questa e altre tossine prodotte dalle amanitacee sono state impiegate in passato come allucinogeni, dagli usi imprevedibili e affascinanti riassunti da questa interessante pagina.
Proprietà acido-base degli amminoacidi
[modifica | modifica sorgente]Forma Zwitterionica
[modifica | modifica sorgente]
Gli amminoacidi sono sostanze anfotere, che contengono cioè sia una funzione acida (carbossilica) che una basica (amminica). Al punto isoelettrico non sono presenti come specie neutre, bensì come ioni dipolari, cioè composti neutri aventi cariche elettriche formali unitarie di segno opposto [2] (detti anche zwitterioni, dal tedesco zwitter, ibrido) originati dalla reazione acido base intramolecolare tra il gruppo carbossilico e amminico. Esistono alcune evidenze sperimentali che dimostrano come l'equilibrio tra forma senza separazione di carica e ione dipolare sia spostato verso quest'ultimo.
- Gli amminoacidi sono insolubili in solventi organici (apolari)
- Hanno elevati punti di fusione
- Hanno elevati momenti dipolari
- Le costanti acido-base sono in accordo con la forma zwitterionica. A proposito di quest'ultimo punto è da notare come il valore tipico per la costante di acidità del gruppo carbossilico intorno a 10-5 (Ka acido acetico 1.8E-5), mentre il valore tipico per la costante di basicità del gruppo amminico sia intorno a 10-4 (Kb 1.8E-5). Poiché a comportarsi da acido e da base sono invece rispettivamente NH3+ e COO-, i valori di Ka e Kb per, ad esempio, l'Alanina sono rispettivamente 2.05E-10 e 2.24E-12.
Titolazione di un amminoacido con catena laterale non ionizzabile
[modifica | modifica sorgente]
Da sinistra a destra:
- A sinistra del punto 1: immaginiamo di aver acidificato una soluzione 1 molare di alanina così tanto da aver causato la protonazione nel 100% delle molecole sia della funzione amminica che di quella carbossilica (forma cationica). Aggiungendo una base forte poco alla volta deprotoniamo la funzione carbossilica (più acida della amminica)
- Punto 1: L'aggiunta di mezza mole di base forte fa si che mezza mole di foma cationica dia mezza mole di ione dipolare. Il pH della soluzione è pari alla pKa1
- Punto 2: Dopo l'aggiunta di 1 mole di base forte tutta la forma cationica si è trasformata in ione dipolare. Siamo al punto isoelettrico, cioè al pH al quale numero di cariche positive e negative si equivalgono. In tale condizione la solubilità dell'amminoacido in solventi polari (acqua, tipicamente) è minima. Ora il pH della suluzione è dato dalla media tra pKa1 e pKa2. Per una dimostrazione del motivo si vedano l'equazione di Henderson-Hasselbalch e la definizione di punto isoelettrico nella versione italiana di wikipedia.
- Punto 3: L'aggiunta di una ulteriore mezza mole di base forte trasforma mezza mole di ione dipolare nella forma anionica. Ora il pH è pari alla Ka2.
- Oltre il punto 3: una ulteriore aggiunta di base forte fa progressivamente aumentae la concentrazione della forma anionica a scapito delle altre 2.
Acidità e basicità delle funzioni carbossiliche e amminiche
[modifica | modifica sorgente]- Il pKa medio del gruppo carbossilico in alfa al gruppo amminico è pari a 2.19 , contro una pKa di 4.76 per l'acido acetico. Questa maggiore forza è interpretabile con la vicinanza del gruppo amminico, ad attrazione elettronica poiché protonato. La stessa considerazione vale per i gruppi carbossilici presenti nella catena laterale. In effetti è interessante notare come l'acidità di tali gruppi paia inversamente proporzionale alla vicinanza al gruppo amminico.
- L'acidità del gruppo amminico è comparabile a quella di uno ione alchilammonio primario.
- I due gruppi amminici della lisina presentano costanti di acidità che paiono dipendere dalla vicinanza al carbonio carbossilico, caratterizzato da una parziale carica positiva. Per avere un riferimento è possibile considerare che la pKa dello ione ammonio è 9.3, mentre la pKa della metilammina è 10.64 e quella della dimetilammina è 10.71)
- La basicità della catena laterale dell'arginina è decisamente superiore a quella di una ammina alifatica. Se si protona l'azoto ammidico la donazione di una coppia di non legame da parte dell'azoto amminco rende possibile la scrittura di una struttura di risonanza, che fa intuire come la carica positiva che si ha per protonazione sia delocalizzata.
Amminoacidi negli alimenti
[modifica | modifica sorgente]- Ammine biogene
Secondo la review di Bodmerl et. al.[3] una ammina biogena è una base organica azotata di basso peso molecolare, di solito formata negli alimenti dalla decarbossilazione di amminoacidi liberi. Da questa origine dipende anche il loro nome: l'istamina, ad esempio, è formata dalla decarbossilazione dell'istidina. Questa stessa review è molto utile per avere una idea di quali siano le fonti principali di ammine biogene negli alimenti e di come si possa trattare un alimento per contenerne la concentrazione.
Bibliografia
[modifica | modifica sorgente]- ↑ Pisarewicz K, Mora D, Pflueger F, Fields G, Marí F. Polypeptide chains containing D-gamma-hydroxyvaline. J Am Chem Soc, 127(17), 6207-15 (2005)
- ↑ Per una definizione puntuale vedi la relativa sezione dello IUPAC gold book
- ↑ S. Bodmer, C. Imark and M. Kneubühl. Biogenic amines in foods: Histamine and food processing. Inflammation Research 48(6):296-300 (1999)