Chimica organica/Sistemi Proteici
Latte
[modifica | modifica sorgente]Il latte, come l'uovo che sarà descritto in una prossima sezione, è una delle poche sostanze delle quali si nutre l'uomo che in natura ha come funzione principale proprio quella di essere un alimento. Ha inoltre la peculiarità di essere, allo stato naturale, una sospensione.
- Le Caseine
Tra le proteine che si trovano nel latte vengono indicate come caseine quelle che precipitano quando il pH del latte venga abbassato a 4.6 alla temperatura di 30 °C. Molte caratteristiche reologiche del latte dipendono dalla presenza delle caseine, sulla cui struttura è giusto dunque spendere qualche parola. Horne [1] indica come col termine di caseine ci si riferisca ad una famiglia di proteine, suddivisibile in αS1, aS2, β e κ caseina. Tutte le caseine sono accomunate dalla forte idrofobicità, tanto che McMahon [2] le indica come tra le proteine più idrofobiche di tutte. Le prime 3 sono caratterizzate dalla presenza di fosfoserina. La quarta è una glicoproteina descritta [3] come caratterizzata da due parti o, più propriamente, domini: uno globulare, apolare, e uno, quello contenente i residui glucidici, allungato e fortemente idrofilo. Tutte si trovano nel latte sotto forma di micelle, all'interno delle quali si trovano anche minerali, prevalentemente calcio e fosforo. Tutte queste proteine tendono fortemente ad associarsi. Le prime tre tendono a precipitare in presenza di calcio, poiché questo, alle condizioni tipiche del latte, è in grado di legarsi a gruppi fosforici di 2 caseine fosforilate. La κ-caseina non segue la stessa tendenza, sia per l'assenza di fosfoserina, sia per la repulsione elettrostatica tra i residui glicosidici, carichi negativamente a pH tipico del latte. La contemporanea presenza di tutte le caseine in ciascuna micella fa sì che la κ-caseina impedisca alle altre di aggregarsi.
- Le micelle di caseina
Il modo nel quale le caseine si aggregano all'interno del latte è oggetto di ampio dibattito. Lo schema attualmente più accettato è presentato sotto forma di disegno dal Prof. Douglas dell'università di Guelph [4] (per una review di tutti i modelli proposti ad oggi si veda il lavoro di Phadungath)[5]. Secondo tale schema la micella di caseine è pressappoco sferica, fortemente idratata e molto aperta allo scambio di acqua con la fase continua. Le catene polipeptidiche interne sono legate a dare una matrice (in inglese cross-linked) per mezzo di inclusioni di calcio fostato grandi alcuni nanometri. La κ-caseina si trova distribuita in modo pressappoco uniforme all'interno della micella, come brillantemente rivelato da Horisberger e Rouvet-Vauthey.[6] La struttura interna della micella fa sì che all'esterno si protendano segmenti poco compatti e carichi negativamente, prevalentemente a causa della presenza di κ-caseina. Tali segmenti ricordano i peli, tanto che lo strato esterno è definito in inglese hairy, "peloso". Lo strato hairy rende difficoltosa la flocculazione delle micelle grazie all'ingombro sterico e alla repulsione tra cariche dello stesso segno. A proposito di quest'ultimo aspetto è opportuno ricordare che tutti gli aggregati in soluzione acquosa la cui superficie sia carica tendono ad essere circondati da un doppio strato di ioni, descritto di nuovo con chiarezza da McMahon [2]. Quelli presenti nello strato più interno hanno carica opposta rispetto a quella della superficie dell'aggregato. Questa considerazione risulta importante nel momento in cui si studino in profondità le trasformazioni delle micelle che portano alla produzione del formaggio.
- Yogurt: consistenza e esopolisaccaridi
Alcuni articoli scritti a fini didattici, tra i quali quello di Martin et. al.[7] indicano quale sia il nesso tra principali parametri tecnologici, composizione del prodotto, e caratteristiche reologiche dello yogurt. Interessante è la morbidezza al palato conferita dai carboidrati considerati cumulativamente col termine di EsoPoliSaccaridi. "slime content").
Formaggio
[modifica | modifica sorgente]La formazione del formaggio a partire dal latte per via enzimatica avviene attraverso tre stadi:[2]proteolisi enzimatica, aggregazione e gellificazione. L'enzima chimosina ![]() , contenuto nel caglio
, contenuto nel caglio ![]() viene impiegato per la scissione del legame peptidico tra la fenilalanina 105 e la metionina 106 della κ-caseina. Questo separa il dominio idrofilo da quello apolare. Il primo va in soluzione mentre il secondo, che dopo la divisione viene chiamato para-κ-caseina, rimane nella micella. Le condizioni sono ora favorevoli perché le micelle si aggreghino.
viene impiegato per la scissione del legame peptidico tra la fenilalanina 105 e la metionina 106 della κ-caseina. Questo separa il dominio idrofilo da quello apolare. Il primo va in soluzione mentre il secondo, che dopo la divisione viene chiamato para-κ-caseina, rimane nella micella. Le condizioni sono ora favorevoli perché le micelle si aggreghino.
- La repulsione sterica tra le micelle vicine diminuisce
- La repulsione elettrostatica, dovuta almeno in parte ai residui glucidici, parimenti diminuisce.
- L'idrofobicità complessiva delle micelle risulta complessivamente aumentata, rendendo più intense le interazioni idrofobiche tra di esse.
McMahon [2] descrive brillantemente da dove derivi la spinta termodinamica alla formazione di interazioni idrofobiche in ambiente acquoso: l'interazione tra acqua e proteine introduce un certo livello di ordine nella disposizione delle molecole di acqua attorno alle proteine stesse. L'entropia del sistema risulta dunque diminuita dalla presenza di proteine. L'aggregazione delle proteine riduce il numero di interazioni tra di esse e le molecole di acqua ed è dunque favorita dal punto di vista entropico. Ricordando la relazione ΔG= ΔH-TΔS, risulta intuibile come le interazioni siano favorite da un incremento di temperatura. La diretta proporzionalità tra temperatura e intensità delle interazioni è considerata un vero e proprio carattere distintivo delle interazioni idrofobiche tra molecole presenti in ambiente acquoso. A proposito della repulsione elettrostatica tra micelle è interessante notare come un abbassamento della temperatura successivo alla fase di proteolisi enzimatica aumenti la concentrazione di Ca2+ in soluzione, liberato dal fosfato di calcio, che è in grado di compensare più efficacemente la carica negativa superficiale delle micelle, diminuita a seguito della scissione della κ-caseina, ma pur sempre presente. Nuovi ponti calcio possono inoltre stabilirsi tra micelle.
Albume
[modifica | modifica sorgente]L'abume dell'uovo di gallina è composto per circa l'86% di acqua. Del restante 14% la maggior parte è rappresentata da proteine, suddivise come riportato in tabella: [8]
| Proteine dell'albume | Albume spesso | Albume al microscopio ottico | |||
| Ovalbumina | 54% | Ovotransferrina | 12% |  |
 |
| Ovomucoide | 11% | Globuline | 8% | ||
| Lisozima | 3.5% | Ovomucina | 1.5% | ||
| Avidina | 0.6% | Altre | 10% | ||
Anche l'uovo, come il latte, di fatto si è sviluppato in natura con la funzione di alimento, cosa che probabilmente incide in modo diretto sul valore dell'uovo come nutriente per l'essere umano.
L'albume di un uovo fresco presenta 4 porzioni, distinguibili in modo chiaro per la diversa compattezza. Se un uovo viene aperto su una superficie liscia una parte dell'albume si allontana dal tuorlo, poiché più liquido ![]() . Vicino al tuorlo (e addirittura sopra, nelle uova freschissime) rimane l'albume denso
. Vicino al tuorlo (e addirittura sopra, nelle uova freschissime) rimane l'albume denso ![]() . Questo in realtà ingloba, come fosse una sacca, una seconda porzione di albume liquido, che circonda a sua volta una ultima porzione di albume denso, fotografata sopra.
. Questo in realtà ingloba, come fosse una sacca, una seconda porzione di albume liquido, che circonda a sua volta una ultima porzione di albume denso, fotografata sopra.
Tutte le proteine presenti nell'albume sono globulari, tranne l'ovomucina, chiaramente filamentosa, come rivela l'immagine sopra al microscopio ottico. È intuibile che questa proteina sia responsabile della diversa consistenza dei due tipi di albume. In effetti la sua concentrazione, pur bassa in entrambi, è maggiore in quello denso. Il dibattito sulla proteina responsabile della densità dell'albume in realtà è molto acceso, quasi infuocato, a tratti. Per una ottima review si veda il lavoro di Li-Chan.[9]
- Possibile meccanismo d'azione dell'ovomucina sulla compattezza dell'albume
È tuttavia interessante riportare almeno una opinione riguardante l'ovomucina. Se questa è responsabile della densità dell'albume, il suo meccanismo di azione non passa attraverso la formazione di legami tra filamenti (crosslinks), ma piuttosto attraverso l'ingarbugliamento tra questi, un po' come si verifica in una matassa disordinata. Questa opinione è basata sul fatto che le energie sufficienti a far perdere di consistenza all'albume denso sono troppo basse, incompatibili con la scissione di legami chimici. A dimostrazione di questo c'è un esperimento eseguito presso il Campus di Scienze degli Alimenti di Cesena, [10] al quale le immagini sotto si riferiscono. Sono state registrate le sollecitazioni trasmesse alle uova dal pianale di carico di un tir utilizzato comunemente per il loro trasporto dal luogo di produzione a quello di vendita. Tali sollecitazioni sono state ripetute su uova di vario tipo, mediante un elettroattuatore. L'effetto delle vibrazioni subite dalle uova durante il trasporto sono sufficienti a ridurre la compattezza dell'albume denso, una sorta di invecchiamento accelerato.
| Sollecitazioni: registrazione... | ... e riproduzione |

|

|

| |
| Accelerometri applicati al pianale di un camion e a uova durante un trasporto | Riproduzione di quanto registrato |
- Antimicrobici dell'albume
La porosità del guscio delle uova di gallina è tale da permettere l'ingresso di patogeni, che rappresentano un rischio per la sopravvivenza dell'embrione, oltre che per la salute di chi si nutra dell'uovo. Sono attivi tuttavia alcuni meccanismi all'interno dell'albume che ostacolano la proliferazione dei patogeni. Tra questi uno poco noto, ma in questa sede interessante, è rappresentato della compattezza stessa dell'albume. Yadav [11] descrive come sottoponendo l'albume a ultrasuoni si sia ridotta la compattezza dell'albume senza incidere sulle altre caratteristiche, riuscendo ad accrescere la proliferazione di diversi patogeni, tra i quali Salmonella.
L'ovalbumina, la proteina maggiormente presente nell'albume, può essere vista come un antimicrobico mancato. Essa appartiene alla famiglia delle serpine, proteine caratterizzate da una struttura globulare e da una sorta di estroflessione o, più propriamente, un loop. È stato dimostrato [12] che in opportune condizioni il loop può penetrare la parte globulare intrappolando e rendendo inattivi batteri.
- Cara, l'albume è impazzito
La descrizione del montaggio a neve ![]() degli albumi mediante sbattitura
degli albumi mediante sbattitura ![]() permette di introdurre alcuni concetti di carattere generale. Alla base della formazione della emulsione è la denaturazione delle proteine, causata da due meccanismi concomitanti:[13] Il rimescolamento determina forze che fanno perdere alle proteine la struttura terziaria.
permette di introdurre alcuni concetti di carattere generale. Alla base della formazione della emulsione è la denaturazione delle proteine, causata da due meccanismi concomitanti:[13] Il rimescolamento determina forze che fanno perdere alle proteine la struttura terziaria. ![]() Nella massa dell'albume viene inglobata aria. La modifica delle interazioni tra la proteina e l'ambiente circostante ne determina un riarrangiamento. In particolare la proteina che si trovi all'interfaccia tra la massa acquosa e l'aria tende ad esporre verso l'acqua le parti polari. In questo la proteina ricorda le molecole anfifiliche come i fosfolipidi. La presenza di proteine all'interfaccia acqua-aria riduce la tensione superficiale dell'acqua, stabilizzando l'emulsione. Se troppe proteine vengono denaturate l'effetto positivo della ridotta tensione superficiale è superato dalle troppo ridotte interazioni tra proteine e acqua. L'acidificazione della schiuma, solitamente per aggiunta di cremor tartaro, aumenta le interazioni proteine-acqua, stabilizzando la schiuma. La stabilizzazione si può anche ottenere per utilizzo di un contenitore di rame. La pagina di wikipedia citata sopra descrive questi due aspetti.
[14]
Nella massa dell'albume viene inglobata aria. La modifica delle interazioni tra la proteina e l'ambiente circostante ne determina un riarrangiamento. In particolare la proteina che si trovi all'interfaccia tra la massa acquosa e l'aria tende ad esporre verso l'acqua le parti polari. In questo la proteina ricorda le molecole anfifiliche come i fosfolipidi. La presenza di proteine all'interfaccia acqua-aria riduce la tensione superficiale dell'acqua, stabilizzando l'emulsione. Se troppe proteine vengono denaturate l'effetto positivo della ridotta tensione superficiale è superato dalle troppo ridotte interazioni tra proteine e acqua. L'acidificazione della schiuma, solitamente per aggiunta di cremor tartaro, aumenta le interazioni proteine-acqua, stabilizzando la schiuma. La stabilizzazione si può anche ottenere per utilizzo di un contenitore di rame. La pagina di wikipedia citata sopra descrive questi due aspetti.
[14]
Carne
[modifica | modifica sorgente] |

|

|
 | ||
Il muscolo scheletrico (di vitello) è costituito per il 60% di acqua, per il 18% di proteine e per il 22% di lipidi.
Nel muscolo scheletrico [15] può essere individuata una serie di membrane concentriche, la più esterna delle quali, che inguaina il moscolo nella sua totalità, è l'epimisio (indicato col numero 2 nella prima figura). All'interno è possibile identificare i fasci muscolari, separati dal perimisio (5). Ciascun fascio è costituito da più cellule muscolari (3), dette anche fibre, affiancate. Ciascuna cellula è avvolta dall'endomisio (6). All'interno della cellula è identificabile una membrana a 3 strati, il sarcolemma, all'interno del quale si trova il sistema contrattile del muscolo. Questo è formato dalle miofibrille, ciascuna delle quali ha un diametro di circa 1 μm. Le miofibrille sono formate da due serie di proteine intrecciate. La F-actina si estende da entrambi i lati della struttura identificata in figura col nome di "disco Z". La miosina si interseca con le catene di actina legate a due dischi Z consecutivi. L'actina ha l'aspetto di un filamento sottile mentre la miosina appare come un filamento spesso. Il loro intrecciarsi fa si che il muscolo appaia come striato, con zone più scure in corrispondenza dei filamenti di miosina (Bande A) e più chiare in corrispondenza dell'actina (bande I).
- Sorte dell'acqua nella trasformazione del muscolo in carne
La quasi totalità dell'acqua che compone il muscolo si trova all'interno delle cellule. Alla morte dell'animale si verifica una serie di processi [16] che si completa in circa 24 ore e che porta alla perdita di funzionalità delle membrane cellulari. Questo comporta la fuoriuscita del 20% circa dell'acqua citoplasmatica, che va ad occupare gli spazi tra le cellule e tra i fasci muscolari.[17] La fuoriuscita dell'acqua è favorita anche dall'avvicinamento dei filamenti di miosina a seguito della discesa del pH [18](da completare). L'acqua extracellulare (o forse più propriamente extramiofibrillare, dal momento che le membrane cellulari sono profondamente alterate) è stata recentemente visualizzata mediante tecniche di NMR imaging.[19] Da tempi più lunghi è invece noto il nesso diretto esistente tra la percentuale di acqua extracellulare e l'acqua persa per sgocciolamento durante la cottura (cooking loss). [20]
- Effetti del congelamento
L'acqua extramiofibrillare congela a temperatura superiore rispetto alla intramiofibrillare, plausibilmente a causa di minori interazione con i soluti e le proteine strutturali. Il congelamento dell'acqua extramiofibrillare richiama acqua dalle miofibrille, che si disidratano e schiacciano. Le immagini al microscopio elettronico (reference da aggiungere) mostrano infatti spazi extracellulari abnormi e strutture quasi filiformi. A queste modifiche si aggiunge il danno meccanico causato alle strutture dai cristalli di ghiaccio. Un successivo scongelamento ripristina in modo non completo la situazione oroginaria. È nozione comune infatti che la carne scongelata perda per cottura più acqua della fresca.
Pane
[modifica | modifica sorgente]| Chicco di grano | 100 g di farina integrale di grano contengono[21] | Elasticità: Schema loops & trains | ||

|
Componente | % | ||
| Carboidrati digeribili | 60.7 | Amido: 98.8% Mono e disaccaridi: 1.2% | ||
| Fibre | 9.9 | |||
| Grassi | 2.2 | |||
| Proteine | 10.6 | Albumine+globuline: 10-15% gliadine+glutenine: 85-90% | ||

| ||||
La farina bianca deriva dalla macinazione dell'endosperma del chicco di alcuni cereali. Le pareti delle cellule che lo compongono forniscono le cellulose e gli altri carboidrati insolubili. All'interno delle cellule di trovano gli amiloplasti, contenenti amido e proteine. Queste ultime possono essere suddivise in due gruppi in base alla solubilità in acqua: albumine e globuline sono solubili, gliadine e glutenine, che complessivamente costituiscono il glutine, non lo sono. Dalle caratteristiche e dalla concentrazione di queste ultime dipendono molte delle proprietà degli impasti con acqua che interessano il panificatore: da aggiuingere .
- Elasticità
L'elasticità dell'impasto è legata alle proprietà di alcune subunità delle proteine che compongono il glutine, note come HMW (high molecular weight subunits). Le subunità HMW di molecole diverse sono unite testa-coda da ponti disolfuro. Inoltre nella farina disidratata, secondo Belton, [22] tra le subunità facenti parte di proteine diverse si può stabilire una elevata quantità di legami ponte a idrogeno. Tali subunità formano così strutture simili ai fogli β, sebbene di gran lunga più disordinate, descritte schematicamente dalla figura 1 in alto. Belton identifica tali zone con il temine di "trains". Quando la farina viene idratata l'acqua rompe particolari zone dei trains, che si riarrangiano in "loops", come in figura 2. L'impastamento, inoltre, distende le glutenine aumentando l'ordine dei "trains" e aiuta le proteine ad avvolgere le camere contenenti CO2 formate dalla lievitazione ![]() . All'aumentare della idratazione, il rapporto tra loops e trains si sposta sempre più a favore dei primi, come mostra la figura 3. In seguito a trazione meccanica i loops sono in grado di estendersi e, al termine della trazione, di riacquistare la conformazione originaria, conferendo elasticità all'impasto.
. All'aumentare della idratazione, il rapporto tra loops e trains si sposta sempre più a favore dei primi, come mostra la figura 3. In seguito a trazione meccanica i loops sono in grado di estendersi e, al termine della trazione, di riacquistare la conformazione originaria, conferendo elasticità all'impasto.
- Tenacia
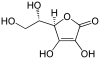
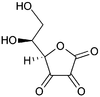
Alla tenacia dell'impasto contribuisce la formazione di ponti disolfuro tra residui di cisteina. Le sostanze ossidanti favoriscono la loro creazione. Tra queste è necessario ricordare ClO2, la cui addizione agli impasti è oggi vietata. Gli idroperossidi, formati dalla ossidazione dei lipidi, accelerano la medesima reazione, tanto che una farina invecchiata 12 mesi, dà origine ad un pane dal volume maggiore rispetto ad una farina appena macinata. Il processo Chorleywood (dal nome della cittadina dove si trova la Flour Milling and Baking Research Association che nel 1961 lo inventò) consiste nell'aggiunta di acido ascorbico seguito da una impastatura molto rapida. L'acido ascorbico si ossida a deidroascorbico.
| Acido ascorbico | Acido deidroascorbico | Glutatione | |
|
|

|
Quest'ultimo ossida il glutatione (GSH) ![]() , causandone la dimerizzazione e la conseguente inattivazione. Il glutatione è un tripeptide, che contiene un insolito legame peptidico tra il gruppo amminico di una cisteina e il gruppo carbossilico della catena laterale del glutammato. Il glutatione riduce i ponti disolfuro a cisteine agendo da donatore di elettroni, con la conseguenza di ostacolare il riarrangiamento dei legami a ponte disolfuro tipico della fase di lievitazione del pane. [23]
, causandone la dimerizzazione e la conseguente inattivazione. Il glutatione è un tripeptide, che contiene un insolito legame peptidico tra il gruppo amminico di una cisteina e il gruppo carbossilico della catena laterale del glutammato. Il glutatione riduce i ponti disolfuro a cisteine agendo da donatore di elettroni, con la conseguenza di ostacolare il riarrangiamento dei legami a ponte disolfuro tipico della fase di lievitazione del pane. [23]
- Stabilità delle bolle gassose
Per intuire quali molecole sono responsabili della stabilità delle bolle gassose è possibile osservare dove le varie molecole si collochino all'interno dell'impasto. Nelle splendide immagini realizzate da Li e altri [24] si nota che le glutenine si collocano nella massa dell'impasto, dove formano reticoli. All'interfaccia tra questa e le bolle di gas si collocano gliadine e lipidi polari. Sono queste molecole che con più probabilità hanno il compito di trattenere le bolle. Amido e lieviti sono intrappolati nel reticolo di glutenine sotto forma di inclusioni (granuli). I lipidi non polari rivestono le inclusioni oppure sono presenti sotto forma di micelle. È opportuno notare come parte delle gliadine e dei lipidi polari si inframmezzi alle glutenine nella massa dell'impasto, contribuendo probabilmente alla regolazione della elasticità.
- Viscosità
Questa parte è da completare. Tuttavia è utile sottolineare il ruolo delle gliadine nella viscosità.
Bibliografia
[modifica | modifica sorgente]- ↑ Latte: D.S. Horne. Casein structure, self-assembly and gelation. Current Opinion in Colloid & Interface Science 7:456-461 (2002)
- ↑ 2,0 2,1 2,2 2,3 Formaggio: D.J. McMahon and and R.J. Brown. Enzymic Coagulation of Casein Micelles: A Review. Journal of Dairy Science 67(5):919-929 (1984)
- ↑ Latte: H. Swaisgood. Primary Sequence of Kappa-Casein. J Dairy Sci 58:583-592 (1975)
- ↑ Latte:
 Professor H. Douglas Goff, Ph.D. at University of Guelph
Professor H. Douglas Goff, Ph.D. at University of Guelph
- ↑ Latte: C. Phadungath. Casein micelle structure: a coincise review. Songklanakarin J. Sci. Technol. 27(1):201-212 (2005).
- ↑ Latte:
 M. Horisberger and M. Rouvet-Vauthey. Localization of glycosylated κ-casein on thin sections of casein micelles by lectin-labelled gold markers. Histochemistry 80:523-526 (1984)
M. Horisberger and M. Rouvet-Vauthey. Localization of glycosylated κ-casein on thin sections of casein micelles by lectin-labelled gold markers. Histochemistry 80:523-526 (1984)
- ↑ Latte: N.C. Martin, J. Skokanova, E. Latrille, C. Beal and G. Corrieu. Influence of fermentation and storage conditions on the sensory properties of plain low fat stirred yogurt. Journal of Sensory Studies 14(2):139-160 (1999)
- ↑ Albume: w:en:Egg_white#Composition
- ↑ Albume: E. Li-Chan and S. Nakai. Biochemical basis for the properties of egg white, in Critical reviews in Poultry Biology 2(1):21-58 (1989)
- ↑ Albume: A.C. Berardinelli, M.A. Cremonini, A. Franchini, A. Giunchi, A. Guarnieri, L. Laghi, G. Placucci and L. Ragni. Effetto delle sollecitazioni meccaniche dovute al trasporto sulla qualità dell'uovo. Rivista di avicoltura 635:35-40 (2003)
- ↑ Albume: N.K. Yadav and V. Vadera Mechanism of egg white resistance to bacterial growth. Journal of Food Science 42:97-99 (1977)
- ↑ Albume: W.W. Chang, M.R. Wardell, D.A. Lomas and R.W. Carrell. Probing serpin reative-loop conformations by proteolytic cleavage. Biochem. J. 314:647-653 (1996)
- ↑ Albume: w:en:Egg_white#Creating an egg foam
- ↑ Albume: w:en:Egg_white#Creating an egg foam
- ↑ Carne: N.F.S. Gault. Structural aspects of raw meat. In: D.E. Johnston, M.K. Knight and D.A. Ledward, Editors, The chemistry of muscle based foods, The Royal Society of Chemistry, Cambridge, UK (1992), pp. 79–105
- ↑ Carne: A. Shafer, K. Rosenvold, P.P. Purslow, H.J. Andersen and P. Heckel. Physiological and structural events post mortem of importance for drip loss in pork. Meat Science 61:355-366 (2002)
- ↑ Carne: L. Laghi et al., (Still) unpublished.
- ↑ Carne: F. Guignot, X. Vignon and G. Monin. Post mortem evolution of myofilament spacing and extracellular space in veal muscle. Meat Science 33:333-347 (1993)
- ↑ Carne: H.C. Bertram, A.K. Whittaker, H.J. Andersen and A.H. Karlsson. Vsualization of drip channels in meat using NMR microimaging. Meat Science 68:667-670 (2004)
- ↑ Carne: H.C. Bertram, A.K. Whittaker, W.R. Shorthose, H.J. Andersen and A.H. Karlsson. water characteristics in cooked beef as induced by ageing and high-pressure treatment - an NMR micro imaging study. Meat Science 66:301-306 (2004)
- ↑ Pane: www.fineli.fi
- ↑ Pane: P.S. Belton. On the Elasticity of Wheat Gluten. Journal of Cereal Science 29:103-107 (1999)
- ↑ Pane: W. Grosh and H. Wieser Redox reactions in wheat dough as affected by ascorbic acid J. cereal sci. 29(1):1-16 (1999)
- ↑ Pane: W. Li, B.J. Dobraszczyk and P.J. Wilde. Surface properties and locations of gluten proteins and lipids revealed using confocal scanning laser microscopy in bread dough. Journal of Cereal Science 39(3):403-411 (2004)

