Chimica organica/Sostituzione elettrofila aromatici
I composti aromatici sono caratterizzati da una eccezionale stabilità che proviene dall'avere un guscio completo di orbitali molecolari delocalizzati. Nella loro reattività i composti aromatici sono quindi vittima di attacchi elettrofili. La specie cationica intermedia, conosciuta come indermedio di Wheland, cercherà di ripristinare il sistema aromatico, intrinsecamente stabile, o eliminando l'elettrofilo (con il che eliminando un protone, con il risultato netto di una sostituzione, invece che addizione come negli alcheni/alchini.

Questo meccanismo è noto come sostituzione elettrofila aromatica o SEAr.
La reazione procede con varî elettofili, spesso attivati da un catalizzatore, principalmente un acido di Lewis che facility la formazione del catione elettrofilo. Alcuni esempi di reattivi e catalizzatori sono riportati nella tabella seguente.
| reazione | reagenti e catalizzatori | Elettrofilo E+ | prodotto di reazione col benzene |
|---|---|---|---|
| solfonazione | H2SO4 + SO3 | HSO3+ | acido benzensolfonico Ph-SO3H |
| nitrazione | HNO3 (+ H2SO4) | NO2+ | nitrobenzene Ph-NO2 |
| nitrosazione | NaNO2 + HX | NO+ | nitrosobenzene Ph-NO |
| alogenazione | Cl2/Br2 + FeCl3 | Cl+ | cloro- /bromobenzene Ph-Cl/Ph-Br |
| alchilazione di Friedel-Crafts | R-Cl + AlCl3 | R+ | alchilbenzene Ph-R |
| acilazione di Friedel-Crafts | R-CO-Cl + AlCl3 | R-CO+ | fenil-alchil-chetone Ph-CO-R |
La reazione è accelerata dalla presenza di gruppi elettron-donatori (I+,M+) sull'anello che aumentano la carica disponibile, si dice allora che l'anello è attivato; viceversa in presenza di gruppo elettron-attrattore (I-,M-), la carica delocalizzata dell'anello è ridotta, rendendola meno reattiva. Si dice allora che l'anello è disattivato.
Il gruppo uscente è espulso perdendo un doppietto di elettroni nella sfera di valenza, e deve perciò essere una specie capace di esistere come tale. In pratica il gruppo uscente è essenzialmente il protone H+, esempi con altri gruppi essendo molto scarsi.
Effetto di direzione
[modifica | modifica sorgente]Un'altra caratteristica delle reazioni di sostituzione aromatica è l'esistenza di un effetto di direzione, cioè la presenza e la disposizione di gruppi legati all'anello aromatico dettano ove l'elettrofilo verrà a legarsi.
Le reazioni di sostituzione sono reazioni di equilibrio e l'intermedio di Wheland che si formerà in misura maggiore sarà quello termodinamicamente più stabile.
orto/para
[modifica | modifica sorgente]meta
[modifica | modifica sorgente]
Un riassunto delle proprietà attivanti e direttrici dei principali gruppi funzionali organici è presentato nella tabella seguente
| Gruppo | Effetto | Direzionalità | |
|---|---|---|---|
| -OH, -O-, -SH, -S- | attivante forte | -I +M | orto forte |
| -Cl, -Br | disattivante debole | -I +M | orto debole |
| -OR | medio attivante | +M | orto medio |
| -NO2 | forte disattivante | -I -M | meta forte |
| -F | attivante | -I +M | orto debole |
| -NH2, -NHR, -NR2 | attivante | +M | orto |
| alchili | debole attivante | +I | orto debole |
| -CF3 | disattivante forte | -I | meta debole |
| -CHO, -COOH, -COR, COOR | debole disattivante | +M | meta debole |
Sostituzione nucleofila aromatica
[modifica | modifica sorgente]Quando l'anello è altamente sostituito con gruppi elettron attrattori buoni gruppi uscenti (p.es. alogeni—tranne F—, diazonio, etc.), esso diviene elettron-deficiente e può subire attacco nucleofilo portando alla sostituzione nucleofila aromatica SNAr
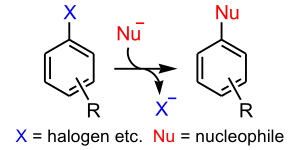
Dato che la stabilizzazione richiesta è quella di una carica negativa, gli effetti di direzione e di attivazione sono invertiti rispetto alla sostituzione elettrofila aromatica.
Il gruppo uscente è rimosso portando con sé un doppietto elettronico, e quindi un buon gruppo uscente deve poter stabilmente. Pertanto l'idrogeno non è mai sostituito in questa reazione (dovrebbe partire come ione idruro H-).
Effetto del gruppo uscente
[modifica | modifica sorgente]Nella stragrande maggioranza dei casi di sostituzione nucleofila aromatica, lo stadio lento è quello dell'addizione del nucleofilo all'anello ed è accelerato da una carica parziale positiva sul carbonio, cioè dall'elettronegatività dell'atomo (o gruppo) legato allo stesso, il che spiega l'ordine di "buon gruppo uscente" F >> Cl > Br > I. Da notare che tale ordine è invertito rispetto alla sostituzione SN2.


